Câu hỏi/bài tập:
Thành phần phần trăm về khối lượng nguyên tố có trong hợp chất X là 85,7% C và 14,3% H.
a) Xác định công thức thực nghiệm của hợp chất X.
b) Phổ MS cho thấy X có phân tử khối là 56. Xác định công thức phân tử của X.
c) Cho biết công thức cấu tạo có thể có của X trong mỗi trường hợp:
c1) X là hydrocarbon mạch thẳng. c2) X là hydrocarbon mạch hở, phân nhánh.

dựa vào phần trăm nguyên tố của hợp chất để tìm được công thức thực nghiệm của chất đó.

a) Gọi công thức phân tử của glyoxaal là CxHy.
Ta có x : y = \(\frac{{\% C}}{{12}}:\frac{{\% H}}{1}\)
Advertisements (Quảng cáo)
→ Công thức thực nghiệm: CH2
b) Theo bài ra: (CH2)n = 56 → n = 4.
Vậy công thức phân tử của X là C4H8.
c) công thức cấu tạo của X
c1) Mạch thẳng:
CH2 = CH – CH2 – CH3
CH3 – CH = CH – CH3
Trong đó: có đồng phân hình học:
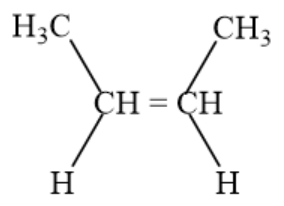
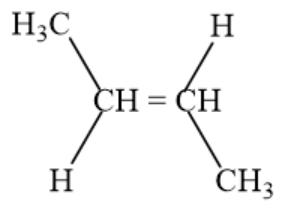
c2) mạch nhánh: CH2 = C(CH3) – CH3
