Cho cân bằng hoá học:
Cân bằng chuyển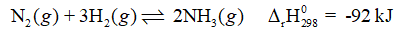 dịch theo chiều nào (có giải thích) khi:
dịch theo chiều nào (có giải thích) khi:
a) tăng nhiệt độ.
b) tách ammonia ra khỏi hỗn hợp phản ứng.
c) giảm thể tích của hệ phản ứng.

Advertisements (Quảng cáo)
Nguyên lí Le Chatelier: Một phản ứng thuận nghịch đang ở trạng thái cân bằng khi chịu một tác động từ bên ngoài như biến đổi nồng độ, áp suất, nhiệt độ thì cân bằng sẽ chuyển dịch theo chiều làm giảm tác động đó.

a) Phản ứng thuận là phản ứng tỏa nhiệt, phản ứng nghịch là phản ứng thu nhiệt. Khi tăng nhiệt độ, cân bằng chuyển dịch theo chiều làm giảm nhiệt độ (chiều tỏa nhiệt) → Cân bằng chuyển dịch theo chiều nghịch.
b) Tách ammonia ra khỏi hỗn hợp phản ứng, làm giảm nồng độ ammonia. Cân bằng chuyển dịch theo chiều làm tăng nồng độ ammonia → Cân bằng chuyển dịch theo chiều thuận.
c) Giảm thể tích của hệ phản ứng tức là tăng áp suất của hệ. Cân bằng chuyển dịch theo chiều làm giảm áp suất của hệ (chiều giảm số mol khí) → Cân bằng chuyển dịch theo chiều thuận.
