4.1
Nhà bác học Men–đê–lê–ép là người nước nào? Các nguyên tố hóa học trong bảng tuần hoàn do ông xây dựng được sắp xếp theo nguyên tắc nào?

- Năm 1869, D. I. Mendeleev – nhà bác học người Nga xây dựng bảng tuần hoàn các nguyên tố hóa học theo chiều tăng dần khối lượng nguyên tử.

Nhà bác học Men–đê–lê–ép là người nước Nga, các nguyên tố hóa học trong bảng tuần hoàn do ông xây dựng được sắp xếp theo chiều tăng dần của khối lượng nguyên tử.
4.2
Cho các cụm từ: “tăng dần khối lượng”, “tăng dần điện tích hạt nhân”, “cùng cột”, “cùng hàng”. Chọn cụm từ thích hợp điền vào các vị trí có đánh số (1), (2), (3), (4) để hoàn thành nội dung sau.
a) Bảng tuần hoàn của Men-đê-lê-ép sắp xếp theo chiều ..(1).. nguyên tử.
b) Ngày nay, bảng tuần hoàn các nguyên tố hóa học sắp xếp các nguyên tố theo chiều ..(2).. nguyên tử. Các nguyên tố ..(3).. có cùng số lớp electron trong nguyên tử, còn các nguyên tố ..(4).. có tính chất gần giống nhau.

- Năm 1869, D. I. Mendeleev – nhà bác học người Nga xây dựng bảng tuần hoàn các nguyên tố hóa học theo chiều tăng dần khối lượng nguyên tử.
- Ngày nay, bảng tuần hoàn các nguyên tố hóa học (bảng tuần hoàn) gồm 118 nguyên tố hóa học, được xây dựng theo nguyên tắc:
+ Các nguyên tố hóa học được sắp xếp theo chiều tăng dần của điện tích hạt nhân.
+ Các nguyên tố trong cùng một hàng có cùng số lớp electron trong nguyên tử.
+ Các nguyên tố trong cùng một cột có tính chất gần giống nhau.

a) Bảng tuần hoàn của Men-đê-lê-ép sắp xếp theo chiều (1) tăng dần khối lượng nguyên tử.
b) Ngày nay, bảng tuần hoàn các nguyên tố hóa học sắp xếp các nguyên tố theo chiều (2) tăng dần điện tích hạt nhân nguyên tử. Các nguyên tố (3) cùng hàng có cùng số lớp electron trong nguyên tử, còn các nguyên tố (4) cùng cột có tính chất gần giống nhau.
4.3
Phát biểu nào sau đây là đúng?
A. Bảng tuần hoàn gồm 116 nguyên tố hóa học.
B. Bảng tuần hoàn gồm 6 chu kì.
C. Bảng tuần hoàn gồm 8 nhóm A và 8 nhóm B.
D. Các nguyên tố trong bảng tuần hoàn được sắp xếp theo chiều tăng dần khối lượng nguyên tử.

Phát biểu A sai vì hiện nay bảng tuần hoàn có 118 nguyên tố hóa học.
Phát biểu B sai vì hiện nay bảng tuần có 7 chu kì.
Phát biểu C đúng vì bảng tuần hoàn gồm 8 nhóm A được đánh số từ IA đến VIIIA và 8 nhóm B được đánh số từ IB đến VIIIB.
Phát biểu D sai vì ngày nay các nguyên tố trong bảng tuần hoàn được sắp xếp theo chiều tăng dần điện tích hạt nhân.
⇨ Chọn C.
4.4
Dựa vào bảng tuần hoàn hãy cho biết kí hiệu hóa học, tên nguyên tố, số hiệu nguyên tử và khối lượng nguyên tử của các nguyên tố ở ô số 3, 9.

- Số hiệu nguyên tử là số thứ tự của nguyên tố trong bảng tuần hoàn.
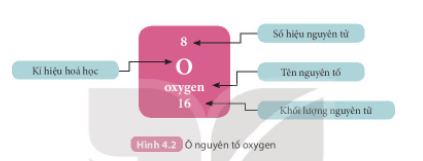

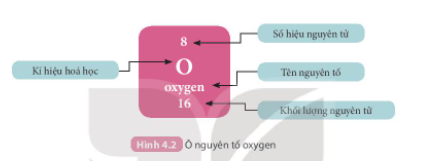
- Nguyên tố ở ô số 3
+ Kí hiệu hóa học: Li.
+ Tên nguyên tố: Lithium.
+ Số hiệu nguyên tử: 3.
+ Khối lượng nguyên tử: 7.
- Nguyên tố ở ô số 6
+ Kí hiệu hóa học: F.
+ Tên nguyên tố: Flourine.
+ Số hiệu nguyên tử: 9.
+ Khối lượng nguyên tử: 19.
4.5
Chọn các cụm từ thích hợp điền vào chỗ trống để hoàn thành các câu sau:
a) ..?.. chính là số thứ tự của nguyên tố trong bảng tuần hoàn.
b) Nguyên tử của các nguyên tố thuộc cùng chu kì có cùng ..?..
c) Nguyên tử của các nguyên tố có cùng nhóm A có ..?..

- Ô nguyên tố cho biết: kí hiệu hóa học, tên nguyên tố, số hiệu nguyên tử và khối lượng nguyên tử của nguyên tố đó.
- Chu kì là dãy các nguyên tố mà nguyên tử của chúng có cùng số lớp electron, được xếp theo chiều điện tích hạt nhân tăng dần khi đi từ trái qua phải.
- Nhóm: bảng tuần hoàn gồm 8 nhóm A được đánh số từ IA đến VIIIA và 8 nhóm B được đánh số từ IB đến VIIIB.

a) Số hiệu nguyên tử chính là số thứ tự của nguyên tố trong bảng tuần hoàn.
b) Nguyên tử của các nguyên tố thuộc cùng chu kì có cùng số lớp electron.
c) Nguyên tử của các nguyên tố có cùng nhóm A có số electron lớp ngoài cùng.
4.6
Phát biểu nào sau đây là sai?
A. Bảng tuần hoàn gồm 3 chu kì nhỏ và 4 chu kì lớn.
B. Số thứ tự của chu kì bằng số electron ở lớp ngoài cùng của nguyên tử các nguyên tố thuộc chu kì đó.
C. Số thứ tự của chu kì bằng số lớp electron của nguyên tử các nguyên tố thuộc chu kì đó.
D. Các nguyên tố trong cùng chu kì được sắp xếp theo chiều điện tích hạt nhân tăng dần.

- Hiện bảng tuần hoàn có 7 chu kì, đánh số từ 1 đến 7.
+ Chu kì 1, 2, 3 gọi là chu kì nhỏ.
+ Chu kì 4, 5, 6 gọi là chu kì lớn.

Phát biểu A đúng vì bảng tuần hoàn có 7 chu kì gồm.
+ Chu kì 1, 2, 3 gọi là chu kì nhỏ.
+ Chu kì 4, 5, 6 gọi là chu kì lớn.
Phát biểu B sai vì số thứ tự của chu kì bằng số lớp electron của nguyên tử các nguyên tố trong chu kì đó, không phải là số electron ở lớp ngoài cùng của nguyên tử các nguyên tố thuộc chu kì đó.
⇨ Phát biểu C đúng.
Phát biểu D đúng vì các nguyên tố trong cùng chu kì được sắp xếp theo chiều điện tích hạt nhân tăng dần khi đi từ trái qua phải.
⇨ Chọn B.
4.7
Phát biểu nào sau đây là đúng?
A. Nhóm gồm các nguyên tố mà nguyên tử của chúng có số lớp electron lớp ngoài cùng bằng nhau và được xếp vào cùng một hàng.
B. Các nguyên tố cùng nhóm có tính chất gần giống nhau.
C. Bảng tuần hoàn gồm 8 nhóm được kí hiệu từ 1 đến 8.
D. Các nguyên tố trong nhóm được xếp thành một cột theo chiều khối lượng nguyên tử tăng dần.

- Nhóm: bảng tuần hoàn gồm 8 nhóm A được đánh số từ IA đến VIIIA và 8 nhóm B được đánh số từ IB đến VIIIB.
- Các nguyên tố trong cùng một nhóm A có số electron ở lớp ngoài cùng bằng nhau (trừ He) nên chúng có tính chất gần giống nhau.

Phát biểu A sai vì các nguyên tố nhóm A gồm các nguyên tố mà nguyên tử của chúng có số lớp electron lớp ngoài cùng bằng nhau và được xếp vào cùng một hàng; còn một số nguyên tố nhóm B không được sắp xếp vào nhóm dựa trên số electron ở lớp ngoài cùng.
Phát biểu B đúng vì các nguyên tố trong cùng một cột (nhóm) có tính chất gần giống nhau.
Phát biểu C sai vì bảng tuần hoàn gồm 8 nhóm A được đánh số từ IA đến VIIIA và 8 nhóm B được đánh số từ IB đến VIIIB.
Phát biểu D sai vì các nguyên tố trong nhóm được sắp xếp theo chiều điện tích hạt nhân tăng dần.
⇨ Chọn đáp án B.
4.8
Chọn các từ/cụm từ thích hợp điền vào chỗ trống có đánh số (1), (2) để hoàn thành các câu sau:
“Bảng tuần các nguyên tố hóa học gồm các nguyên tố kim loại, ..(1).. và khí hiếm. Trong đó nguyên tố ..(2).. chiếm đến 80% tổng số nguyên tố.”

Trong 118 nguyên tố hóa học có hơn 90 nguyên tố kim loại, chưa đến 20 nguyên tố phi kim và 7 nguyên tố khí hiếm.

“Bảng tuần các nguyên tố hóa học gồm các nguyên tố kim loại, (1) phi kim và khí hiếm. Trong đó nguyên tố (2) kim loại chiếm đến 80% tổng số nguyên tố.”
4.9
Phát biểu nào sau đây là đúng?
A. Các nguyên tố kim loại tập trung hầu hết ở góc trên bên phải của bảng tuần hoàn.
B. Các nguyên tố kim loại tập trung hầu hết ở góc dưới bên trái của bảng tuần hoàn.
C. Các nguyên tố khí hiếm nằm ở giữa bảng tuần hoàn.
D. Các nguyên tố phi kim nằm ở cuối bảng tuần hoàn.

* Kim loại
- Trong 118 nguyên tố hóa học có hơn 90 nguyên tố kim loại.
- Các nguyên tố kim loại ở góc dưới bên trái của bảng tuần hoàn. Gồm:
+ Hầu hết các nguyên tố thuộc nhóm IA, IIA, IIIA và một số nguyên tố ở các nhóm IVA, VA, VIA.
+ Các nguyên tố thuộc nhóm IB đến VIIIB, các nguyên tố lanthanide và các nguyên tố actinide được xếp riêng thành hai hàng ở cuối bảng.
* Phi kim
- Trong 118 nguyên tố hóa học đã biết, có chưa đến 20 nguyên tố phi kim.
- Trong bảng tuần hoàn, các nguyên tố phi kim chủ yếu ở góc trên bên phải của bảng. Gồm:
+ Hầu hết các nguyên tố nhóm VIIA, VIA, VA.
+ Một số nguyên tố nhóm IVA, IIIA.
+ Nguyên tố H ở nhóm IA.
* Khí hiếm
- Trong 118 nguyên tố hóa học đã biết, có 7 nguyên tố khí hiếm.
- Nguyên tố khí hiếm nằm ở nhóm VIIIA trong bảng tuần hoàn.

Phát biểu A sai vì các nguyên tố kim loại tập trung hầu hết ở góc dưới bên trái của bảng tuần hoàn.
⇨ Phát biểu B đúng.
Phát biểu C sai vì các nguyên tố khí hiếm ở nhóm VIIIA – cuối chu kì của bảng tuần hoàn.
Phát biểu D sai vì các nguyên tố phi kim chủ yếu ở góc trên bên phải của bảng.
⇨ Chọn B.
4.10
Phát biểu nào sau đây là sai?
A. Các nguyên tố phi kim tập trung ở các nhóm VA, VIA, VIIA.
B. Các nguyên tố khí hiếm nằm ở nhóm VIIIA.
C. Các nguyên tố kim loại có mặt ở tất cả các nhóm trong bảng tuần hoàn.
D. Các nguyên tố lanthanide và actinide, mỗi họ gồm 14 nguyên tố được xếp riêng thành hai dãy ở cuối bảng.

Phát biểu C sai vì các nguyên tố kim loại thuộc nhóm IA, IIA, IIIA, một số nguyên tố ở các nhóm IVA, VA, VIA, và các nhóm từ IB đến VIIIB.
Các nguyên tố kim loại không có mặt ở nhóm VIIIA trong bảng tuần hoàn.
⇨ Chọn C.
4.11
Phát biểu nào sau đây là đúng?
A. Ở điều kiện thường, tất cả các nguyên tố kim loại tồn tại ở thể rắn.
B. Ở điều kiện thường, tất cả các nguyên tố phi kim tồn tại ở thể lỏng.
C. Ở điều kiện thường, tất cả các nguyên tố khí hiếm tồn tại ở thể khí.
D. Ở điều kiện thường, tất cả các nguyên tố phi kim tồn tại ở thể khí.

- Ở điều kiện thường, các kim loại đều ở trạng thái rắn (trừ Hg).
- Trong điều kiện thường, phi kim tồn tại dưới cả ba trạng thái:
+ Rắn: C, P, S, …
+ Lỏng: Br2, …
+ Khí: O2, H2, Cl2, N2,…
- Ở điều kiện thường, các nguyên tố khí hiếm tồn tại ở trạng thái khí.

Advertisements (Quảng cáo)
Phát biểu A sai vì ở điều kiện thường, các nguyên tố kim loại tồn tại ở thể rắn trừ thủy ngân tồn tại ở thể lỏng.
Phát biểu B sai vì ở điều kiện thường, ngoài các phi kim tồn tại ở thể lỏng, còn có các nguyên tố phi kim ở tồn tại ở thể rắn (ví dụ: carbon) và các phi kim tồn tại ở thể khí (ví dụ: oxygen).
⇨ Phát biểu D sai.
Phát biểu C đúng.
⇨ Chọn đáp C.
4.12
Hãy cho biết tên và kí hiệu của nguyên tố ở nhóm VA, chu kì 3 và nguyên tố ở nhóm VIIIA, chu kì 2.

- Ô nguyên tố cho biết: kí hiệu hóa học, tên nguyên tố, số hiệu nguyên tử và khối lượng nguyên tử của nguyên tố đó.
- Chu kì là dãy các nguyên tố mà nguyên tử của chúng có cùng số lớp electron, được xếp theo chiều điện tích hạt nhân tăng dần khi đi từ trái qua phải.
- Nhóm: bảng tuần hoàn gồm 8 nhóm A được đánh số từ IA đến VIIIA và 8 nhóm B được đánh số từ IB đến VIIIB.

4.13
Hydrogen là nguyên tố nhẹ nhất trong tất cả các nguyên tố và phổ biến nhất trong vũ trụ. Hãy cho biết kí hiệu của nguyên tố hydrogen và cho biết nó ở chu kì nào và nhóm nào trong bảng tuần hoàn.

- Ô nguyên tố cho biết: kí hiệu hóa học, tên nguyên tố, số hiệu nguyên tử và khối lượng nguyên tử của nguyên tố đó.
- Chu kì là dãy các nguyên tố mà nguyên tử của chúng có cùng số lớp electron, được xếp theo chiều điện tích hạt nhân tăng dần khi đi từ trái qua phải.
- Nhóm: bảng tuần hoàn gồm 8 nhóm A được đánh số từ IA đến VIIIA và 8 nhóm B được đánh số từ IB đến VIIIB.


Kí hiệu hóa học: H
Thuộc ô số 1, chu kì 1, nhóm IA.
4.14
Silicon là nguyên tố phổ biến thứ hau trên Trái Đất, tồn tại chủ yếu trong cát và là chất hóa học phổ biến nhất trong vỏ trái đất. Hãy cho biết kí hiệu của nguyên tố silicon và cho biết nó ở chu kì nào và nhóm nào trong bảng tuần hoàn?


Kí hiệu hóa học: Si
Thuộc ô số 14, chu kì 3, nhóm IVA.
4.15
Viết kí hiệu và tên của các nguyên tố thuộc nhóm IA, IIA, VIIA và VIIIA ở chu kì 2.


4.16
Nguyên tố Mg thuộc chu kì 3, nhóm IIA. Hỏi nguyên tử của nguyên tố Mg có bao nhiêu lớp electron và bao nhiêu electron ở lớp ngoài cùng?

* Chu kì:
- Chu kì là dãy các nguyên tố mà nguyên tử của chúng có cùng số lớp electron.
- Hiện bảng tuần hoàn có 7 chu kì, đánh số từ 1 đến 7.
- Số thứ tự của chu kì bằng số lớp electron của nguyên tử các nguyên tố trong chu kì đó.
* Nhóm:
- Nhóm: bảng tuần hoàn gồm 8 nhóm A được đánh số từ IA đến VIIIA và 8 nhóm B được đánh số từ IB đến VIIIB.
- Số thứ tự của nhóm A bằng số electron ở lớp ngoài cùng của nguyên tử các nguyên tố trong nhóm đó.

Nguyên tố Mg thuộc chu kì 3 nên nguyên tử của nguyên tố Mg có 3 lớp electron.
Nguyên tố Mg thuộc nhóm IIA nên nguyên tử của nguyên tố Mg có 2 electron ở lớp ngoài cùng.
4.17
Biết nguyên tố P ở nhóm VA, chu kì 3. Hãy cho biết nhận định sau đúng hay sai và giải thích: “Nguyên tử P có 5 lớp electron và 3 electron ở lớp ngoài cùng”.

- Chu kì là dãy các nguyên tố mà nguyên tử của chúng có cùng số lớp electron.
- Số thứ tự của nhóm A bằng số electron ở lớp ngoài cùng của nguyên tử các nguyên tố trong nhóm đó.

- Nhận định trên là sai vì
+ Số thứ tự của nhóm A bằng số electron ở lớp ngoài cùng của nguyên tử các nguyên tố trong nhóm đó.
+ Số thứ tự của chu kì bằng số lớp electron của nguyên tử các nguyên tố trong chu kì đó.
- Do đó
+ Nguyên tố P ở nhóm VA nên nguyên tử P có 5 electron lớp ngoài cùng.
+ Nguyên tố P ở chu kì 3 nên nguyên tử P có 3 lớp electron.
4.18
Trong tự nhiên có khoảng 25 nguyên tố cần thiết cho sự sống. Trong đó nguyên tố X (thuộc nhóm VIIA, chu kì 5 trong bảng tuần hoàn) là nguyên tố vi lượng mà hàng ngày con người cần khoảng 15 miligam cho hoạt động của tuyến giáp, nếu thiếu nguyên tố X có thể gây bướu cổ. Dựa vào bảng tuần hoàn hóa học hãy cho biết kí hiệu hóa học, tên nguyên tố và khối lượng nguyên tử của nguyên tố X.

- Ô nguyên tố cho biết: kí hiệu hóa học, tên nguyên tố, số hiệu nguyên tử và khối lượng nguyên tử của nguyên tố đó.
- Chu kì là dãy các nguyên tố mà nguyên tử của chúng có cùng số lớp electron, được xếp theo chiều điện tích hạt nhân tăng dần khi đi từ trái qua phải.
- Nhóm: bảng tuần hoàn gồm 8 nhóm A được đánh số từ IA đến VIIIA và 8 nhóm B được đánh số từ IB đến VIIIB.


Tên nguyên tố: Iodine
Kí hiệu hóa học: I
Khối lượng nguyên tử: 127.
4.19
Nguyên tố X (Z = 11) là nguyên tố có trong thành phần của muối ăn. Hãy cho biết tên nguyên tố X và vẽ mô hình sắp xếp electron ở vỏ nguyên tử X. X có bao nhiêu lớp electron, bao nhiêu electron ở lớp ngoài cùng? Từ đó cho biết X thuộc chu kì mấy, nhóm mấy trong bảng tuần hoàn.

- Số hiệu nguyên tử (Z) = Số electron = 11 ⇨ X là Sodium
- Sự phân bố của các electron trên các lớp electron của nguyên tử Sodium
+ Lớp electron gần hạt nhân nhất (lớp thứ nhất) có 2 electron.
+ Lớp electron thứ 2 chứa tối đa 8 electron.
+ Lớp electron thứ 3 chứa 11 – 8 - 2 = 1 electron.
- Mô hình sắp xếp electron ở vỏ nguyên tử Sodium
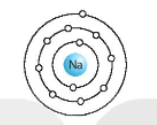
- Sodium có 3 lớp electron ⇨ Sodium thuộc chu kì 3.
- Sodium có 1 electron lớp ngoài cùng ⇨ Sodium thuộc nhóm IA.
4.20
Nguyên tố X (Z = 20) là thành phần không thể thiếu trong sản phẩm sữa. Sự thiếu hụt một lượng rất nhỏ của X trong cơ thể đã ảnh hưởng tới sự hình thành và phát triển của xương và răng, nhưng nếu cơ thể thừa nguyên tố X lại có thể dẫn đến bênh sỏi thận. Hãy cho biết tên nguyên tố X và vẽ mô hình sắp xếp electron ở vỏ nguyên tử X. X có bao nhiêu lớp electron, bao nhiêu electron lớp ngoài cùng. Từ đó cho biết X thuộc chu kì mấy, nhóm mấy trong bảng tuần hoàn.

- Số hiệu nguyên tử (Z) = Số electron = 20 ⇨ X là Calcium
- Sự phân bố của các electron trên các lớp electron của nguyên tử Sodium
+ Lớp electron gần hạt nhân nhất (lớp thứ nhất) có 2 electron.
+ Lớp electron thứ 2 chứa tối đa 8 electron.
+ Lớp electron thứ 3 chứa tối đa 8 electron.
+ Lớp electron thứ 4 chứa 20 – 2 – 8 – 8 = 2 electron.
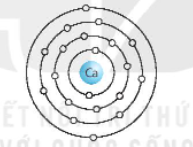
- Calcium có 4 lớp electron ⇨ Calcium thuộc chu kì 4.
- Calcium có 2 electron lớp ngoài cùng ⇨ Calcium thuộc nhóm IIA.
4.21
Dựa vào bảng tuần hoàn, hãy cho biết trong số các nguyên tố: Na, K, Mg, Ba, Be, B, C, N, O, Ar, những nguyên tố nào thuộc cùng một chu kì và là chu kì mấy.

Na (Z=11), K (Z=19), Mg (Z=12), Ba (Z=56), Be (Z=4), B (Z=5), C (Z=6), N (Z=7), O (Z=8), Ar (Z=18).
Những nguyên tố thuộc cùng chu kì 2: Be, B, C, N, O.
Những nguyên tố thuộc cùng chu kì 3: Na, Mg, Ar.
4.22
Dựa vào bảng tuần hoàn, hãy cho biết trong số các nguyên tố: Na, K, Mg, Ba, Be, B, C, N, O, Ar, những nguyên tố nào thuộc cùng một nhóm và là nhóm mấy.

Na (Z=11), K (Z=19), Mg (Z=12), Ba (Z=56), Be (Z=4), B (Z=5), C (Z=6), N (Z=7), O (Z=8), Ar (Z=18).
Những nguyên tố thuộc cùng nhóm IA: Na, K.
Những nguyên tố thuộc cùng nhóm IIA: Be, Mg, Ba.
4.23
Dựa vào bảng tuần hoàn, hãy cho biết trong số các nguyên tố: Na, Cl, Fe, K, Kr, Mg, Ba, C, N, S, Ar, những nguyên tố nào là kim loại? Những nguyên tố nào là phi kim? Những nguyên tố nào là khí hiếm?


4.24
Hãy tìm hiểu và cho biết:
a) Tên và kí hiệu của nguyên tố kim loại duy nhất tồn tại ở thể lỏng, ở điều kiện thường Dựa vào bảng tuần hoàn, hãy cho biết nguyên tố đó ở ô số bao nhiêu?
b) Tên và kí hiệu của nguyên tố kim loại có trong thành phần của hemoglobin (chất có khả năng vận chuyển khí oxygen từ phổi đến các tế bào), nếu thiếu nguyên tố này cơ thể chúng ta sẽ mắc bệnh thiếu máu. Hãy kể ra ít nhất 3 ứng dụng trong đời sống của nguyên tố kim loại đó,
c) Tên và kí hiệu của nguyên tố khí hiếm dùng để bơm vào bóng bay hoặc khinh khí cầu.

Ô nguyên tố cho biết: kí hiệu hóa học, tên nguyên tố, số hiệu nguyên tử và khối lượng nguyên tử của nguyên tố đó.


4.25
Nguyên tố xenon (Xe) có 8 electron ở lớp vỏ nguyên tử. Hãy cho biết xenon là kim loại, phi kim hay khí hiếm? Ở điều kiện thường xenon tồn tại ở thể nào?

- Số thứ tự của nhóm A bằng số electron ở lớp ngoài cùng của nguyên tử các nguyên tố trong nhóm đó.
- Khí hiếm nằm ở nhóm VIIIA trong bảng tuần hoàn,
- Lớp electron ngoài cùng của khí hiếm có 8 electron hoặc 2 electron (với He).

Nguyên tố xenon (Xe) có 8 electron ở lớp vỏ nguyên tử.
⇨ Xenon nằm ở nhóm VIIIA trong bảng tuần hoàn.
⇨ Xenon là khí hiếm.
Ở điều kiện thường xenon tồn tại ở khí.
4.26
X là nguyên tố cần thiết cho quá trình hô hấp của sinh vật, nếu thiếu nguyên tố này sự cháy không thể xảy ra. Hãy cho biết tên, kí hiệu và vị trí (ô nguyên tố, chu kì, nhóm) của X trong bảng tuần hoàn. Nguyên tố X là kim loại, phi kim hay khí hiếm?


4.27
Hãy cho biết vị trí của nguyên tố Y trong bảng tuần hoàn, biết vỏ nguyên tử của nguyên tố Y có 2 lớp electron, trong đó lớp ngoài cùng có 4 electron. Từ đó cho biết Y là kim loại, phi kim hay khí hiếm?

- Vỏ nguyên tử của nguyên tố Y có 2 lớp electron ⇨ Y ở chu kì 2.
- Lớp ngoài cùng của Y có 4 electron. ⇨ Y ở nhóm IVA.
- Số electron của Y
+ Lớp electron gần hạt nhân nhất (lớp thứ nhất) có 2 electron.
+ Lớp electron thứ 2 (lớp ngoài cùng) có 4 electron.
⇨ Nguyên tử Y có 6 electron.
⇨ Y ở ô thứ 6 trong bảng tuần hoàn.
4.28
a) Dựa vào bảng tuần hoàn hãy liệt kê kí hiệu và điện tích hạt nhân Z của các nguyên tố thuộc chu kì 3.
b) Hãy xác định tên và kí hiệu nguyên tố X biết nó thuộc chu kì 3, có điện tích hạt nhân Z > 12, dẫn điện tốt, dẫn nhiệt tốt, dẻo, dễ dát mỏng, có ánh kim. Giải thích.
c) Hãy kể ra ít nhất 3 ứng dụng trong đời sống của nguyên tố X.


