Câu hỏi/bài tập:
Cho các nguyên tố X, Y, Z có số hiệu nguyên tử lần lượt là 6, 9, 14. Thứ tự tính phi kim tăng dần của các nguyên tố đó là
A. X < Z < Y.
B. Z < X < Y.
C. Z < Y < X.
D. Y < X < Z.

- Xu hướng biến đổi tính kim loại, tính phi kim:
+ Trong một chu kì, theo chiều tăng dần của điện tích hạt nhân, tính kim loại giảm dần, tính phi kim tăng dần
+ Trong một nhóm, theo chiều tăng dần của điện tích hạt nhân, tính kim loại tăng dần, tính phi kim giảm dần
- Cách thực hiện:
+ Bước 1: Xác định vị trí các nguyên tố trong bảng tuần hoàn (chu kì nào? Nhóm nào?)
+ Bước 2: Dựa vào xu hướng biến đổi tính kim loại, tính phi kim để xác định đáp án đúng

Advertisements (Quảng cáo)
- Bước 1: Xác định vị trí các nguyên tố trong bảng tuần hoàn
+ Nguyên tố X có Z = 6 => Cấu hình electron của X là: 1s22s22p2
=> X thuộc chu kì 2, nhóm IVA
+ Nguyên tố Y có Z = 9 => Cấu hình electron của Y là: 1s22s22p5
=> Y thuộc chu kì 2, nhóm VIIA
+ Nguyên tố Z có Z = 14 => Cấu hình electron của Z là: 1s22s22p63s23p2
=> Z thuộc chu kì 3, nhóm IVA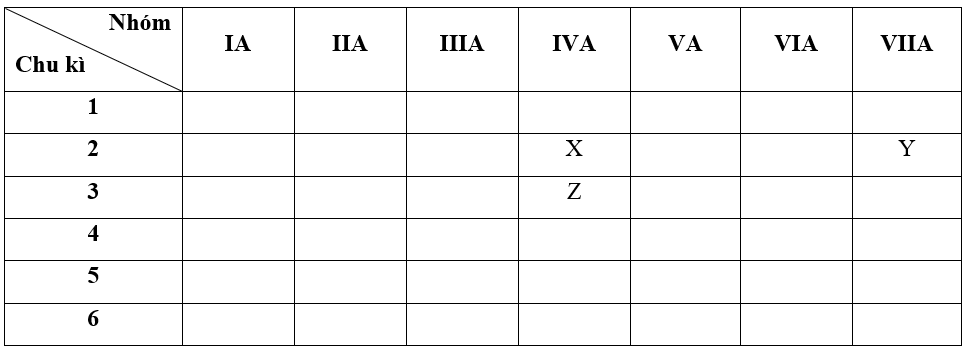
- Bước 2: Dựa vào xu hướng biến đổi tính kim loại, tính phi kim
+ Trong cùng một chu kì 2, theo chiều tăng dần về điện tích hạt nhân, ta có chiều tăng dần tính phi kim là: X < Y (1)
+ Trong cùng một nhóm IVA, theo chiều tăng dần về điện tích hạt nhân, ta có chiều tăng dần tính phi kim là: Z < X (2)
=> Từ (1) và (2) ta có dãy sắp xếp theo chiều tăng dần tính phi kim:
Z < X < Y
=> Đáp án: B
