13.1
Biểu đồ dưới đây thể hiện mối tương quan giữa nhiệt độ sôi và số nguyên tử carbon trong phân tử alkene.
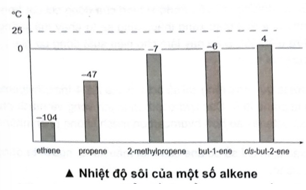
Có bao nhiêu alkene trong biểu đồ ở thể khí trong điều kiện thường(25 °C)?
A. 4. B. 2. C. 3. D. 5.

Những chất ở thể khí có nhiệt độ sôi thấp hơn nhiệt đồ phòng.

Trên đồ thị, ta thấy có 5 alkene có nhiệt độ sôi nhỏ hơn nhiệt độ phòng (25 oC). Do đó, 5 alkene này ở thể khí trong điều kiện thường.
→ Chọn D.
13.2
Ứng với công thức phân tử C5H8 có bao nhiêu alkyne là đồng phân cấu tạo của nhau?
A. 3. B. 2. C.5. D.4

Alkyne là những hydrocarbon mạch hở, chỉ chứa các liên kết đơn và một liên kết ba C≡C trong phân tử, có công thức chung CnH2n-2 (n ≥ 2).
Đồng phân cấu tạo (gồm đồng phân mạch carbon, đồng phân loại nhóm chức, đồng phân vị trí nhóm chức)

Các đồng phân cấu tạo của alkyne C5H8

→ Chọn A.
13.3
Cho các alkene sau:
1. CH2=CH-CH2-CH3 2. (CH3)2C=C(CH3)2
3. CH3-CH2-CH=CH-CH3 4. CH3-CH2-CH=CH-CH2-CH3
Số alkene có đồng phân hình học là
A. 4. B. 2. C. 3. D. 1.

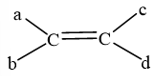
Với a, b, c, d là các nhóm thế.
Điệu kiện để alkene có đồng phân hình học: a ≠ b và c ≠ d.

Trong phân tử của hai alkene CH2=CH-CH2-CH3, (CH3)2C=C(CH3)2, ta thấy nguyên tử C trong liên kết đôi liên kết với hai nhóm thế giống nhau nên chúng không có đồng phân hình học.
Trong phân tử của hai alkene CH3-CH2-CH=CH-CH3, CH3-CH2-CH=CH-CH2-CH3, ta thấy nguyên tử C trong liên kết đôi liên kết với hai nhóm thế khác nhau nên chúng có đồng phân hình học.
→ Chọn B.
13.4
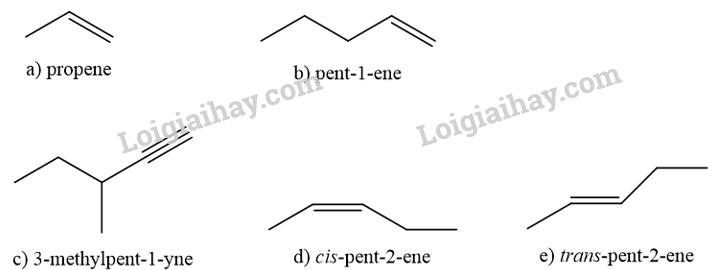
Viết công thức khung phân tử của
a) propene.
b) pent-1-ene.
c) 3-methylpent-1-yne.
d) cis-pent-2-ene.
e) trans-pent-2-ene.

Công thức khung phân tử: Dùng nét gạch để biểu diễn liên kết giữa các nguyên tử carbon với nhau và giữa carbon với nguyên tử khác mà không phải là hydrogen. Trong công thức khung phân tử chỉ ghi kí hiệu các nguyên tử khác C và H (trừ H nằm ở trong nhóm chức).

13.5
Cho các phân tử alkene có công thức khung phân tử dưới đây
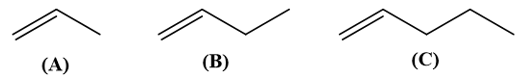
a) Gọi tên các phân tử alkene nêu trên theo danh pháp thay thế.
b) So sánh tương tác van der Waals giữa các phân tử alkene nếu trên. Từ đó em có kết luận gì?

- Tên theo danh pháp thay thế của alkene hoặc alkyne không phân nhánh

- Tương tác Van der Waals giữa các phân tử tăng khi khối lượng phân tử tăng.

a) (A): propene.
(B): but-1-ene.
(C): pent -1-ene.
b) Đi từ propene đến pent-1-ene, kích thước phân tử alkene tăng dần làm cho diện tích bề mặt tiếp xúc giữa chúng cũng tăng, tương tác van der Waals giữa các phân tử do đó cũng tăng dần, dẫn đến nhiệt độ sôi các alkene tăng dần. Ngoài ra, ở điều kiện thường, propene và but-1-ene là các chất khí trong khi pent-1-ene là chất lỏng vì tương tác van der Waals giữa các phân tử propene và but-1-ene chưa đủ lớn. Các phân tử alkene có từ 18 nguyên tử carbon trở lên ở thể rắn, do tương tác van der Waals giữa chúng là mạnh đáng kể.
13.6
Viết công thức cấu tạo và gọi tên tất cả các alkene và alkyne có công thức phân tử lần lượt là C5H10 và C5H8. Trong tất cả các chất mà em đã liệt kê, chất nào có đồng phân hình học? Viết công thức và gọi tên các đồng phân hình học đó.

- Tên theo danh pháp thay thế của alkene hoặc alkyne không phân nhánh

- Tên theo danh pháp thay thế của alkene hoặc alkyne phân nhánh
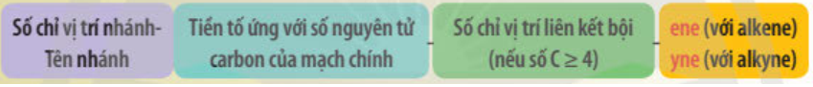
- Đồng phân hình học của alkene:
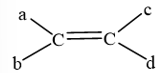
Với a, b, c, d là các nhóm thế.
Điệu kiện để alkene có đồng phân hình học: a ≠ b và c ≠ d.

- Công thức cấu tạo của alkene C5H10:
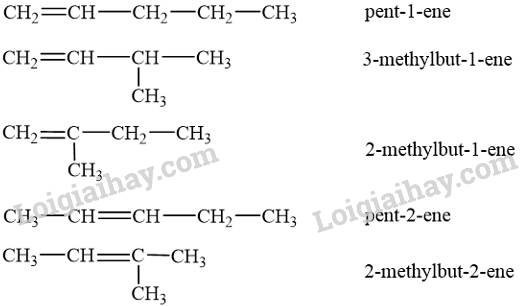
Trong đó pent-2-ene có 2 đồng phân hình học:
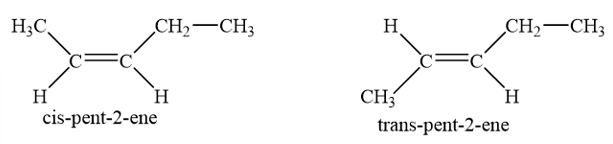
- Công thức cấu tạo của alkyne C5H8:
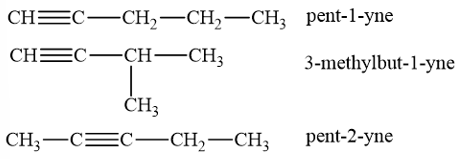
13.7
So sánh nhiệt độ sôi của các đồng phân cis, trans của cùng một phân tử alkene. Giải thích và cho ví dụ minh hoạ.

Xét tổng moment lưỡng cực của hai phân tử. Phân tử có nhiệt độ sôi cao hơn là phân tử phân cực hơn.

Đồng phân trans có tổng moment lưỡng cực thường triệt tiêu hoặc gần triệt tiêu, còn đồng phân cis có tổng moment lưỡng cực không triệt tiêu, do đó đồng phân trans có nhiệt độ sôi thấp hơn đồng phân cis.
Ví dụ phân từ cis-but-2-ene và trans-but-2-ene đều chứa nhóm -CH3 là nhóm đẩy electron làm phân tử mỗi chất hình thành các momen lưỡng cực yếu C-C như trong hình bên dưới. Tuy nhiên, cis-but-2-ene có tổng moment lưỡng cực không triệt tiêu, còn trans-but-2-ene có tổng moment lưỡng cực triệt tiêu. Do đó cis-but-2-ene là phần tử phân cực nhẹ trans-but-2-ene là phân tử không phân cực, dẫn đến nhiệt độ sôi của cis-but-2-ene cao hơn so với trans-but-2-ene.
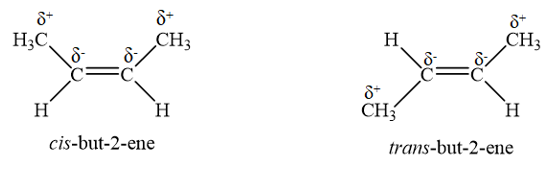
13.8
Giải thích vì sao liên kết ba C≡C của một phân tử alkyne tuy giàu mật độ electron hơn so với liên kết đôi C=C của một phân tử alkene tương ứng nhưng khả năng phản ứng cộng (X2, HX, H2O) vào alkyne lại kém hơn vào alkene tương ứng?

electron π trong liên trong C≡C bị giữ chặt hơn so với các electron π trong C=C, dẫn đến khả năng phản ứng cộng (X2, HX, H2O) của alkyne kém hơn alkene tương ứng.

Tuy liên kết ba C≡C của một alkyne giàu mật độ electron hơn so vớiliên kết đôi C=C của một alkene tương ứng nhưng khả năng phản ứng cộng (X2, HX, H2O) vào alkyne lại kém hơn vào alkene tương ứng. Điều này có thể giải thích là do nguyên tử carbon trong liên kết C≡C ở trạng thái lai hoá sp, có độ âm điện lớn hơn các nguyên tử carbon trong liên kết C=C ở trạng thái lai hoá sp2, làm cho các electron π trong C≡C bị giữ chặt hơn so với các electron π trong C=C, dẫn đến khả năng phản ứng cộng (X2, HX, H2O) của alkyne kém hơn alkene tương ứng.
Ví dụ ethylene nhanh chóng làm mất màu nước bromine, acetylene làm mất màu nước bromine chậm hơn. Tốc độ mất màu nước bromine của ethylene gấp 5 lần so với acetylene.
13.9
Giải thích vì sao liên kết π của trans-but-2-ene có mật độ electron cao hơn đáng kể so với liên kết π của trans-2,3-dibromobut-2-ene? Từ đó so sánh khả năng phản ứng cộng bromine của trans-but-2-ene và trans-2,3- dibromobut-2-ene.

Trong liên kết cộng hóa trị phân cực, electron bị lệch về phía nguyên tử có độ âm điện lớn hơn.
Mật độ electron càng lớn ở vị trí liên đôi càng nhiều, phản ứng cộng của alkene càng dễ xảy ra.

Advertisements (Quảng cáo)
Do nguyên tử bromine có độ âm điện lớn hơn nguyên tử carbon nên liên kết C–Br bị phân cực mạnh về phía bromine, kết quả liên kết đôi của trans-2,3-dibromobut-2-ene có mật độ electron thấp hơn đáng kể so với liên kết đôi của trans-but-2-ene. Chính vì vậy khả năng phản ứng cộng bromine của trans-2,3-dibromobut-2-ene kém hơn so với trans-but-2-ene.
13.10
So sánh khả năng phản ứng cộng bromine vào liên kết ba C≡C của một alkyne và vào liên kết đôi C=C của một dibromoalkene tương ứng. Giải thích.

Trong liên kết cộng hóa trị phân cực, electron bị lệch về phía nguyên tử có độ âm điện lớn hơn.
Mật độ electron càng lớn ở vị trí liên bội càng nhiều, phản ứng cộng của hydrocarbon không no càng dễ xảy ra.

Phản ứng cộng bromine vào liên kết ba C≡C của một alkyne dễ hơn vào liên kết đôi C=C của một dibromoalkene tương ứng. Điều này được giải thích là do nguyên tử bromine có độ âm điện mạnh, đã làm liên kết C-Br phân cực mạnh về phía bromine, làm mật độ electron trên liên kết đôi của dibromoalkene kém hơn hẳn so với trên liên kết ba của alkyne tương ứng.
13.11
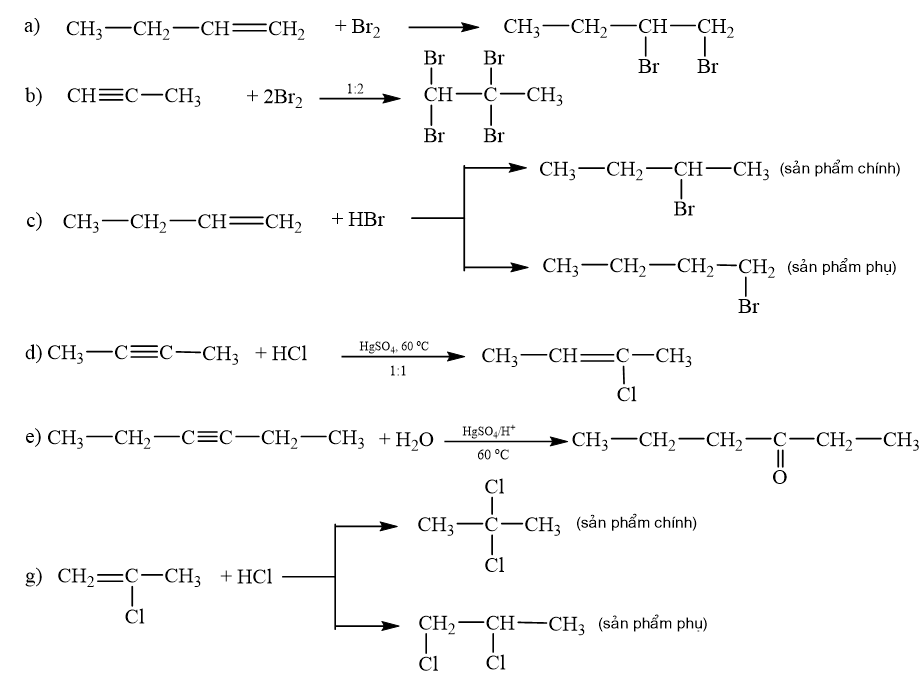
Hoàn thành các phương trình phản ứng sau (nêu rõ sản phẩm chính, phụ nếu có).
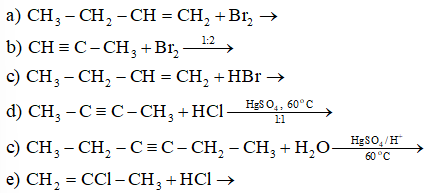

Alkene hoặc alkyne không đối xứng tác dụng với hydrogen halide (HX) tạo thành hỗn hợp sản phẩm, trong đó sản phẩm chính tuân theo quy tắc Markovnikov: “Nguyên tử hydrogen ưu tiên cộng vào nguyên tử carbon chưa no có nhiều hydrogen hơn, còn nguyên tử X ưu tiên cộng vào nguyên tử carbon chưa no có ít hydrogen hơn”.

13.12
Khi cho ethylene phản ứng với nước bromine, bên cạnh sản phẩm 1,2-dibromoethane, người ta còn thu được sản phẩm 2-bromoethanol có công thức như sau:
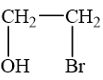
Viết phương trình phản ứng minh hoạ.

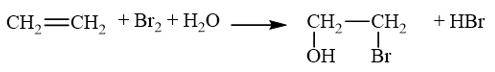
Chất phản ứng: ethylene, H2O, Br2.
Sản phẩm: 2-bromoethanol, HBr

13.13
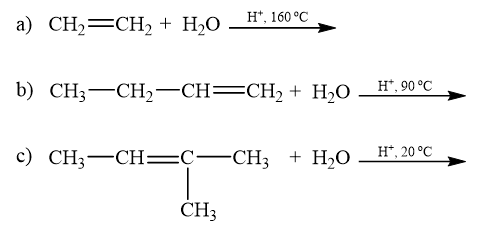
Khi tiến hành cho phân tử alkene cộng nước cần xúc tác là acid, sản phẩm thu được là alcohol. Nhiệt độ cần thiết cho phản ứng phụ thuộc vào bậc của alcohol tạo thành. Alcohol bậc III chỉ cần nhiệt độ dưới 25 °C. alcohol bậc II cần nhiệt độ dưới 100 °C và alcohol bậc I cần nhiệt độ dưới 170 °C. Viết các phương trình phản ứng sau (chỉ viết sản phẩm chính):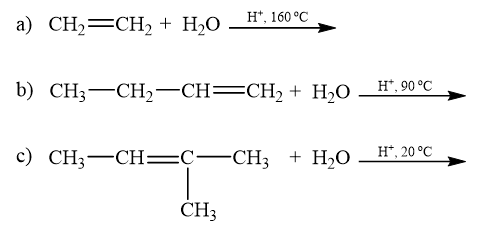

Alkene hoặc alkyne không đối xứng tác dụng với hydrogen halide (HX) tạo thành hỗn hợp sản phẩm, trong đó sản phẩm chính tuân theo quy tắc Markovnikov: “Nguyên tử hydrogen ưu tiên cộng vào nguyên tử carbon chưa no có nhiều hydrogen hơn, còn nguyên tử X ưu tiên cộng vào nguyên tử carbon chưa no có ít hydrogen hơn”.

13.14
Có 2 chất lỏng mất nhãn là hexane và hex-1-ene. Thuốc thử nào được dùng để phân biệt hai hoá chất này? Có thể phân biệt hai chất lỏng này dựa vào kết quả phân tích phổ hồng ngoại của chúng được không?

Alkene tham gia phản ứng cộng với bromine, làm mất màu nước bromine.
Alkene có nối đôi C=C, alkane không có. Do đó, khi sử dụng phổ hồng ngoại, alkene có peak đặc trưng của nối đôi C=C.

Có thể sử dụng nước bromine để phân biệt hexane và hex-1-ene. Hex-1-ene làm mất màu nước bromine, hexane không làm mất màu nước bromine.
Có thể phân biệt hai chất lỏng này dựa vào kết quả phân tích phổ hồng ngoại vì hex-1-ene có peak 1650 cm-1 của nối đôi C=C, còn hexane thì không.
13.15
a) Đề nghị phương pháp hoá học phân biệt 2 chất lỏng mất nhãn là hex-1-yne và hex-2-yne.
b) Trình bày phương pháp vật lý phân biệt 2 chất lỏng mất nhãn trên.

Các alk-1-yne như ethyne, propyne, ... có phản ứng tạo kết tủa với dung dịch AgNO3 trong ammonia. Đây là phản ứng thường dùng để nhận biết alk-1-yne.

a) Sử dụng AgNO3/NH3 để phân biệt hex-1-yne và hex-2-yne. Hex-1-yne tạo kết tủa vàng nhạt với dung dịch silver nitrate trong ammonia, còn hex-2-yne thì không.
b) Sử dụng phổ hồng ngoại để phân biệt hex-1-yne và hex-2-yne. Vì trong phổ hồng ngoại, peak đặc trưng của các alk-1-yne là peak khoảng 3300 cm-1, các alkyne khác không có peak này. Do đó, phổ hồng ngoại có peak khoảng 3300 cm-1 là hex-1-yne, chất còn lại là hex-2-yne.
13.16
a) Vì sao nguyên tử carbon ở trạng thái lai hoá sp (trong liên kết baC≡C) có độ âm điện lớn hơn nguyên tử carbon ở trạng thái lại hoá sp2 (trong liên kết đôi C=C) và nguyên tử carbon ở trạng thái lai hoá sp3 (trong liên kết đơn C−C)? Điều này ảnh hưởng gì đến độ linh động của các nguyên tử hydrogen liên kết trực tiếp với các nguyên tử carbon ở các trạng thái lai hoá trên?
b) Nêu công thức cấu tạo một hydrocarbon bất kì có chứa 3 nguyên tử hydrogen linh động trong phân tử.

a) Nguyên tử carbon ở trạng thái lai hóa có độ âm điện càng lớn, nguyên tử hydrogen liên kết trực tiếp với carbon này càng linh động.
b) Alkyne có liên kết ba C≡C có hydrogen linh động.

a) Nguyên tử carbon ở trạng thái lai hoá sp có tỉ lệ đóng góp của orbital s là 50%, cao hơn so với nguyên tử carbon ở trạng thái lai hoá sp2 (33,3%) và nguyên tử carbon ở trạng thái lai hoá sp3 (25%) nên orbital lai hoá sp của nguyên tử carbon ở gần hạt nhân hơn, dẫn đến nguyên tử carbon lai hóa sp có độ âm điện cao hơn. Vì thế nguyên tử hydrogen liên kết trực tiếp với các nguyên tử carbon mang liên kết ba có tính linh động.
b) Hydrocarbon có 3 nguyên tử hydrogen linh động có thể là:
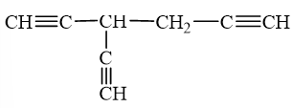
13.17
Dẫn 150 gam acetylene qua ống sắt nóng đỏ thu được 90 gam benzene. Viết phương trình phản ứng xảy ra và tính hiệu suất phản ứng.

Có thể tính hiệu suất dựa vào acetylene hoặc benzene.
Tính hiệu suất theo benzene: ta cần tính khối lượng của benzene theo lý thuyết dựa vào acetylene đề bài cho.


\[\begin{array}{l}{{\rm{n}}_{{{\rm{C}}_{\rm{2}}}{{\rm{H}}_{\rm{2}}}}} = \frac{{150}}{{26}} = \frac{{75}}{{13}}{\rm{ }}({\rm{mol}})\\ \Rightarrow {{\rm{n}}_{{{\rm{C}}_{\rm{6}}}{{\rm{H}}_{\rm{6}}}}} = \frac{1}{3} \times {{\rm{n}}_{{{\rm{C}}_{\rm{2}}}{{\rm{H}}_{\rm{2}}}}} = \frac{1}{3} \times \frac{{75}}{{13}} = \frac{{25}}{{13}}{\rm{ }}({\rm{mol}})\\ \Rightarrow {{\rm{m}}_{{{\rm{C}}_{\rm{6}}}{{\rm{H}}_{\rm{6}}}(lt)}} = \frac{{25}}{{13}} \times 78 = 150{\rm{ (g)}}\\ \Rightarrow {\rm{H}} = \frac{{90}}{{150}} \times 100\% = 60\% \end{array}\].
13.18
Có một số loại trái cây chưa chín mà chúng ta lại muốn được sớm thưởng thức chúng, chẳng hạn một quả bơ, xoài, ... Có một cách giải quyết đơn giản là cho quả bơ vào túi giấy cùng với vài quả chuối, bơ sẽ chín nhanh hơn nhiều. Giải thích cách làm trên.

Ethylene là hormon sinh trưởng của thực vật, có tác dụng làm cây mau già và quả mau chín. Ethylene được dùng để làm chín trái cây, điều khiển quá trình sinh mủ của cây cao su,...

Đó là do chuối khi chuẩn bị chín sẽ giải phóng một loại hormone thực vật ở thể khí là ethylene, ethylene giúp đẩy nhanh quá trình chín nhiều loại quả khác nhau. Nhờ đó quả bơ cũng được đẩy nhanh chín theo.
13.19
Nhu cầu sử dụng PVC trên toàn thế giới liên tục tăng trong các năm qua. Để thu được PVC, cần đi từ monomer là vinyl chloride. Có thể điều chế vinyl chloride từ acetylene hoặc ethylene. Một trong những cách điều chế vinyl chloride từ ethylene hiện nay là theo sơ đồ:
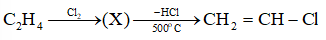
Viết các phương trình phản ứng minh hoạ.

- Phản ứng cộng halogen vào nối đôi C=C.
- Phản ứng tách hydrogen chloride ra khỏi dẫn xuất halogen.

\[\begin{array}{l}{\rm{C}}{{\rm{H}}_2} = {\rm{C}}{{\rm{H}}_2} + {\rm{C}}{{\rm{l}}_{\rm{2}}} \to {\rm{C}}{{\rm{H}}_{\rm{2}}}{\rm{Cl}} - {\rm{C}}{{\rm{H}}_{\rm{2}}}{\rm{Cl}}\\{\rm{C}}{{\rm{H}}_{\rm{2}}}{\rm{Cl}} - {\rm{C}}{{\rm{H}}_{\rm{2}}}{\rm{Cl}} \to {\rm{C}}{{\rm{H}}_{\rm{2}}} = {\rm{CH}} - {\rm{Cl}} + {\rm{HCl}}\end{array}\]
13.20
Vinyl acetate có công thức CH3COOCH=CH2, là một ester được dùng nhiều trong lĩnh vực sản xuất keo, sơn, làm chất nhũ hoá các sản phẩm như súp, nước sốt, ... Vinyl acetate được điều chế từ hỗn hợp gồm acetic acid, ethylene và oxygen dưới sự có mặt của xúc tác palladium ở 175 °C – 200 °C và áp suất 5 bar – 9 bar. Viết phương trình phản ứng minh hoạ điều chế vinyl acetate.

Chất phản ứng: acetic acid, ethylene và oxygen.
Sản phẩm: vinyl acetate.
Điều kiện phản ứng: xúc tác palladium ở 175 °C – 200 °C và áp suất 5 bar – 9 bar.

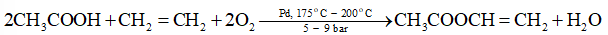
13.21
Ngày nay, các nhà máy thường sử dụng chu trình khép kín hoặc tích hợp các phương pháp để nâng cao hiệu suất, hạ giá thành sản phẩm, đồng thời giảm thiểu ô nhiễm môi trường. Viết các phương trình phản ứng biểu diễn sơ đồ sản xuất sau và cho biết sơ đồ nào là tích hợp các phương pháp sản xuất vinyl chloride? Sơ đồ nào thải sản phẩm phụ ra môi trường?
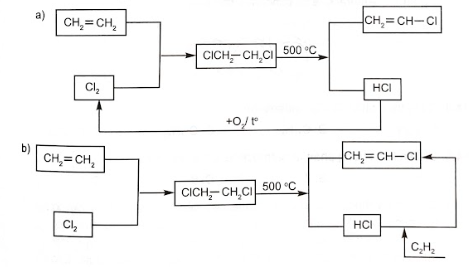

Các phản ứng trên hai sơ đồ gồm:
- Phản ứng cộng chloride vào nối đôi C=C.
- Phản ứng tách hydrogen chloride ra khỏi dẫn xuất halogen.
- Phản ứng cộng HCl vào nối đôi C=C.
Chú ý điều kiện phản ứng đã cho trên sơ đồ.


