25.1
Cặp chất nào sau đây không là đồng phân của nhau?
A. HCHO, CH3CHO. B. CH2=CHCH2OH, CH3CH2CHO.
C. CH3COCH3, CH3CH2CHO. D. CH3COOH, HCOOCH3.

Những hợp chất hữu cơ khác nhau nhưng có cùng công thức phân tử được gọi là các chất đồng phân của nhau.

|
Chất thứ nhất |
Chất thứ hai |
Kết luận |
||
|
Công thức cấu tạo |
Công thức phân tử |
Công thức cấu tạo |
Công thức phân tử |
|
|
HCHO |
CH2O |
CH3CHO |
C2H4O |
Không là đồng phân của nhau. |
|
CH2=CHCH2OH |
C3H6O |
CH3CH2CHO |
C3H6O |
Là đồng phân của nhau. |
|
CH3COCH3 |
C3H6O |
CH3CH2CHO |
C3H6O |
Là đồng phân của nhau. |
|
CH3COOH |
C2H4O2 |
HCOOCH3 |
C2H4O2 |
Là đồng phân của nhau. |
→ Chọn A.
25.2
Ba chất A, B, C có nhiệt độ sôi được biểu thị như hình sau:
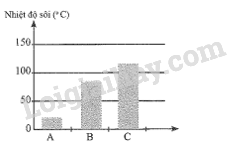
Các chất A, B, C lần lượt là
A. ethanol, acetaldehyde, acetic acid. B. acetaldehyde, ethanol, acetic acid.
C. acetaldehyde, acetic acid, ethanol. D. acetic acid, acetaldehyde, ethanol.

Với các hợp chất có khối lượng phân tử tương đương:
Thứ tự tăng dần về nhiệt độ sôi của các chất là: alkane

C có nhiệt độ sôi cao nhất, nên C là acetic acid.
A có nhiệt độ sôi thấp nên A là acetaldehyde.
Chất B còn lại là ethanol.
→ Chọn B.
25.3
Để phân biệt aldehyde và ketone, có thể dùng thuốc thử nào sau đây?
A. Dung dịch acid. B. Dung dịch base.
C. I2 trong môi trường kiềm. D. Dung dịch AgNO3 trong NH3

Ketone không bị oxi hoá bởi thuốc thử Tollens, aldehyde bị oxi hoá bởi thuốc thử Tollens, vì vậy có thể dùng thuốc thử Tollens để phân biệt aldehyde với ketone và các hợp chất khác.

Để phân biệt aldehyde và ketone, có thể dùng thuốc thử là dung dịch AgNO3 trong NH3.
→ Chọn D.
25.4
Nhận xét nào sau đây không đúng?
A. Aldehyde vừa có tính oxi hoá, vừa có tính khử.
B. Chỉ có ketone tham gia phản ứng tạo iodoform.
C. Acid và ester no, đơn chức, mạch hở có công thức chung là CnH2nO2.
D. Carboxylic acid làm đổi màu giấy quỳ.

- Các hợp chất carbonyl bị khử bởi các tác nhân khử như NaBH4, LiAlH4, … (kí hiệu: [H]) tạo thành các alcohol tương ứng: aldehyde bị khử thành alcohol bậc I, ketone bị khử thành alcohol bậc II.
Aldehyde dễ bị oxi hoá bởi các tác nhân oxi hoá thông thường như: Br2/H2O, [Ag(NH3)2]OH, Cu(OH)2/OH- ….
- Các hợp chất aldehyde, ketone có nhóm methyl cạnh nhóm carbonyl có thể phản ứng với I2 trong môi trường kiềm.
- Acid và ester no, đơn chức, mạch hở có công thức chung là CnH2nO2 với n ≥ 1.
- Carboxylic acid có tính acid yếu làm quỳ tím hóa đỏ.

Nhận xét B không đúng vì ngoài ketone (có nhóm methyl cạnh nhóm carbonyl) tham gia phản ứng tạo idoform, còn có aldehyde (có nhóm methyl cạnh nhóm carbonyl) tham gia phản ứng tạo idoform ví dụ như CH3CHO.
→ Chọn B.
25.5
Cho các chất sau: Na, NaOH, Cu, CuO, CaCO3, CaSO4.
Số chất phản ứng được với acetic acid là
A. 3. B. 4. C. 5. D. 6.

Carboxylic acid có tính acid yếu:
+ Làm quỳ tím hóa đỏ.
+ Tác dụng với kim loại đứng trước hydrogen trong dãy hoạt động hóa học, giải phóng khí hydrogen.
+ Tác dụng với base, oxide base.
+ Tác dụng với một số muối.

Các chất phản ứng với acetic acid là Na, NaOH, CuO, CaCO3.
→ Chọn B.
25.6
Số đồng phân cấu tạo mạch hở của acid và ester có công thức phân tử C4H6O2 (không tính đồng phân hình học) là
A. 5. B. 6. C. 7. D. 8.

Advertisements (Quảng cáo)
Carboxylic acid là các hợp chất hữu cơ trong phân tử có nhóm carboxyl (−COOH) liên kết với nguyên tử carbon (trong gốc hydrocarbon hoặc – COOH) hoặc nguyên tử hydrogen.
Ester đơn chức có công thức chung là RCOOR’ , trong đó R là gốc hydrocarbon hoặc H ; R’ là gốc hydrocarbon.

Các đồng phân cấu tạo mạch hở của acid và ester có công thức phân tử C4H6O2 (không tính đồng phân hình học) là
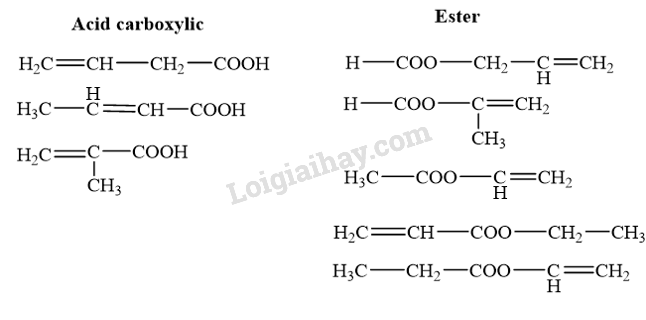
→ Chọn D.
25.7
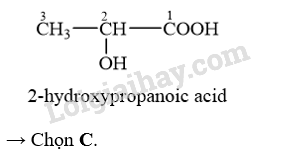
Lactic acid là một acid có trong sữa chua, dưa muối. Lactic acid có công thức cấu tạo là CH3CH(OH)COOH. Tên theo danh pháp thay thế của lactic acid là
A. 2-methylhydroxyethanoic acid. B. 2-methylhydroxyacetic acid.
C. 2-hydroxypropanoic acid. D. 2-hydroxypropanoic acid.

Tên theo danh pháp thay thế của carboxylic acid đơn chức, mạch hở:
Số chỉ vị trí nhánh-Tên nhánh +Tên hydrocarbon ứng với mạch chính (bỏ kí tự e ở cuối) + oic + acid.

25.8
Có bốn chất lỏng có thể tích bằng nhau là ethanol, acetone, acetaldehyde, acetic acid. Tiến hành chưng cất hỗn hợp này, sau một thời gian, hàm lượng chất nào trong bình chưng cất còn lại lớn nhất?
A. Ethanol. B. Acetone. C. Acetaldehyde. D. Acetic acid.

- Chưng cất là phương pháp tách chất dựa vào sự khác nhau về nhiệt độ sôi của các chất trong hỗn hợp ở một áp suất nhất định.
- Với các hợp chất có khối lượng phân tử tương đương:
Thứ tự tăng dần về nhiệt độ sôi của các chất là: alkane

Do acetic acid có nhiệt độ sôi cao nhất nên khi tiến hành chưng cất hỗn hợp, hàm lượng acetic acid còn lại trong bình chưng cất là lớn nhất.
→ Chọn D.
25.9
Cho ba chất lỏng riêng biệt sau: C2H5OH, CH3CHO, CH3COOH.
Cách nào sau đây phù hợp để phân biệt ba chất lỏng trên?
A. Dùng quỳ tím, sau đó dùng dung dịch NaOH.
B. Dùng quỳ tím, sau đó dùng dung dịch AgNO3 trong NH3.
C. Dùng Na sau đó dùng dung dịch AgNO3 trong NH3.
D. Dùng Na sau đó dùng quỳ tím.

Carboxylic acid làm quỳ tím hóa đỏ, aldehyde có phản ứng tráng bạc với dung dịch AgNO3 trong NH3.

Có thể dùng quỳ tím, sau đó dùng dung dịch AgNO3 trong NH3 để nhận biết C2H5OH, CH3CHO, CH3COOH.
|
C2H5OH |
CH3CHO |
CH3COOH |
|
|
Quỳ tím |
Không đổi màu. |
Không đổi màu. |
Hóa đỏ |
|
Dung dịch AgNO3 trong NH3 |
Không hiện tượng. |
Kết tủa bạc. |
|
→ Chọn B.
25.10
Hoàn thành sơ đồ chuyền hoá sau và viết các phương trình hoá học, ghi rõ điều kiện phản ứng (nếu có).
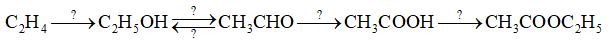

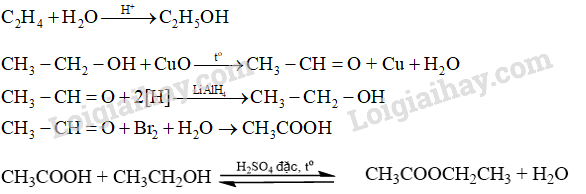
Phản ứng cộng nước của alkene trong môi trường acid.
Phản ứng oxi hóa không hoàn toàn alcohol bằng CuO, to.
Phản ứng khử aldehyde với xúc tác LiAlH4.
Phản ứng oxi hóa aldehyde tạo acid carboxylic.
Phản ứng ester hóa.

25.11
Hỗn hợp X gồm hai acid no, đơn chức, kế tiếp nhau trong dãy đồng đẳng. Cho X tác dụng với Na2CO3, thu được 2,231 lít khí (đkc) và 16,2 g muối acid hữu cơ. Xác định công thức cấu tạo của hai acid trong hỗn hợp X.

Tìm \(\overline {\rm{M}} \)của hai gốc acid rồi suy ra công thức cấu tạo.

\({{\rm{n}}_{{\rm{C}}{{\rm{O}}_{\rm{2}}}}} = \frac{{2,231}}{{24,79}} \approx 0,09{\rm{ (mol)}}\)
Gọi công thức chung của hai acid là R-COOH.
Phương trình phản ứng: \({\rm{2R - COOH}} + {\rm{N}}{{\rm{a}}_{\rm{2}}}{\rm{C}}{{\rm{O}}_{\rm{3}}} \to {\rm{R - COONa}} + {\rm{C}}{{\rm{O}}_{\rm{2}}} + {{\rm{H}}_{\rm{2}}}{\rm{O}}\)
\(\begin{array}{l} \Rightarrow {{\rm{n}}_{{\rm{R - COONa}}}}{\rm{ = 2}}{{\rm{n}}_{{\rm{C}}{{\rm{O}}_{\rm{2}}}}}{\rm{ = 2}} \times {\rm{0,09 = 0,18 (mol)}}\\ \Rightarrow {{\rm{M}}_{{\rm{R - COONa}}}}{\rm{ = }}\frac{{16,2}}{{0,18}} = 90{\rm{ (g/mol)}}\\ \Rightarrow {\overline {\rm{M}} _{\rm{R}}} = 90 - (12 + 16 \times 2 + 23) = 23\end{array}\)
Vì X gồm hai acid no, đơn chức, kế tiếp nhau trong dãy đồng đẳng nên \(23 3- và C2H5-
Vậy hai acid cần tìm là CH3COOH và C2H5COOH.
25.12
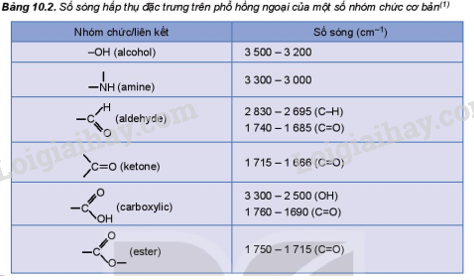
Ba hợp chất thơm A, B, C đều có ứng dụng trong thực tiễn: A có tác dụng chống sinh vật kí sinh (chấy, rận); B làm chất tạo mùi hạnh nhân; C là chất bảo quản thực phẩm do có tác dụng kháng nấm, diệt khuẩn. A có công thức phân tử là C7H8O, phổ IR của A có peak hấp thụ ở vùng 3300 cm-1. Xác định công thức cấu tạo của A, B, C và viết các phương trình hoá học hoàn thành sơ đồ chuyển hoá sau:
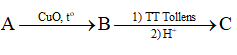

Alcohol bậc I bị oxi hóa không hoàn toàn tạo thành aldehyde.
Aldehyde bị oxi hoá bởi thuốc thử Tollens, vì vậy có thể dùng thuốc thử Tollens.


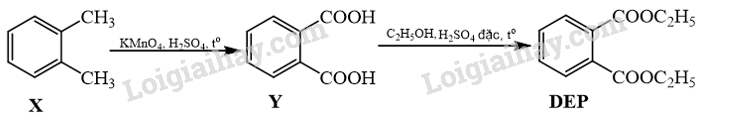
25.13
Diethyl phthalate (còn gọi là DEP) được sử dụng làm thuốc trị ghẻ ngứa, côn trùng đốt. DEP có chứa vòng benzene và hai nhóm thế ở vị trí ortho. DEP được tổng hợp từ hydrocarbon thơm X có công thức phân tử C8H10 theo sơ đồ sau đây. Xác định công thức cấu tạo của X, Y, DEP.
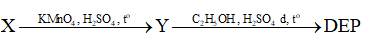

Alkylbenzene tác dụng được với dung dịch KMnO4 trong môi trường acid tạo carboxylic acid.
Phản ứng ester hóa là phản ứng giữa alcohol và carboxylic acid:
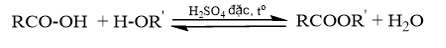

X có chứa vòng benzene và có CTPT C8H10. Do DEP có hai nhóm thế ở vị trí ortho nên X sẽ có hai nhánh ở vị trí ortho. Vậy X là o-dimethylbenzene. Oxi hóa X sẽ tạo diacid Y (phtalic acid). Ester hóa Y sẽ tạo thành DEP.