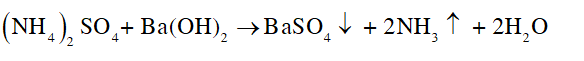Trình bày cách sử dụng dung dịch barium hydroxide để phân biệt ba phân đạm có thành phần chính lần lượt là NaNO3, NH4Cl, (NH4)2SO4.

Ion được nhận biết nhờ phản ứng với ion Ba2+ tạo kết tủa BaSO4 màu trắng. Kết tủa này không tan trong dung dịch acid và base.
Ion ammonium . Khi phản ứng với dung dịch kiềm, sinh khí NH3 (ammonia) có mùi khai, xốc.

Đánh số thứ tự từng mẫu phân đạm, trích mẫu thử sang ống nghiệm đánh số tương ứng.
Advertisements (Quảng cáo)
Cho lần lượt từng mẫu thử tác dụng với dung dịch barium hydroxide (Ba(OH)2), đun nóng nhẹ:
- Mẫu thử nào tan và không có hiện tượng gì thêm thì mẫu thử đó là NaNO3.
- Mẫu thử nào tan và xuất hiện khí có mùi khai, xốc thì mẫu thử đó là NH4Cl:
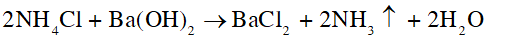
- Mẫu thử nào tan, xuất hiện kết tủa trắng và khí có mùi khai, xốc thì mẫu thử đó là (NH4)2SO4: