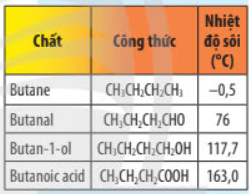
So sánh nhiệt độ sôi của butanoic acid với nhiệt độ sôi của các chất trong bảng sau. Giải thích.

Do cấu tạo của nhóm carboxyl nên carboxylic acid có khả năng tạo thành liên kết hydrogen bền vững hơn liên kết hydrogen giữa các phân tử alcohol, do đó ảnh hưởng lớn đến tính chất vật lý của chúng.
Nhiệt độ sôi của carboxylic acid cao hơn nhiệt độ sôi của alcohol, aldehyde, ketone tương ứng vì có liên kết hydrogen giữa 2 phân tử hoặc giữa nhiều phân tử.

Advertisements (Quảng cáo)
Butanoic acid có nhiệt độ sôi lớn nhất. Giải thích:
+ Butanoic acid có nhiệt độ sôi cao hơn butan-1-ol vì liên kết O–H trong nhóm carboxyl phân cực hơn liên kết O-H trong alcohol, dẫn đến liên hydrogen trong các phân tử butanoic acid bền hơn liên kết hydrogen giữa các phân tử butan-1-ol.
+ Các phân tử butanal không tạo được liên kết hydrogen nên nhiệt độ sôi của butanal thấp hơn nhiệt độ sôi của butan-1-ol.
+ Phân tử butanal phân cực hơn butane, do đó nhiệt độ sôi của butanal cao hơn butane.
=> Thứ tự tăng dần về nhiệt độ sôi của các chất là: butane < butanal < butan-1-ol < butanoic acid.
