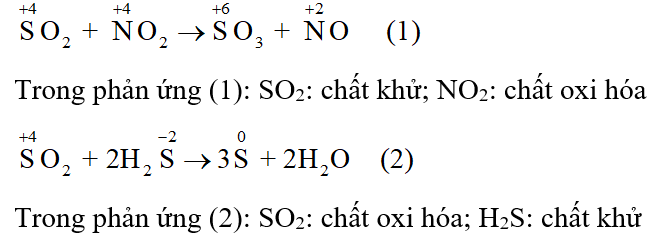Trả lời câu hỏi trang 38 Câu hỏi1 Bài 6. Sulfur và sulfurdioxide sách Hóa học 11 - Chân trời sáng tạo
Xác định tính oxi hóa, tính khử của mỗi chất trong các phản ứng hóa học (1) và (2).
\[\begin{array}{l}{\rm{S}}{{\rm{O}}_{\rm{2}}}{\rm{ + N}}{{\rm{O}}_{\rm{2}}} \to {\rm{S}}{{\rm{O}}_{\rm{3}}}{\rm{ + NO (1)}}\\{\rm{S}}{{\rm{O}}_{\rm{2}}}{\rm{ + 2}}{{\rm{H}}_{\rm{2}}}{\rm{S}} \to 3{\rm{S + 2}}{{\rm{H}}_2}{\rm{O (2)}}\end{array}\]

Advertisements (Quảng cáo)
Trong phản ứng oxi hóa khử, chất khử là chất cho electron, có số oxi hóa tăng; chất oxi hóa là chất nhận electron, có số oxi hóa giảm.