Câu hỏi trang 38 Mở đầu (MĐ)
Để tạo thành phức chất bát diện, cation Co3+ nhận 6 cặp electron chưa liên kết từ các anion hoặc phối tử. Quan sát Hình 6.1, hãy dự đoán cần bao nhiêu phân tử ethylenediamine để tạo phức chất với một cation Co3+. Giải thích.
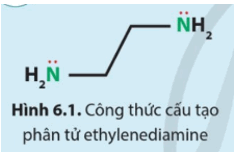

Dựa vào cation Co3+ nhận 6 cặp electron chưa liên kết từ các anion hoặc phối tử.

Cần 3 phân tử ethylenediamine để tạo phức chất với một cation Co3+, vì mỗi phân tử ethylenediamine có 2 cặp electron chưa liên kết.
Câu hỏi trang 38 Câu hỏi
Cặp anion F- và CN- đã cho cặp electron liên kết để trở thành phối tử trong hai phức chất: [FeF6]4- và [Fe(CN)6]3-.
Cho biết số oxi hóa của nguyên tử trung tâm trong mỗi phức chất trên.

Dựa vào nguyên tử trung tâm và số phối trí của nguyên tử trung tâm trong phức chất.

Gọi số oxi hóa của Fe trong phức chất [FeF6]4- là x ta có: x + (-1).6 = 4- \( \to \)x = +2
Gọi số oxi hóa của Fe trong phức chất [Fe(CN)6]3- là x ta có: x + (-1).6 = 3- \( \to \)x = +3.
Câu hỏi trang 39 Luyện tập (LT) 1
Cho biết số oxi hóa của nguyên tử trung tâm trong hai phức chất sau:
[Ni(CO)4] và [NiCl4]2-.

Dựa vào cách xác định số oxi hóa.

Gọi số oxi hóa của Ni trong phức [Ni(CO)4] là x ta có: x + (-1).4 = 0 \( \to \)x = +4
Gọi số oxi hóa của Ni trong phức [NiCl4]2- là x ta có: x + (-1).4 = -2 \( \to \)x = +2.
Câu hỏi trang 39 Câu hỏi
Số phối trí của nguyên tử trung tâm trong phức chất tứ diện, vuông phẳng và bát diện lần lượt là bao nhiêu?

Dựa vào nguyên tử trung tâm và số phối trí của nguyên tử trung tâm trong phức chất.

Số phối trí của nguyên tử trung tâm trong phức chất tứ diện, vuông phẳng và bát diện lần lượt là 4, 4, và 6.
Câu hỏi trang 39 Luyện tập (LT) 2
Hãy cho biết số phối trí của nguyên tử trung tâm trong phức chất [Ni(OH2)6]2+ và phức chất [NiCl4]2-.

Dựa vào số phối trí của nguyên tử trung tâm trong phức chất là số liên kết σ giữa nguyên tử trung tâm và các phối tử.

Số phối trí trong phức [Ni(OH2)6]2+ là: 6
Số phối trí trong phức [NiCl4]2- là: 4
Câu hỏi trang 40 Câu hỏi
Mỗi loại phối tử trong phức chất ở Hình 6.2 có dung lượng phối trí là bao nhiêu?
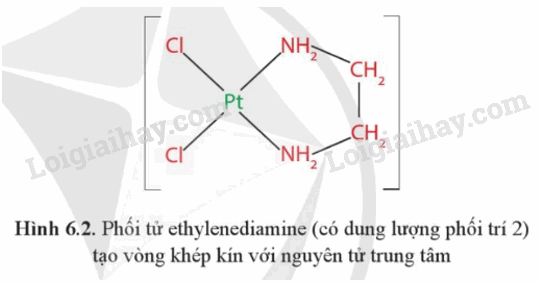

Dựa vào khái niệm dung lượng phối trí.

Phối tử ethylenediamine thường có dung lượng phối trí 2.
Câu hỏi trang 40 Luyện tập (LT)
Vì sao trong nhiều phức chất, ethyleneglycol (HOCH2CH2OH) là phối tử có dung lượng phối trí 2?
Advertisements (Quảng cáo)

Dựa vào khái niệm dung lượng phối trí.

Trong quá trình tạo thành phức chất, ethyleneglycol (HOCH2CH2OH) có thể cho nguyên tử trung tâm hai cặp electron chưa liên kết của 2 nguyên tử O để hình thành hai liên kết s với nguyên tử trung tâm theo kiểu cho – nhận nên trong nhiều phức chất, ethyleneglycol (HOCH2CH2OH) là phối tử có dung lượng phối trí 2.
Câu hỏi trang 41
Chlorophyll b là một phức chất tạo nên màu xanh của lá. Hãy cho biết:
a) Số phối trí của nguyên tử trung tâm.
b) Số phối tử trong một phân tử phức chất.
c) Dung lượng phối trí của phối tử.

dựa vào hình sau: 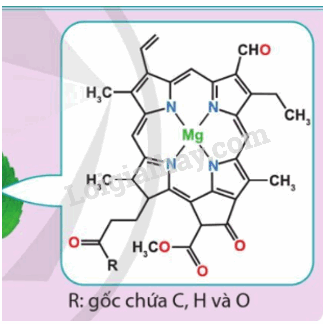

a) số phối trí của nguyên tử trung tâm là 4.
b) số phối tử trong một phân tử phức chất là 4.
c) Dung lượng phối trí của phối tử là 1.
Cation Co3+ tạo nguyên tử trung tâm có số phối trí 6. Viết công thức của các phức chất tạo bởi: một cation Co3+ với các phân tử NH3; một cation Co3+ với hai anion Cl- và các phân tử NH3.

Dựa vào kiến thức về phức chất.

Công thức phức chất lần lượt là: [Co(NH3)6]3+; [Co(Cl)6]3+
Với phức chất có công thức [Pt(en)2]2+, hãy cho biết:
a) Nguyên tử trung tâm và phối tử.
b) Số phối trí của nguyên tử trung tâm.
c) Dung lượng phối trí của phối tử.

Dựa vào kiến thức về phức chất.

a) Nguyên tử trung tâm là Pt; phối tử là NH2[CH2]2NH2.
b) Số phối trí là 4.
c) Dung lượng phối trí của phối tử là 2.
Xét phức chất có cấu tạo như hình dưới đây, hãy cho biết:
a) Nguyên tử trung tâm và phối tử.
b) Số phối trí của nguyên tử trung tâm
c) Dung lượng phối trí của phối tử.
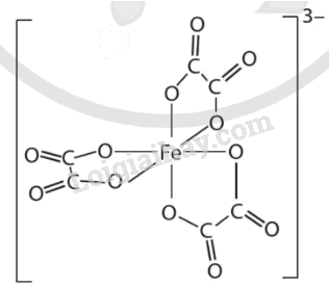

Dựa vào kiến thức về phức chất.

a) Nguyên tử trung tâm là Fe; phối tử là 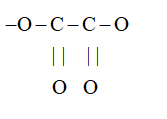
b) Số phối trí là 3
c) Dung lượng phối trí của phối tử là 2.
