2.7
Hình nào sau đây không phải là đồ thị biểu diễn quá trình đẳng nhiệt?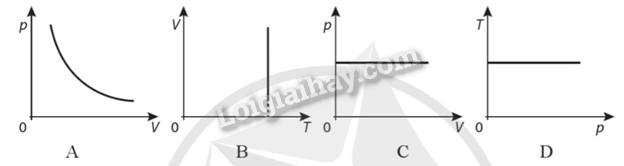

Vận dụng kiến thức về quá trình đẳng nhiệt

Hình C là quá trình đẳng tích
Đáp án: C
2.8
Đâu là nhóm các thông số trạng thái của một lượng khí xác định?
A. Áp suất, nhiệt độ, thể tích.
B. Áp suất, nhiệt độ, khối lượng.
C. Khối lượng, nhiệt độ, thể tích.
D. Khối lượng, áp suất, thể tích.

Vận dụng lý thuyết về trạng thái của một lượng khí xác định

Trạng thái của một lượng khí xác định bao gồm: áp suất, nhiệt độ, thể tích.
Đáp án: A
2.9
Hệ thức nào sau đây thể hiện đúng mối liên hệ giữa các thông số trạng thái khí lý tưởng trong quá trình đẳng áp?
A. \({p_1}{V_1} = {p_2}{V_2}\)
B. \(\frac{{{V_1}}}{{{T_1}}} = \frac{{{V_2}}}{{{T_2}}}\)
C.\({V_1}{T_1} = {V_2}{T_2}\)
D. \(\frac{{{p_1}}}{{{T_1}}} = \frac{{{p_2}}}{{{T_2}}}\)

Vận dụng kiến thức về quá trình đẳng áp

Mối liên hệ giữa các thông số trạng thái khí lý tưởng trong quá trình đẳng áp là: \(\frac{{{V_1}}}{{{T_1}}} = \frac{{{V_2}}}{{{T_2}}}\)
Đáp án: B
2.10
Đồ thị nào sau đây biểu diễn quá trình biến đổi trạng thái của khí lý tưởng khi áp suất không đổi?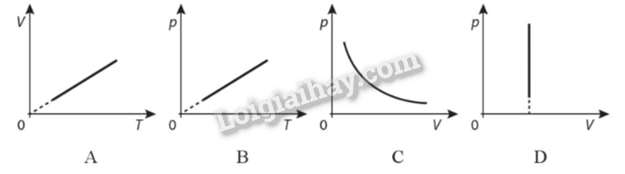

Vận dụng kiến thức về quá trình đẳng áp

Hình A làquá trình đẳng áp
Đáp án: A
2.11
Trong quá trình nào sau đây, cả ba thông số trạng thái p, V, T của một lượng khí xác định đều thay đổi?
A. Không khí được nung nóng trong một bình đậy kín.
B. Không khí trong một phòng mở cửa khi nhiệt độ môi trường và áp suất khí quyển tăng lên.
C. Khi nitrogen trong quả bóng bay bị bóp xẹp từ từ.
D. Khí oxygen trong bình kín vừa được làm lạnh vừa được nén cho áp suất không đổi.

Vận dụng kiến thức về quá trình đẳng áp

Không khí trong một phòng mở cửa khi nhiệt độ môi trường và áp suất khí quyển tăng lên làm cả ba thông số trạng thái p, V, T đều thay đổi
Đáp án: B
2.12
Một lượng khí ở nhiệt độ 30 °C có thể tích 1,0 m3 và áp suất 2,0.105 Pa. Thực hiện nén khí đẳng nhiệt đến áp suất 3,5.105 Pa thì thể tích của lượng khí là
A. 0,6.105 m3.
B. 1,75 m3.
C. 0,6.10-5 m3.
D. 0,6 m3.

Vận dụng kiến thức về quá trình đẳng nhiệt

\({p_1}{V_1} = {p_2}{V_2} \to {V_2} = \frac{{{p_1}{V_1}}}{{{p_2}}} = \frac{{{{2.10}^5}.1}}{{{{3,5.10}^5}}} = \frac{4}{7} \approx 0,6({m^3})\)
Đáp án: D
2.13
Trong các phát biểu sau đây, phát biểu nào đúng, phát biểu nào sai?
a) Một lượng khí được xác định bởi số các phân tử khí.
b) Đường đẳng nhiệt trong hệ toạ độ (p – T) là đường hypebol.
c) Định luật Boyle cho biết mối liên hệ tỉ lệ thuận giữa áp suất và thể tích của một lượng khí xác định khi nhiệt độ không đổi.
d) Định luật Boyle cho biết mối liên hệ tỉ lệ nghịch giữa áp suất và thể tích của một lượng khí xác định khi nhiệt độ không đổi.

Vận dụng kiến thức về quá trình đẳng khí

a) Đúng
b) Sai. Đường đẳng nhiệt trong hệ toạ độ (p – T) là đường thẳng
c) Sai. Định luật Boyle cho biết mối liên hệ tỉ lệ nghịch giữa áp suất và thể tích của một lượng khí xác định khi nhiệt độ không đổi.
d) Đúng
2.14
Trong các phát biểu sau đây, phát biểu nào đúng, phát biểu nào sai?
a) Định luật Charles là định luật thu được từ kết quả thực nghiệm về chất khí.
b) Đường biểu diễn quá trình đẳng áp của một lượng khí trong hệ toạ độ (V-T) là đường thẳng kéo dài đi qua gốc toạ độ.
c) Trong quá trình đẳng áp, thể tích của một lượng khi luôn tỉ lệ nghịch với nhiệt độ (K) của lượng khi đó.
d) Phương trình trạng thái của khí lý tưởng thể hiện mối liên hệ giữa nhiệt độ, khối lượng và áp suất của một lượng khí.

Vận dụng kiến thức về quá trình đẳng khí

a) Đúng
b) Đúng
c) Sai. Trong quá trình đẳng áp, thể tích của một lượng khi luôn tỉ lệ thuận với nhiệt độ (K) của lượng khi đó.
d) Sai. Phương trình trạng thái của khí lý tưởng thể hiện mối liên hệ giữa nhiệt độ, thể tích và áp suất của một lượng khí.
2.15
Trong các phát biểu sau đây, phát biểu nào đúng, phát biểu nào sai?
a) Khi thể tích được giữ không đổi, áp suất của một lượng khí tỉ lệ nghịch với
nhiệt độ.
b) Với một lượng khí lý tưởng thì \(\frac{{pV}}{T}\)là hằng số.
Advertisements (Quảng cáo)
c) Khi nhiệt độ tăng từ 20 °C lên 40 °C thì áp suất của một lượng khí trong bình kín sẽ tăng lên hai lần.
d) Đường biểu diễn quá trình đẳng tích (thể tích không đổi) của một lượng khí trong hệ toạ độ (p - T) là đường thẳng kéo dài đi qua gốc toạ độ.

Vận dụng kiến thức về quá trình đẳng khí

a) Sai. Khi thể tích được giữ không đổi, áp suất của một lượng khí tỉ lệ thuận với
nhiệt độ.
b) Đúng
c) Sai. Khi nhiệt độ tăng từ 20 °C lên 40 °C \( \Leftrightarrow \) t1 = 293 K; t2 = 313 K thì áp suất của một lượng khí trong bình kín sẽ tăng lên 1,07 lần.
d) Đúng
2.16
Buồng chứa sản phẩm điều chế là khí hydrogen được giữ ở 20,0 °C và áp suất 1,00 atm. Cần lấy ..... m3 khí hydrogen từ buồng này để nạp đầy bình có thể tích 0,0500 m3 và áp suất 25,0 atm. Coi quá trình nạp khí được giữ cho nhiệt độ không đổi.

Vận dụng kiến thức về quá trình đẳng nhiệt

Áp dụng định luật Boyle, ta có:
\({p_1}{V_1} = {p_2}{V_2} \Leftrightarrow {V_1} = \frac{{{p_2}{V_2}}}{{{p_1}}} = \frac{{25.0,05}}{1} = 1,25({m^3})\)
2.17
Một bình chứa oxygen ở điều kiện bảo quản 20,0 °C thì có áp suất 5,0 atm. Nếu nhiệt độ phòng bảo quản tăng lên 40,0 °C thì áp suất của bình là ....atm

Vận dụng kiến thức về quá trình đẳng tích

Áp dụng định luật Sác-lơ, ta có:
\(\frac{{{p_1}}}{{{T_1}}} = \frac{{{p_2}}}{{{T_2}}} \Leftrightarrow {p_2} = \frac{{{p_1}{T_2}}}{{{T_1}}} = \frac{{5.313}}{{293}} \approx 5,34(atm)\)
2.18
Một bình chứa khí có vách ngăn di chuyển được. Khi dịch vách ngăn để bình có thể tích 15,0 lít ở nhiệt độ 27,0 °C thì áp suất khí trong bình là 1,50 atm. Tiếp tục dịch chuyển vách ngăn để nén khi đến thể tích 12,0 lít thì áp suất khí trong bình là 3,00 atm. Nhiệt độ của khí trong bình lúc này là ...... C.

Vận dụng kiến thức về quá trình đẳng khí

\(\frac{{{p_1}{V_1}}}{{{T_1}}} = \frac{{{p_2}{V_2}}}{{{T_2}}} \Leftrightarrow {T_2} = \frac{{{p_2}{V_2}{T_1}}}{{{p_1}{V_1}}} = \frac{{3.12.300}}{{1,5.15}} = 480(K) = 207{(^o}C)\)
2.19
Ở điều kiện tiêu chuẩn (nhiệt độ 0 °C và áp suất 1,00 atm) thì khí oxygen có khối lượng riêng là 1,43 kg/m . Tính khối lượng khí oxygen gây ra áp suất 25,0 atm trong bình chứa 10,0 lít ở 0 °C.

Vận dụng kiến thức về quá trình đẳng khí

Áp dụng định luật Boyle, ta có:
\({p_1}{V_1} = {p_2}{V_2} \Leftrightarrow {V_1} = \frac{{{p_2}{V_2}}}{{{p_1}}} = \frac{{25.10}}{1} = 250(l) = {250.10^{ - 3}}({m^3})\)
Khối lượng khí oxygen gây ra áp suất 25 atm trong bình chứa 10 lít ở 0 °C là:
m = pV1 = 1,43.250.10-3 = 0,3575 = 35,75.10-2 (kg)
2.20
Để mở nút chai bị kẹt, một người dùng cách hơ nóng khí trong chai. Biết rằng khí trong chai lúc chưa hơ nóng thì có áp suất bằng áp suất khí quyển 1,0.105 Pa và
có nhiệt độ là 7 °C. Để làm nút bật ra cần có chênh lệch áp suất giữa khí trong chai và bên ngoài là 0,6.105 Pa. Người này cần làm khí trong chai nóng đến nhiệt độ ít nhất bằng bao nhiêu để nút chai bật ra?

Vận dụng kiến thức về quá trình đẳng tích

Áp dụng định luật Sác-lơ, ta có:
\(\frac{{{p_1}}}{{{T_1}}} = \frac{{{p_2}}}{{{T_2}}} \Leftrightarrow {T_2} = \frac{{{p_2}{T_2}}}{{{p_1}}} = \frac{{{{1,6.10}^5}.280}}{{{{1.10}^5}}} = 448(K)\)
2.21
Một mol khí lý tưởng có các quá trình biến đổi. giữa ba trạng thái 1, 2, 3 được biểu diễn trong hệ toạ độ thể tích V (m3) - nhiệt độ T (K) như đồ thị Hình 2.3. Hãy vẽ đồ thị biểu diễn các quá trình này của mol khí trong hệ toạ độ áp suất p (Pa) - nhiệt độ T (K).
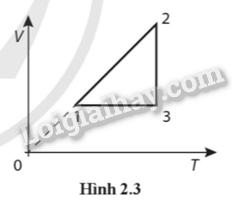

Vận dụng kiến thức về quá trình đẳng khí

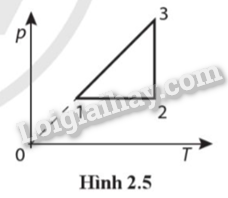
Mol khí có quá trình 1 → 2 là đẳng áp, 2 → 3 là đẳng nhiệt, 3 → 1 là đẳng tích được biểu diễn trong hệ toạ độ (p − T) như Hình 2.5.
2.22
Bóng thám không là một thiết bị thường dùng trong ngành khí tượng để hỗ trợ thu thập các thông số của các tầng khí quyển. Một bóng thám không ở dưới mặt đất được bơm khí ở áp suất 1,00 atm và nhiệt độ 27 °C. Để bóng này khi lên đến tầng khí quyển có áp suất 0,04 atm và nhiệt độ −50 °C vẫn không phình quá 5,00.102 m3 thì thể tích bóng khi được bơm ở mặt đất tối đa là bao nhiêu?

Vận dụng kiến thức về quá trình đẳng khí

\(\frac{{{p_1}{V_1}}}{{{T_1}}} = \frac{{{p_2}{V_2}}}{{{T_2}}} \Leftrightarrow {V_1} = \frac{{{p_2}{V_2}{T_1}}}{{{p_1}{T_2}}} = \frac{{{{0,04.5.10}^2}.300}}{{1.223}} = 26,9({m^3})\)
2.23
Một phòng trống có kích thước 5,0 m × 10,0 m × 3,0 m. Lúc đầu, không khí trong phòng ở điều kiện tiêu chuẩn (nhiệt độ 0,0 °C và áp suất 1,0.105 Pa) và có khối lượng mol là 29 g/mol.
a) Xác định số mol và khối lượng không khí có trong phòng. Biết hằng số khí lý tưởng là R = 8,31 J.mol-1 K-1
b) Khi mở cửa phòng thì nhiệt độ phòng tăng lên 20 °C và áp suất khí trong phòng bằng áp suất bên ngoài phòng là 0,9.105 Pa. Tính khối lượng không khí trong phòng đã thoát ra ngoài.

Vận dụng kiến thức về quá trình đẳng khí

a) pV = nRT → số mol không khí trong phòng là n = 6,6.103 mol.
Khối lượng không khí trong phòng là m = 1,9.102 g.
b) Xét lượng khí trong phòng lúc đầu khi ở nhiệt độ 20 °C và áp suất 0,9.105 Pa có thể tích là V2 = 178 m3 lớn hơn thể tích phòng V1 = 150 m3. Như vậy, đã có ∆V = 28 m3 khí ở nhiệt độ 20 °C và áp suất 0,9.105 Pa thoát ra khỏi phòng.
Khối lượng không khí trong phỏng đã thoát ra ngoài bằng:
\(\Delta m = \frac{{28}}{{178}}m = \frac{{14}}{{89}}({1,9.10^2}) = {0,3.10^2}(g)\)
2.24
Một người chế tạo dụng cụ đo độ nghiêng của bề mặt nằm ngang là một ống thuỷ tinh tiết diện S nhỏ được bịt kín hai đầu. Trong ống có chứa khí và ở giữa ống có một cột thuỷ ngân (Hg) dài l. Khi đặt ống trên mặt phẳng nằm ngang, cột thuỷ ngân nằm chính giữa ống (Hình 2.4a) và phần ống chứa khí ở hai đầu dài L như nhau. Khi dựng ống thẳng đứng, cột thuỷ ngân bị dịch xuống một đoạn ∆l, phần ống chứa khí phía dưới ngắn hơn phần ống phía trên (Hình 2.4b).
a) Vì sao cột thuỷ ngân lại dịch xuống khi dựng ống thẳng đứng?
b) Cho L = 0,50 m; l = 0,10 m; ∆l = 0,05 m. Hãy xác định áp suất po của khí trong ống thuỷ tinh khi ống nằm ngang theo đơn vị cmHg.

Vận dụng kiến thức về quá trình đẳng khí

a) Khi ống thuỷ tinh nằm ngang, phần ống chứa khí ở hai đầu dài bằng nhau nên lượng khí ở hai đầu ống là giống nhau, có thể xem như cùng một lượng khí. Khi dựng ống thuỷ tinh thẳng đứng, áp suất của cột khí phía dưới p1 cân bằng với áp suất của cột khí phía trên p2 và áp suất của cột thuỷ ngân pHg : p1 = p2 + pHg hay
p1 > p2.
Do đó, cột thuỷ ngân dịch xuống để thể tích phần khí phía dưới nhỏ hơn thể tích khí phía trên.
b) \({p_2} = \frac{{{p_{Hg}}(L - \Delta l)}}{{2\Delta l}} = 45(cmHg)\)
Áp dụng định luật Boyle cho lượng khí ở phần ống phía trên:
– Khi ống nằm ngang, lượng khí này có áp suất po và thể tích SL.
– Khi ống thẳng đứng, lượng khí này có áp suất p2 và thể tích S(L + ∆l).
Vậy po = 49,5 cmHg.
