Câu hỏi trang 52 Câu hỏiMở đầu
Để giải các bài tập về sự chuyển trạng thái của khí lí tưởng thì cần dùng những công thức nào? Nêu rõ ý nghĩa và cách dùng của từng công thức.

Vận dụng kiến thức đã học

1. Phương trình trạng thái khí lí tưởng:
P₁V₁/T₁ = P₂V₂/T₂
- Ý nghĩa:
+ Mối liên hệ giữa 4 đại lượng trạng thái (P, V, T) của một lượng khí lí tưởng nhất định.
+ Áp dụng cho các quá trình biến đổi trạng thái của khí lí tưởng.
- Cách dùng:
+ Xác định các đại lượng trạng thái P₁, V₁, T₁, P₂, V₂ và T₂ của khí.
+ Thay các giá trị vào phương trình để tính toán đại lượng còn lại.
2. Định luật Boyle (Quá trình đẳng nhiệt):
P₁V₁ = P₂V₂
- Ý nghĩa:
+ Áp suất và thể tích của một lượng khí lí tưởng tỉ lệ nghịch với nhau khi nhiệt độ không đổi.
- Cách dùng:
+ Áp dụng cho quá trình biến đổi trạng thái của khí lí tưởng trong đó nhiệt độ không đổi.
+ Xác định hai trạng thái (1 và 2) của khí.
+ Sử dụng công thức để tính toán P₂ hoặc V₂ khi biết P₁, V₁ và ngược lại.
3. Định luật Charles (Quá trình đẳng áp):
V₁/T₁ = V₂/T₂
- Ý nghĩa:
+ Thể tích và nhiệt độ tuyệt đối của một lượng khí lí tưởng tỉ lệ thuận với nhau khi áp suất không đổi.
- Cách dùng:
+ Áp dụng cho quá trình biến đổi trạng thái của khí lí tưởng trong đó áp suất không đổi.
+ Xác định hai trạng thái (1 và 2) của khí.
+ Sử dụng công thức để tính toán V₂ hoặc T₂ khi biết V₁, T₁ và ngược lại.
4. Định luật Avogadro:
- Thể tích của các khí lí tưởng ở cùng điều kiện nhiệt độ và áp suất bằng nhau thì chứa số lượng phân tử bằng nhau.
- Ý nghĩa:
+ Mối liên hệ giữa thể tích và số mol của khí lí tưởng ở cùng điều kiện nhiệt độ và áp suất.
- Cách dùng:
+ Áp dụng cho các bài toán liên quan đến so sánh thể tích của các khí lí tưởng.
+ Xác định số mol của các khí và điều kiện nhiệt độ, áp suất.
+ Sử dụng công thức để tính toán thể tích của các khí.
Ngoài ra, một số công thức khác cũng có thể được sử dụng:
Công thức tính số mol:
n = m/M
Công thức tính khối lượng mol:
M = m/n
Công thức tính mật độ khí:
ρ = m/V
Câu hỏi trang 54 Hoạt động
1. Hãy giải bài tập ví dụ 2 bằng cách vẽ đường đẳng tích thay cho đường đẳng áp.
2. Hãy dùng phương trình \(\frac{{pV}}{T}\) = hằng số để giải Bài tập ví dụ 3.

1. Dựa vào Ví dụ 2
2. Dùng phương trình \(\frac{{pV}}{T}\) = hằng số

1.
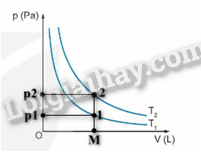
Hình trên cho thấy p1 < p2 vì quá trình chuyển từ trạng thái 1 sang trạng thái 2 là đẳng tích nên T1 < T2
2.
\(\frac{{pV}}{T}\) = hằng số
Câu hỏi trang 54 Bài 1
Advertisements (Quảng cáo)
Một lượng khí ở điều kiện tiêu chuẩn có thể tích 2 m3. Nếu nén đẳng nhiệt lượng khí này tới áp suất 5.105 Pa thì thể tích của lượng khí sẽ là
A. 10 m3.
B. 1 m3.
C. 0,4 m3.
D. 4 m3.

Sử dụng định luật Boyle cho quá trình biến đổi đẳng nhiệt

P₁V₁ = P₂V₂ = 1.105.2 = 5.105.V2
=> V2 = 0,4 m3
Đáp án C
Câu hỏi trang 54 Bài 2
Một bóng thám không có các bộ phận chính như mô tả ở Hình 13.3.
a) Tại sao vỏ bóng phải được làm băng chất liệu đàn hồi?
b) Tại sao để bóng bay lên, người ta phải bơm vào bóng một loại khí có khối lượng riêng nhỏ hơn không khí?
c) Bóng thám không thường chỉ bay lên tới độ cao khoảng từ 30 km đến 40 km là bị vỡ. Tại sao bóng bị vỡ?


Vận dụng lí thuyết về áp suất

a) Vỏ bóng phải được làm bằng chất liệu đàn hồi:
- Khi bơm khí vào, vỏ bóng sẽ căng ra và phình to.
- Chất liệu đàn hồi giúp vỏ bóng có thể co giãn theo áp suất khí bên trong.
- Khi khí thoát ra, vỏ bóng sẽ co lại, giữ cho bóng không bị rách.
b) Bơm khí có khối lượng riêng nhỏ hơn không khí:
- Khí trong bóng thám không thường là heli hoặc hydro.
- Khối lượng riêng của heli và hydro nhỏ hơn nhiều so với không khí.
- Do đó, lực đẩy Archimedes tác dụng lên bóng thám không lớn hơn trọng lượng của bóng, giúp bóng bay lên.
c) Bóng thám không bị vỡ ở độ cao 30 - 40 km:
- Áp suất khí quyển giảm dần theo độ cao.
- Ở độ cao 30 - 40 km, áp suất khí quyển rất thấp.
- Áp suất bên trong bóng thám không không đủ để chống lại áp suất khí quyển bên ngoài, dẫn đến việc bóng bị vỡ.
Câu hỏi trang 54 Bài 3
Một bình dung tích 40 dm3 chứa 3,96 kg khí oxygen. Hỏi ở nhiệt độ nào thì bình có thế bị vỡ, biết bình chỉ chịu được áp suất không quá 60 atm. Lấy khối lượng riêng của oxygen ở điều kiện tiêu chuẩn là 1,43 kg/m3.

Sử dụng phương trình trạng thái khí lý tưởng

\(n = \frac{m}{\rho } = \frac{{3,96}}{{1,43}} = 2,77mol\)
pV = nRT
\( \Rightarrow T = \frac{{pV}}{{nR}} = \frac{{60.0,04}}{{2,77.0,082}} = 116,67^\circ C\)
Câu hỏi trang 54 Bài 4
Một bình chứa một chất khí được nén ở nhiệt độ 27 °C và áp suất 40 atm. Nếu nhiệt độ của khí giảm xuống còn 12 °C và một nửa lượng khí thoát ra khỏi bình thì áp suất khí sẽ bằng bao nhiêu?

Sử dụng kết hợp định luật Boyle và Charles để tính áp suất khí sau khi thay đổi nhiệt độ và số lượng khí

\({p_2} = \frac{{{p_1}{T_2}}}{{{T_1}}} = \frac{{40.285}}{{300}} = 20atm\)
Câu hỏi trang 54 Bài 5
Hình 13.4 vẽ đường biểu diễn bốn quá trình chuyển trạng thái liên tiếp của một lượng khí trong hệ toạ độ (p,T): (1 → 2); (2 → 3); (3 → 4); (4 → 1). Hãy chứng tỏ rằng chỉ có một trong bốn quá trình trên là đăng tích.
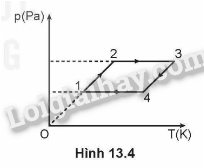

Vận dụng lí thuyết quá trình đẳng tích

Phân tích các quá trính:
(1 → 2): Áp suất tăng, nhiệt độ tăng, quá trình đẳng tích
(2 → 3): Áp suất không đổi, quá trình đẳng áp
(3 → 4): Áp suất giảm, nhiệt độ giảm, quá trình đẳng tích
(4 → 1): Áp suất không đổi, quá trình đẳng áp
