2.1
Có những hạt nào được tìm thấy trong hạt nhân của nguyên tử?
A. Các hạt mang điện tích âm (electron).
B. Các hạt neutron và hạt proton.
C. Các hạt neutron không mang điện.
D. Hạt nhân nguyên tử không chứa hạt nào bên trong.

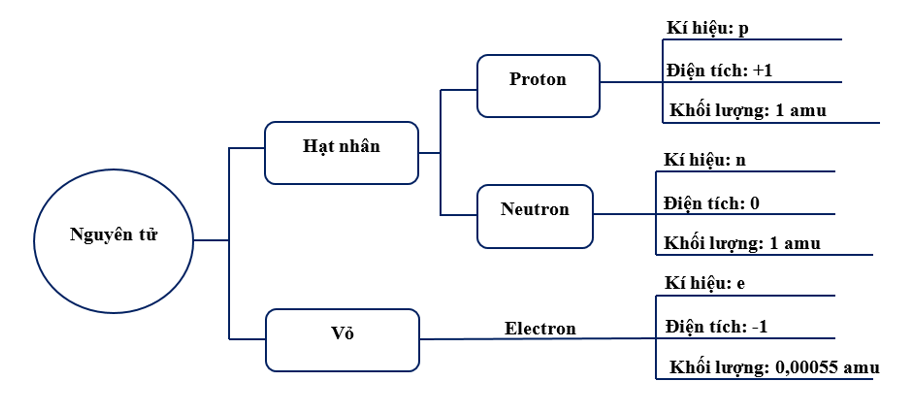

Phát biểu A sai vì hạt electron ở vỏ nguyên tử.
Phát biểu B đúng và phát biểu D sai vì hạt nhân nguyên tử được cấu tạo bởi hai loại hạt là proton và neutron (Riêng với nguyên tử hydrogen, hạt nhân chỉ chứa hạt proton).
Phát biểu C sai vì trong hạt nhân nguyên tử còn có hạt proton mang điện tích dương và hạt neutron không mang điện tích.
⇨ Chọn B.
2.2
Điều nào sau đây mô tả đầy đủ thông tin nhất về proton?
A. Proton là một hạt vô cùng nhỏ và mang điện tích âm.
B. Proton là một hạt mang điện tích dương và được phát hiện trong hạt nhân nguyên tử.
C. Proton là một hạt không mang điện và được tìm thấy trong hạt nhân nguyên tử.
D. Proton là một hạt vô cùng nhỏ, mang điện tích dương và được phát hiện trong hạt nhân nguyên tử.

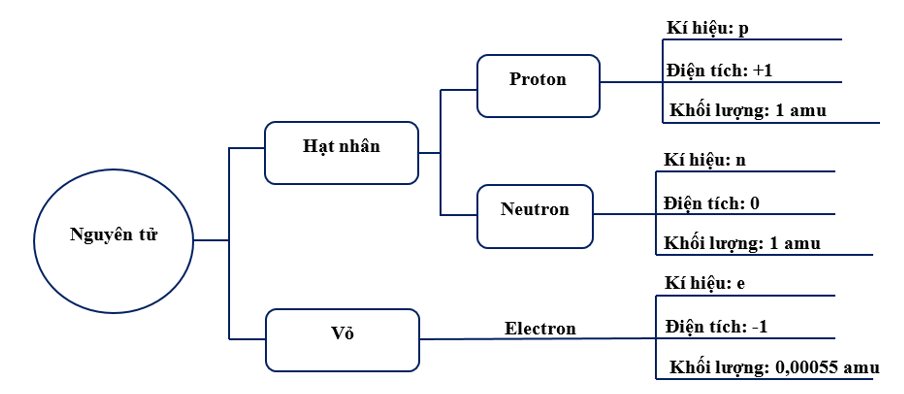
1 amu = 1,6605 x 10-24 (g)

Vì khối lượng của proton là 1 amu (1,6605 x 10-24 g) ⇨ proton là một hạt vô cùng nhỏ.
Proton là nằm ở hạt nhân nguyên tử, mang điện tích dương, mỗi hạt proton mang điện tích +1.
⇨ Chọn D.
2.3
Một đơn vị khối lượng nguyên tử (1 amu) theo định nghĩa có giá trị bằng
A. 1/16 khối lượng của nguyên tử oxygen.
B. 1/32 khối lượng của nguyên tử sulfur.
C. 1/12 khối lượng của nguyên tử carbon.
D. 1/10 khối lượng của nguyên tử boron.

- Khối lượng hạt nhân lớn hơn rất nhiều so với khối lượng vỏ electron nên có thể coi khối lượng nguyên tử tập trung ở hạt nhân.
- Đơn vị khối lượng nguyên tử (atomic mass unit).
- Viết tắt: amu.
- 1 amu = 1,6605 x 10-24 g
- Khối lượng của nguyên tử carbon xấp 12 amu.

Vì khối lượng của nguyên tử carbon là 12 amu.
⇨ 1 amu bằng 1/12 khối lượng nguyên tử carbon.
⇨ Chọn C.
2.4
Trong các nguyên tử sau, nguyên tử nào có khối lượng nguyên tử lớn nhất?
A. Na.
B. O.
C. Ca.
D. H.

- Khối lượng hạt nhân lớn hơn rất nhiều so với khối lượng vỏ electron nên có thể coi khối lượng nguyên tử tập trung ở hạt nhân.
- Đơn vị khối lượng nguyên tử (atomic mass unit).
- Viết tắt: amu.
- 1 amu = 1,6605 x 10-24 g

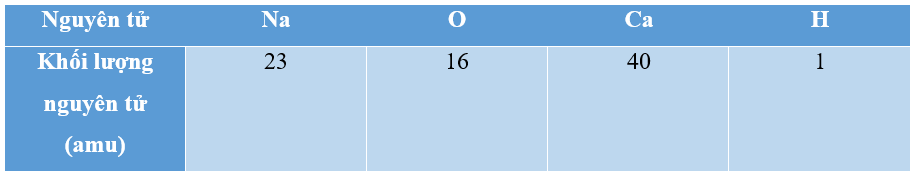
⇨ Chọn C.
2.5
Khối lượng của các hạt dưới nguyên tử (proton, neutron) được đo bằng đơn vị
A. gam.
B. amu.
C. mL.
D. kg.

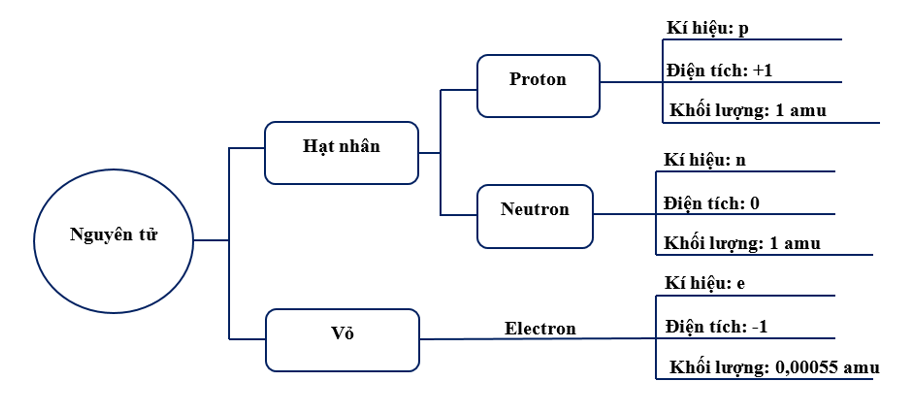

Mỗi hạt proton và neutron có khối lượng xấp xỉ 1 amu.
⇨ Chọn B.
2.6
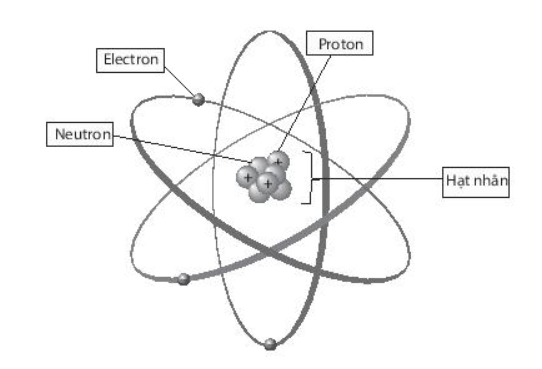
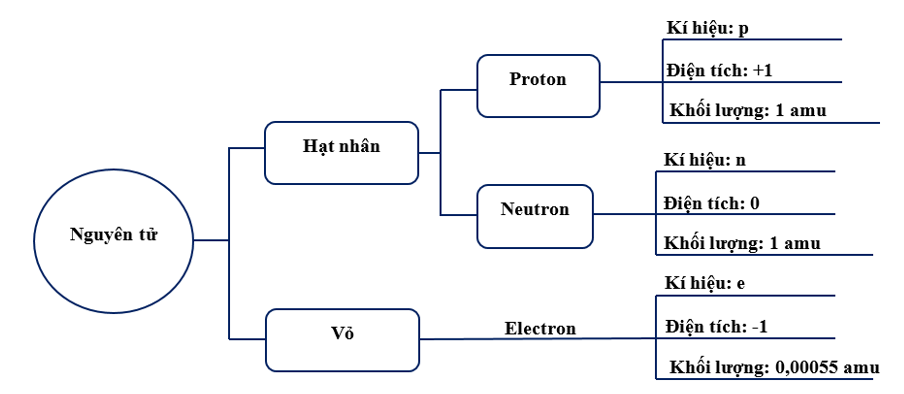
Chú thích cấu tạo nguyên tử trong hình sau:
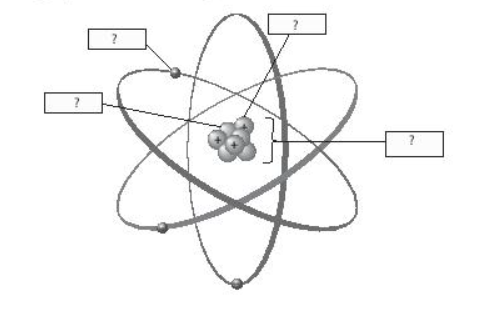

- Nguyên tử có hạt nhân ở tâm mang điện tích dương, các electron mang điện tích âm, chuyển động xung quanh hạt nhân như các hành tinh quay xung quanh Mặt Trời.
- Các electron chuyển động xung quanh hạt nhân theo từng lớp khác nhau.
+ Lớp electron trong cùng (gần hạt nhân nhất) chứa tối đa 2 electron và bị hạt nhân hút mạnh nhất.
+ Lớp thứ hai chứa tối đa 8 electron.
+ Các electron được xếp theo thứ tự từ trong ra ngoài cho đến hết.

Advertisements (Quảng cáo)
2.7
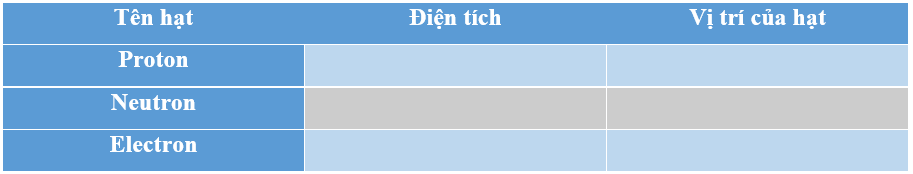
Hoàn thành bảng sau:



2.8
Điền từ thích hợp vào chỗ trống:
nguyên tử; neutron; electron; proton; lớp vỏ electron; hạt nhân
a) Thành phần chính tạo nên mọi vật chất được gọi là ..(1).. Nguyên tử được tạo nên từ ..(2).. và ..(3)…
b) ..(4).. nằm ở trung tâm nguyên tử. Hạt nhân được tạo bởi ..(5).. và ..(6)…
c) Các hạt mang điện tích dương trong hạt nhân nguyên tử được gọi là ..(7).. và các hạt không mang điện tích gọi là ..(8)..
d) ..(9).. chuyển động quanh hạt nhân nguyên tử.

- Nguyên tử có hạt nhân ở tâm mang điện tích dương, các electron mang điện tích âm, chuyển động xung quanh hạt nhân như các hành tinh quay xung quanh Mặt Trời.
- Các electron chuyển động xung quanh hạt nhân theo từng lớp khác nhau.

a) Thành phần chính tạo nên mọi vật chất được gọi là (1) nguyên tử. Nguyên tử được tạo nên từ (2) hạt nhân và (3) lớp vỏ electron.
b) (4) Hạt nhân nằm ở trung tâm nguyên tử. Hạt nhân được tạo bởi (5) proton và (6) neutron.
c) Các hạt mang điện tích dương trong hạt nhân nguyên tử được gọi là (7) proton và các hạt không mang điện tích gọi là (8) neutron.
d) (9) electron chuyển động quanh hạt nhân nguyên tử.
2.9
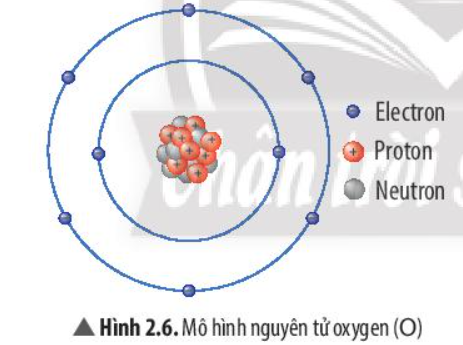
Quan sát hình dưới đây và trả lời các câu hỏi sau:
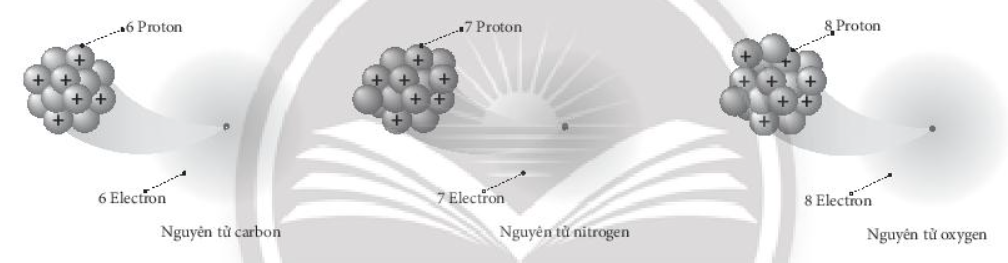
a) Số hạt proton trong các nguyên tử có trong hình trên là bao nhiêu hạt?
b) Các nguyên tử khác nhau sẽ có số hạt nào khác nhau?
c) Vì sao mỗi nguyên tử không mang điện?

- Nguyên tử gồm hạt nhân và vỏ electron
+ Hạt nhân gồm các hạt proton (mang điện tích dương) và neutron (không mang điện).
+ Vỏ electron gồm các hạt electron (mang điện tích âm).
- Các electron chuyển động xung quanh hạt nhân theo từng lớp khác nhau:
+ Lớp electron trong cùng (gần hạt nhân nhất) chứa tối đa 2 electron.
+ Lớp electron thứ hai chứa tối đa 8 electron.
- Nguyên tử trung hòa về điện nên tổng số hạt proton bằng tổng số hạt electron.

a)
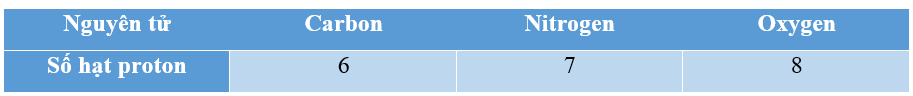
b) Các nguyên tử khác nhau có số hạt proton khác nhau.
c)
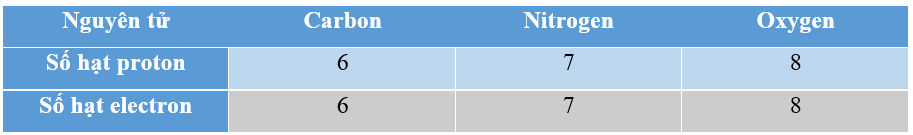
Trong nguyên tử, số hạt proton mang điện tích dương luôn bằng số hạt electron mang điện tích âm. Do đó, nguyên tử luôn trung hòa về điện (không mang điện).
2.10
Hoàn thành bảng sau:
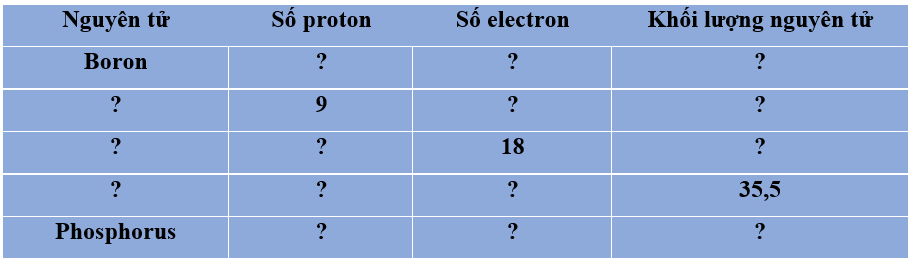

- Nguyên tử gồm hạt nhân và vỏ electron
+ Hạt nhân gồm các hạt proton (mang điện tích dương) và neutron (không mang điện).
+ Vỏ electron gồm các hạt electron (mang điện tích âm).
- Nguyên tử trung hòa về điện nên tổng số hạt proton bằng tổng số hạt electron.
- Khối lượng hạt nhân lớn hơn rất nhiều so với khối lượng vỏ electron nên có thể coi khối lượng nguyên tử tập trung ở hạt nhân.
+ Đơn vị khối lượng nguyên tử (atomic mass unit).
+ Viết tắt: amu.

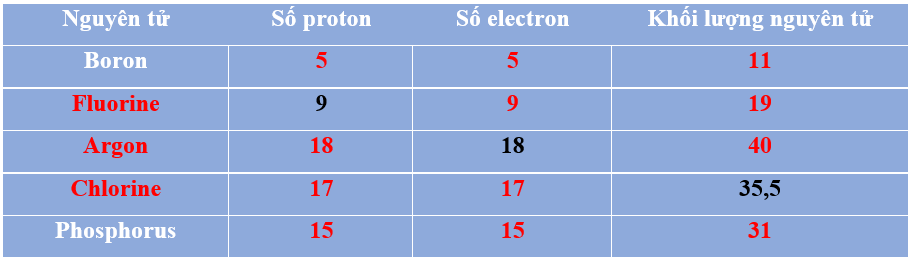
Số hiệu nguyên tử bằng số proton.
- Nguyên tử Boron có 5 proton. Khối lượng nguyên tử của boron bằng 11 amu.
⇨ p = e = 5.
- Nguyên tử Fluorine có 9 proton, khối lượng nguyên tử bằng 19 amu.
⇨ e = p = 9.
- e = p = 18 ⇨ Nguyên tử Argon ⇨ Khối lượng nguyên tử bằng 40 amu.
- Nguyên tử Chlorine có17 proton, khối lượng nguyên tử bằng 35,5 amu.
⇨ p = e = 17.
- Nguyên tử Phosphorus có 15 proton, khối lượng nguyên tử bằng 31 amu.
⇨ p = e = 15.
2.11
Em hãy tìm hiểu trên Internet hoặc sách, báo, tài liệu,.. về lịch sử tìm ra nguyên tử. Viết một đoạn văn ngắn khoảng 200 từ để tóm tắt những đóng góp của các nhà khoa học cho việc tìm ra nguyên tử.

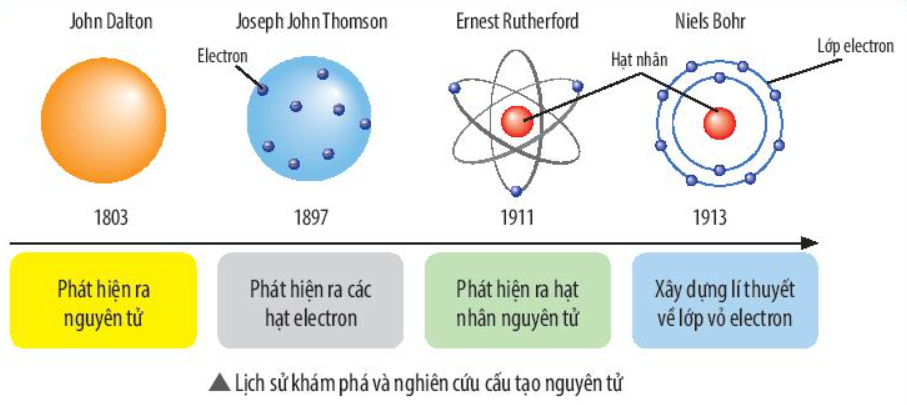

Vào năm 1803, nhà khoa học người Anh – John Dalton tiến hành thì nghiệm và nhận thấy rằng các chất tác dụng với nhau theo lượng xác định. Điều này chứng tỏ có các đơn vị chất tối thiểu (gọi là nguyên tử) để chúng kết hợp vừa đủ với nhau. Bằng các thí nghiệm vật lí, nhà vật lý người Anh - Josep John Thomson đã xác định được electron – một thành phần tạo nên nguyên tử và mang điện tích âm vào năm 1897. Ernest Rutherford – nhà vật lý người New Zealand đã xác định được nguyên tử có cấu tạo rỗng và có hạt nhân ở tâm qua thí nghiệm bắn phá lá vàng. Bằng cách bắn phá các hạt nhân nguyên tử Rutherford tìm ra được hạt proton mang điện tích dương. Năm 1911, Rutherford đề xuất mô hình hạt nhân nguyên tử như sau: nguyên tử có cấu tạo rỗng, có hạt nhân ở tâm mang điện tích dương và các electron mang điện tích âm chuyển động quanh hạt nhân như các hành tinh quay xung quanh mặt trời. Năm 1913, Niels Bohr – nhà vật lý người Đan Mạch – đã hoàn thiện mô hình nguyên tử của Rutherford, theo ông các electron chuyển động xung quanh hạt nhân theo từng lớp khác nhau. Lớp electron trong cùng chứa tối đa 2 electron và bị hạt nhân hút mạnh nhất, các lớp electron khác chứa tối đa 8 electron hoặc nhiều hơn và bị hạt nhân hút yếu hơn. Vào năm 1932, James Chadwick (nhà vật lý người Anh) đã tìm ra hạt neutron không mang điện trong hạt nhân nguyên tử.
2.12
Vì sao trong tự nhiên chỉ có 98 loại nguyên tử nhưng lại có hàng triệu chất khác nhau?

Trong tự nhiên, các chất được tạo thành bởi sự hình thành liên kết hóa học giữa các nguyên tử.

Trong tự nhiên có 98 nguyên tử, các nguyên tử này tạo liên kết hóa học với nhau để tạo thành chất, các chất có thể phản ứng với nhau để tạo thành chất khác, do đó trong tự nhiên có hàng triệu chất khác nhau.
