4.1
Nhà khoa học nổi tiếng người Nga đã có công trong việc xây dựng bảng tuần hoàn sử dụng đến ngày nay là
A. Dimitri. I. Mendeleev.
B. Ernest Rutherford.
C. Niels Bohr.
D. John Dalton.

Năm 1869, D. I. Mendeleev – nhà bác học người Nga xây dựng bảng tuần hoàn các nguyên tố hóa học theo chiều tăng dần khối lượng nguyên tử.

Nhà khoa học nổi tiếng người Nga đã có công trong việc xây dựng bảng tuần hoàn sử dụng đến ngày nay là Dimitri. I. Mendeleev.
⇨ Chọn A.
4.2
Hiện nay có bao nhiêu chu kì trong bảng tuần hoàn các nguyên tố hóa học?
A. 5.
B. 7.
C. 8.
D. 9.

- Các nguyên tố hóa học có cùng số lớp electron trong nguyên tử được sắp xếp vào cùng một hàng ngang trong bảng tuần hoàn. gọi là chu kì.
+ Hiện bảng tuần hoàn có 7 chu kì, đánh số từ 1 đến 7.
+ Chu kì 1, 2, 3 gọi là chu kì nhỏ.
+ Chu kì 4, 5, 6 gọi là chu kì lớn.
+ Số thứ tự của chu kì bằng số lớp electron của nguyên tử các nguyên tố trong chu kì đó.

Hiện nay có 7 chu kì trong bảng tuần hoàn các nguyên tố hóa học.
⇨ Chọn B.
4.3
Các nguyên tố trong bảng tuần hoàn các nguyên tố hóa học được sắp xếp theo thứ tự tăng dần của
A. khối lượng.
B. số proton.
C. tỉ trọng.
D. số neutron.

- Nguyên tử gồm hạt nhân và vỏ electron
+ Hạt nhân gồm các hạt proton (mang điện tích dương) và neutron (không mang điện).
⇨ Điện tích hạt nhân bằng số proton trong hạt nhân.
+ Vỏ electron gồm các hạt electron (mang điện tích âm).

Các nguyên tố trong bảng tuần hoàn các nguyên tố hóa học được sắp xếp theo thứ tự tăng dần của điện tích hạt nhân (số proton).
⇨ Chọn B.
4.4
Nguyên tố phi kim không thuộc nhóm nào sau đây trong bảng tuần hoàn các nguyên tố hóa học?
A. Nhóm IA.
B. Nhóm IVA.
C. Nhóm IIA.
D. Nhóm VIIA.

Các nguyên tố phi kim gồm:
+ Nguyên tố hydrogen ở nhóm IA.
+ Một số nguyên tố nhóm IIIA và IVA.
+ Hầu hết các nguyên tố thuộc nhóm VA, VIA, VIIA.
⇨ Nguyên tố phi kim không thuộc nhóm IIA trong bảng tuần hoàn các nguyên tố hóa học.
⇨Chọn C.
4.5
Số hiệu nguyên tử của một nguyên tố là
A. số proton trong nguyên tử.
B. số neutron trong nguyên tử.
C. số electron trong hạt nhân.
D. số proton và neutron trong hạt nhân.

Số hiệu nguyên tử của một nguyên tố là số proton trong nguyên tử.
⇨ Chọn A.
* Lưu ý: không chọn phát biểu C (số electron trong hạt nhân) vì electron nằm ở vỏ electron của nguyên tử.
4.6
Vị trí kim loại kiềm trong bảng tuần hoàn các nguyên tố hóa học thường
A. ở đầu nhóm.
B. ở cuối nhóm.
C. ở đầu chu kì.
D. ở cuối chu kì.

Kim loại nhóm IA (trừ hydrogen) được gọi là kim loại kiềm.
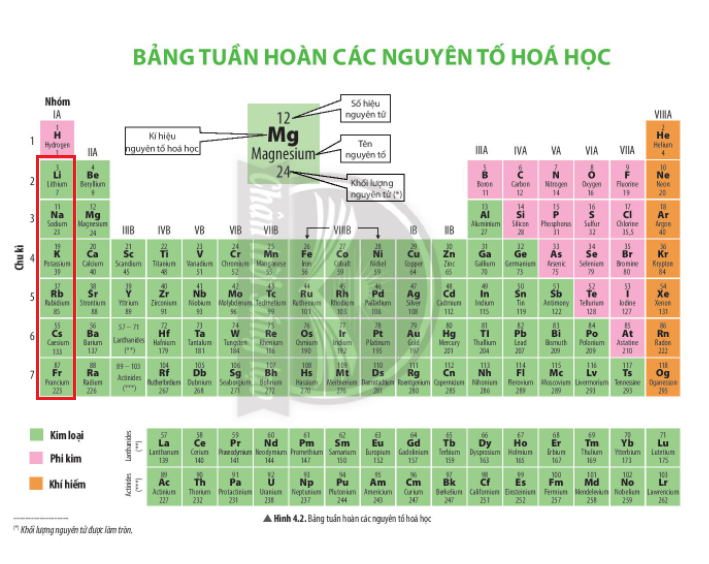 ⇨ Vị trí kim loại kiềm trong bảng tuần hoàn các nguyên tố hóa học thường ở đầu chu kì.
⇨ Vị trí kim loại kiềm trong bảng tuần hoàn các nguyên tố hóa học thường ở đầu chu kì.
⇨ Chọn C.
4.7
Trong ô nguyên tố sau, con số 23 cho biết điều gì?

A. Khối lượng nguyên tử của nguyên tố.
B. Chu kì của nó.
C. Số nguyên tử của nguyên tố.
D. Số thứ tự của nguyên tố.

- Số hiệu nguyên tử là số thứ tự của nguyên tố trong bảng tuần hoàn.
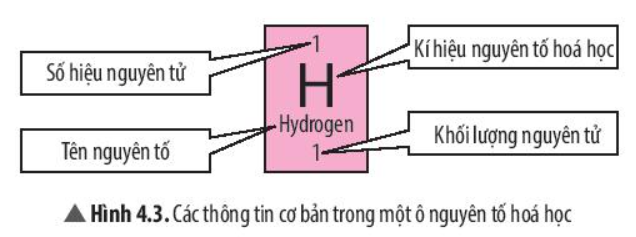

Trong ô nguyên tố sau, con số 23 cho biết khối lượng nguyên tử.
⇨ Chọn A.
4.8
Tên gọi của các cột trong bảng tuần hoàn các nguyên tố hóa học là gì?
A. Chu kì.
B. Nhóm.
C. Loại.
D. Họ.

* Nhóm là tập hợp các nguyên tố hóa học theo cột dọc, có tính chất hóa học tương tự nhau và sắp xếp theo chiều tăng dần của điện tích hạt nhân.
- Trong cùng một nhóm, khi đi từ trên xuống dưới, điện tích hạt nhân nguyên tử của các nguyên tố tăng dần.
- Số thứ tự của nhóm A bằng số electron ở lớp ngoài cùng của nguyên tử các nguyên tố trong nhóm đó.


Tên gọi của các cột trong bảng tuần hoàn các nguyên tố hóa học là nhóm.
⇨ Chọn B.
4.9
Phần lớn các nguyên tố hóa học trong bảng tuần hoàn là
A. kim loại.
B. phi kim.
C. khí hiếm.
D. chất khí.

Phần lớn các nguyên tố hóa học trong bảng tuần hoàn là kim loại (gần 80% tổng số nguyên tố trong bảng tuần hoàn).
⇨ Chọn A.
4.10
Các kim loại kiềm trong nhóm IA đều có số electron lớp ngoài cùng là bao nhiêu?
A. 1.
B. 2.
C. 3.
D. 7.

- Nhóm là tập hợp các nguyên tố hóa học theo cột dọc, có tính chất hóa học tương tự nhau và sắp xếp theo chiều tăng dần của điện tích hạt nhân.
- Trong cùng một nhóm, khi đi từ trên xuống dưới, điện tích hạt nhân nguyên tử của các nguyên tố tăng dần.
- Số thứ tự của nhóm A bằng số electron ở lớp ngoài cùng của nguyên tử các nguyên tố trong nhóm đó.

Vì số thứ tự của nhóm A bằng số electron ở lớp ngoài cùng của nguyên tử các nguyên tố nên Các kim loại kiềm trong nhóm IA đều có số electron lớp ngoài cùng là 1.
⇨ Chọn A.
4.11
Những nguyên tố nào sau đây thuộc nhóm VIIA (Halogen)
A. Chlorine, bromine, fluorine.
B. Fluorine, carbon, bromine.
C. Berryllium, carbon, oxygen.
D. Neon, helium, argon.

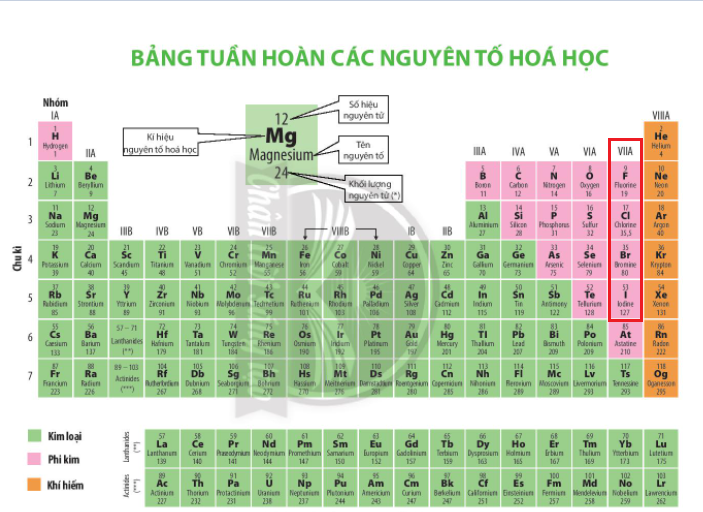

Những nguyên tố thuộc nhóm VIIA là fluorine, chlorine, bromine, iodine.
⇨ Chọn A.
4.12
Nguyên tố nào được sử dụng trong thuốc tẩy gia dụng?
A. Iodine.
B. Bromine.
C. Chlorine.
D. Fluorine.

Nguyên tố chlorine (Cl) được sử dụng trong thuốc tẩy gia dụng.
⇨ Chọn C.
4.13
Các nguyên tố hóa học nhóm IIA có điểm gì chung?
A. Có cùng số nguyên tử.
Advertisements (Quảng cáo)
B. Có cùng khối lượng.
C. Tính chất hóa học tương tự nhau.
D. Không có điểm chung.

- Nhóm là tập hợp các nguyên tố hóa học theo cột dọc, có tính chất hóa học tương tự nhau và sắp xếp theo chiều tăng dần của điện tích hạt nhân.

Các nguyên tố trong cùng một nhóm có tính chất hóa học tương tự nhau.
⇨ Các nguyên tố hóa học nhóm IIA có tính chất hóa học tương tự nhau.
⇨ Chọn C.
4.14
Lý do những nguyên tố hóa học trong IA không thể tìm thấy trong tự nhiên:
A. Vì chúng là những kim loại không hoạt động.
B. Vì chúng là những kim loại hoạt động.
C. Vì chúng do con người tạo ra.
D. Vì chúng là kim loại kém hoạt động.

Các kim loại kiềm trong nhóm I là những kim loại hoạt động mạnh, do đó chúng không tồn tại ở dạng đơn chất trong tự nhiên.
⇨ Chọn B.
4.15
Quan sát hình bên, hãy chỉ ra nguyên tố nào là phi kim?
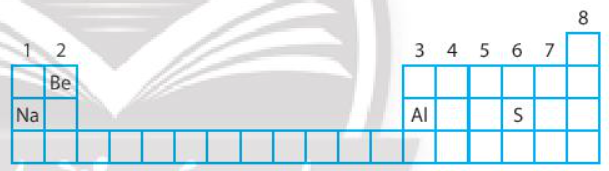
A. Na.
B. S.
C. Al.
D. Be.

- Na, Be, Al là kim loại.
- S là phi kim.
⇨ Chọn B.
4.16
Cho biết kim loại nào có thể cắt bằng dao?
A. Magnesium.
B. Iron.
C. Mercury.
D. Sodium.

Kim loại kiềm là mềm, có thể dùng dao cắt được.
Sodium (Na) là kim loại nhóm IA (kim loại kiềm).
⇨ Chọn D.
4.17
Nguyên tố nào được sử dụng trong việc chế tạo con chíp trong máy tính?
A. Neon.
B. Chlorine.
C. Silver.
D. Silicon.

Nguyên tố được sử dụng trong việc chế tạo con chíp trong máy tính là silicon (Si).
⇨ Chọn D.
4.18
Nguyên tố phi kim nào tồn tại ở dạng lỏng ở nhiệt độ phòng?
A. Nitrogen.
B. Bromine.
C. Argon.
D. Mercury.

- Trong điều kiện thường, phi kim tồn tại dưới cả ba trạng thái:
+ Rắn: C, P, S, …
+ Lỏng: Br2, …
+ Khí: O2, H2, Cl2, N2,…

Nguyên tố bromine (Br) tồn tại ở dạng lỏng ở nhiệt độ phòng.
⇨ Chọn B.
4.19
Hãy cho biết tên gọi của nhóm nguyên tố được tô màu trong bảng tuần hoàn dưới đây.
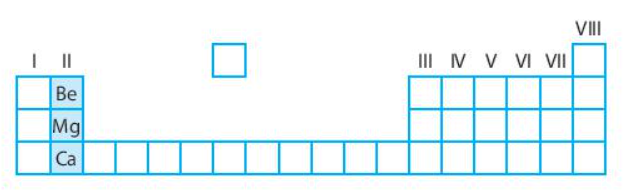
A. Kim loại kiềm.
B. Kim loại kiềm thổ.
C. Kim loại chuyển tiếp.
D. Halogen.

Nhóm IA (trừ hydrogen): Kim loại kiềm.
Nhóm IIA: Kim loại kiềm thổ.
Nhóm IIIA (trừ nguyên tố boron).

Kim loại nhóm IIA còn được gọi là kim loại kiềm thổ.
⇨ Chọn B.
4.20
Quan sát ô nguyên tố và trả lời các câu hỏi sau:

a) Em biết được thông tin gì trong ô nguyên tố calcium?
b) Nguyên tố calcium này nằm ở vị trí nào (ô, nhóm, chu kì) trong bảng tuần hoàn các nguyên tố hóa học?
c) Tên gọi của nhóm chứa nguyên tố này là gì?
d) Calcium có cần thiết cho cơ thể chúng ta không? Lấy ví dụ minh họa.

a) Từ ô nguyên tố của calcium, ta biết được:
+ Số thứ tự của ô: 20.
+ Kí hiệu nguyên tố: Ca.
+ Tên nguyên tố: calcium.
+ Khối lượng nguyên tử: 40.
b) Vị trí của nguyên tố calcium:
+ Ô: 20.
+ Nhóm: IIA.
+ Chu kì: 3.
c) Calcium thuộc nhóm IIA – nhóm kim loại kiềm thổ.
d) Calcium là nguyên tố rất cần thiết cho cơ thể vì:
+ calcium giúp xương chắc khỏe.
+ phòng ngừa bệnh loãng xương.
+ phát triển chiều cao.
+ là chất cần thiết trong hoạt động của tim,…
4.21
Quan sát ô nguyên tố sau:
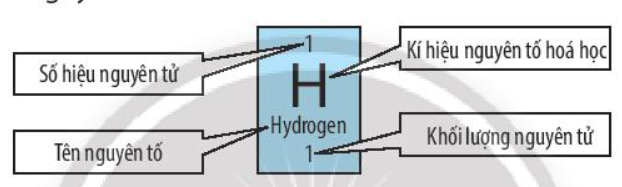
Bổ sung các thông tin còn thiếu trong các ô nguyên tố sau:
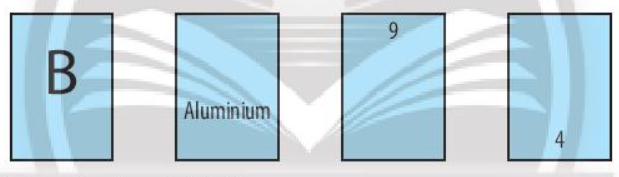

- Mỗi nguyên tố hóa học được sắp xếp vào một ô của bảng tuần hoàn, gọi là ô nguyên tố.
- Ô nguyên tố cho biết: kí hiệu hóa học, tên nguyên tố, số hiệu nguyên tử và khối lượng nguyên tử của nguyên tố đó.
- Số hiệu nguyên tử = Số đơn vị điện tích hạt nhân (số proton trong hạt nhân) = Số electron trong nguyên tử.
- Số hiệu nguyên tử là số thứ tự của nguyên tố trong bảng tuần hoàn.
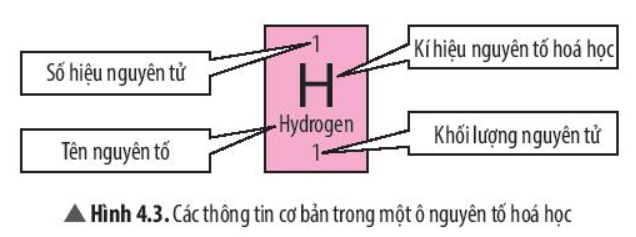

Dựa vào bảng tuần hoàn các nguyên tố hóa học để điền các thông tin còn thiếu trong ô nguyên tố.

4.22
Điền từ thích hợp vào chỗ trống:
Kim loại; phi kim; khí hiếm;
Phần lớn các nguyên tố (1) nằm phía bên trái của bảng tuần hoàn và các nguyên tố (2) được xếp phía bên phải của bảng tuần hoàn. Các nguyên tố (3) nằm ở cột cuối cùng của bảng tuần hoàn các nguyên tố hóa học.

Phần lớn các nguyên tố (1) kim loại nằm phía bên trái của bảng tuần hoàn và các nguyên tố (2) phi kim được xếp phía bên phải của bảng tuần hoàn. Các nguyên tố (3) khí hiếm nằm ở cột cuối cùng của bảng tuần hoàn các nguyên tố hóa học.
4.23
Cho các nguyên tố hóa học sau: H, Mg, B, Na, S, O, Ne, He, Al.
a) Những nguyên tố nào thuộc cùng một nhóm?
b) Những nguyên tố nào thuộc cùng một chu kì?
c) Những nguyên tố nào là kim loại? Phi kim? Khí hiếm?

a) Nhóm IA: H, Na.
Nhóm IIA: Mg.
Nhóm IIIA: B, Al.
Nhóm VA: P.
Nhóm VIA: O, S.
Nhóm VIIIA: Ne, He.
b) Chu kì 1: H, He.
Chu kì 2: B, O, Ne.
Chu kì 3: Na, Mg, Al, P, S.
c) Kim loại: Na, Mg, Al.
Phi kim: H, B, O, P, S.
Khí hiếm: Ne, He.
4.24
Không chỉ riêng nhà khoa học Mendeleev thành công trong việc xây dựng bảng tuần hoàn các nguyên tố hóa học, hiện nay cũng có nhiều bảng tuần hoàn được trình bày rất phong phú và đa dạng. Sử dụng Internet ha sách báo, tạp chí, em hãy tìm, sưu tầm hay thiết kế bảng tuần hoàn các nguyên tố hóa học theo ý tưởng của mình sao cho trình bày độc đáo, mới lạ và giới thiệu cho cả lớp cùng xem.

Năm 1869, D. I. Mendeleev – nhà bác học người Nga xây dựng bảng tuần hoàn các nguyên tố hóa học theo chiều tăng dần khối lượng nguyên tử.


Có thể thiết kế bảng tuần hoàn các nguyên tố hóa học theo những mẫu sau:

