7.1
Đơn chất nitơ bao gồm các phân tử chứa hai nguyên tử nitơ. Công thức hóa học của đơn chất nitơ là
A. N.
B. N2.
C. N2.
D. N2.

Công thức hóa học bao gồm kí hiệu hóa học của nguyên tố và chỉ số biểu diễn số nguyên tử. Chỉ số nằm ở chân bên phải của kí hiệu hóa học.
Phân tử khí nitrogen có hai nguyên tử nitrogen, kí hiệu hóa học của nguyên tố nitrogen là N.
⇨ Công thức hóa học của khí nitrogen là: N2.
⇨ Chọn C.
7.2
Một phân tử của hợp chất carbon dioxide chứa một nguyên tử carbon và hai nguyên tử oxygen. Công thức hóa học của hợp chất carbon dioxide là
A. CO2.
B. CO2.
C. CO2.
D. Co2.

+ Công thức hóa học của hợp chất gồm kí hiệu hóa học của những nguyên tố tạo nên hợp chất kèm theo chỉ số ở chân bên phải của kí hiệu hóa học. Chỉ số là những số nguyên, cho biết số nguyên tử của mỗi nguyên tố trong phân tử hợp chất. Chỉ số bằng 1 thì không ghi.

Công thức hóa học bao gồm kí hiệu hóa học của nguyên tố và chỉ số biểu diễn số nguyên tử. Chỉ số nằm ở chân bên phải của kí hiệu hóa học.
Phân tử của hợp chất carbon dioxide chứa một nguyên tử carbon và hai nguyên tử oxygen.
Kí hiệu hóa học của nguyên tử nguyên tố carbon và oxygen lần lượt là C và O.
⇨ Công thức hóa học của khí carbon dioxide là: CO2.
⇨ Chọn A.
7.3
Công thức hóa học của sodium hydroxide là NaOH. Hợp chất này chứa những nguyên tố hóa học nào? Trong một phân tử sodium hydroxide có bao nhiêu nguyên tử của mỗi nguyên tố đó?

- Công thức hóa học của một chất là cách biểu diễn chất bằng kí hiệu hóa học của nguyên tố kèm theo chỉ số ở chân bên phải kí hiệu hóa học.
- Chỉ số là những số nguyên, cho biết số nguyên tử của mỗi nguyên tố trong phân tử hợp chất. Chỉ số bằng 1 thì không ghi.

- Công thức hóa học của sodium hydroxide là NaOH.
- Hợp chất này chứa nguyên tố hóa học: sodium (Na), oxygen (O), hydrogen (H).
- Vì các chỉ số không được ghi dưới chân kí hiệu nguyên tố trong công thức hóa học NaOH nên trong một phân tử sodium hydroxide có:
+ 1 nguyên tử của nguyên tố sodium.
+ 1 nguyên tử của nguyên tố oxygen.
+ 1 nguyên tử của nguyên tố hydrogen.
7.4
Công thức của sulfuric acid là H2SO4.
a) Gọi tên các nguyên tố có trong sulfuric acid.
b) Có bao nhiêu nguyên tử của mỗi nguyên tố đó trong một phân tử sulfuric acid.

- Công thức hóa học của một chất là cách biểu diễn chất bằng kí hiệu hóa học của nguyên tố kèm theo chỉ số ở chân bên phải kí hiệu hóa học.
- Chỉ số là những số nguyên, cho biết số nguyên tử của mỗi nguyên tố trong phân tử hợp chất. Chỉ số bằng 1 thì không ghi.

a) Các nguyên tố trong sulfuric acid (H2SO4) là: hydrogen (H), sulfur (S), oxygen (O).
b) Trong một phân tử sulfuric acid (H2SO4) có:
+ 2 nguyên tử của nguyên tố hydrogen.
+ 1 nguyên tử của nguyên tố sulfur.
+ 4 nguyên tử của nguyên tố oxygen.
7.5
Hãy viết công thức hóa học của các hợp chất sau đây:
a) Magnesium oxide, biết một phân tử của nó chứa một nguyên tử magnesium và một nguyên tử oxygen.
b) Copper sulfate, biết một phân tử của nó chứa một nguyên tử đồng, một nguyên tử sulfur và bốn nguyên tử oxygen.
c) Đường ăn, biết một phân tử của nó chứa 12 nguyên tử carbon, 22 nguyên tử hydrogen và 11 nguyên tử oxygen.

Công thức hóa học bao gồm kí hiệu hóa học của nguyên tố và chỉ số biểu diễn số nguyên tử. Chỉ số nằm ở chân bên phải của kí hiệu hóa học

a) Phân tử magnesium oxide chứa một nguyên tử magnesium (Mg) và một nguyên tử oxygen (O).
⇨ Công thức hóa học của magnesium oxide là: MgO.
b) Phân tử copper sulfate chứa một nguyên tử đồng (Cu), một nguyên tử sulfur (S) và bốn nguyên tử oxygen (O).
⇨ Công thức hóa học của copper sulfate là: CuSO4.
c) Một phân tử đường ăn chứa 12 nguyên tử carbon (C), 22 nguyên tử hydrogen (H) và 11 nguyên tử oxygen (O).
⇨ Công thức hóa học của đường ăn là: C12H22O11.
7.6
Điền công thức hóa học và mô tả số lượng các nguyên tử của các nguyên tố vào chỗ trống để hoàn thiện bảng sau:

Công thức hóa học bao gồm kí hiệu hóa học của nguyên tố và chỉ số biểu diễn số nguyên tử. Chỉ số nằm ở chân bên phải của kí hiệu hóa học.
Để viết được công thức hóa học, cần phải nhớ được kí hiệu hóa học của nguyên tố.


7.7
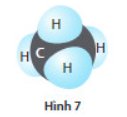
Hình 7 mô tả phân tử khí methane CH4.
a) Trong hợp chất này, nguyên tử C sử dụng bao nhiêu electron lớp ngoài cùng của nó để tạo liên kết cộng hóa trị với các nguyên tử H?
A. 2.
B. 4.
C. 8.
D. 10.
b) Cho biết mỗi một cặp electron dùng chung giữa các nguyên tử C và nguyên tử H tướng ứng với một liên kết cộng hóa trị, thì nguyên tử C tạo được bao nhiêu liên kết cộng hóa trị với các nguyên tử H?
A. 2.
B. 4.
C. 8.
D. 10.

- Số thứ tự của nhóm A bằng số electron ở lớp ngoài cùng của nguyên tử các nguyên tố (trừ helium) trong nhóm đó.
- Lớp electron ngoài cùng bền vững của khí hiếm là 8 electron (trừ helium). Nguyên tử của nguyên tố khác có xu hướng tham gia liên kết hóa học để đạt được lớp electron ngoài cùng giống khí hiếm gần nó nhất trong bảng tuần hoàn.
- Liên kết cộng hóa trị là liên kết được tạo nên giữa hai nguyên tử bằng một hay nhiều cặp electron dùng chung. Mỗi cặp electron dùng chung tạo nên một liên kết cộng hóa trị.

a) Nguyên tử carbon có 4 electron lớp ngoài cùng, để đạt được lớp electron bền vững giống khí hiếm, nguyên tử carbon cần thêm 4 electron và góp chung 4 electron để tạo liên kết cộng hóa trị.
⇨ Chọn B.
b) Mỗi nguyên tử hydrogen có 1 electron, để đạt được lớp electron ngoài cùng bền vững của khí hiếm gần hydrogen là khí helium có 2 electron, nguyên tử hydrogen cần thêm 1 electron và góp chung 1 electron của mình để tạo liên kết cộng hóa trị.
⇨ Nguyên tử carbon tạo 4 liên kết cộng hóa trị với 4 nguyên tử hydrogen.
⇨ Chọn B.
7.8
Hãy xác định hóa trị của các nguyên tố C, Si trong các hợp chất sau:
a) CCl4 biết trong hợp chất này Cl có hóa trị I.
b) SiO2, biết trong hợp chất này O có hóa trị II.

- Quy tắc hóa trị: Trong công thức hóa học của hợp chất hai nguyên tố, tích của chỉ số và hóa trị của nguyên tố này bằng tích của chỉ số và hóa trị của nguyên tố kia.
Ví dụ: \({\rm{P}}_{\rm{2}}^{\rm{V}}{\rm{O}}_{\rm{5}}^{{\rm{II}}}\), ta có: 2 . V = 5 . II.
- Quy ước:
+ Nguyên tố H luôn có hóa trị I.
⇨ Nguyên tử của nguyên tố khác liên kết với bao nhiêu H thì hóa trị bằng bấy nhiêu,
+ Nguyên tố O luôn có hóa trị II.

a) Gọi hóa trị của C cần tìm là A
Ta có công thức dạng chung: \({{\rm{C}}^{\rm{A}}}{\rm{Cl}}_{\rm{4}}^{\rm{I}}\)
Áp dụng quy tắc hóa trị:
\(\begin{array}{l}{\rm{A }}{\rm{. 1 = I }}{\rm{. 4}}\\ \Rightarrow {\rm{A = }}\frac{{{\rm{I }}{\rm{. 4}}}}{{\rm{1}}}{\rm{ = IV}}\end{array}\)
Vậy hóa trị của C trong hợp chất CCl4 có hóa trị IV.
b) Gọi hóa trị của Si cần tìm là A
Ta có công thức dạng chung: \({\rm{S}}{{\rm{i}}^{\rm{A}}}{\rm{O}}_{\rm{2}}^{{\rm{II}}}\)
Áp dụng quy tắc hóa trị:
\(\begin{array}{l}{\rm{A }}{\rm{. 1 = II }}{\rm{. 2}}\\ \Rightarrow {\rm{A = }}\frac{{{\rm{II }}{\rm{. 2}}}}{{\rm{1}}}{\rm{ = IV}}\end{array}\)
Vậy hóa trị của Si trong hợp chất SiO2 có hóa trị IV.
7.9
Hãy viết công thức hóa học và gọi tên của hợp chất được tạo thành từ sự kết hợp giữa các đơn chất sau:
a) sắt và chlorine, biết trong hợp chất này sắt hóa trị III và chlorine hóa trị I.
b) natri và oxygen, biết natri hóa trị I và oxygen hóa trị II.
c) hydrogen và fluorine, biết hydrogen hóa trị I và fluorine hóa trị I.
d) kali và chlorine, biết kali hóa trị I và chlorine hóa trị I.
e) calcium, carbon và oxygenm biết calcium hóa trị II và nhóm nguyên tử CO3 có hóa trị II.

- Quy tắc hóa trị: Trong công thức hóa học của hợp chất hai nguyên tố, tích của chỉ số và hóa trị của nguyên tố này bằng tích của chỉ số và hóa trị của nguyên tố kia.
Ví dụ: \({\rm{P}}_{\rm{2}}^{\rm{V}}{\rm{O}}_{\rm{5}}^{{\rm{II}}}\), ta có: 2 . V = 5 . II.
- Quy ước:
+ Nguyên tố H luôn có hóa trị I.
⇨ Nguyên tử của nguyên tố khác liên kết với bao nhiêu H thì hóa trị bằng bấy nhiêu,
+ Nguyên tố O luôn có hóa trị II.

Kí hiệu hóa học của nguyên tố:
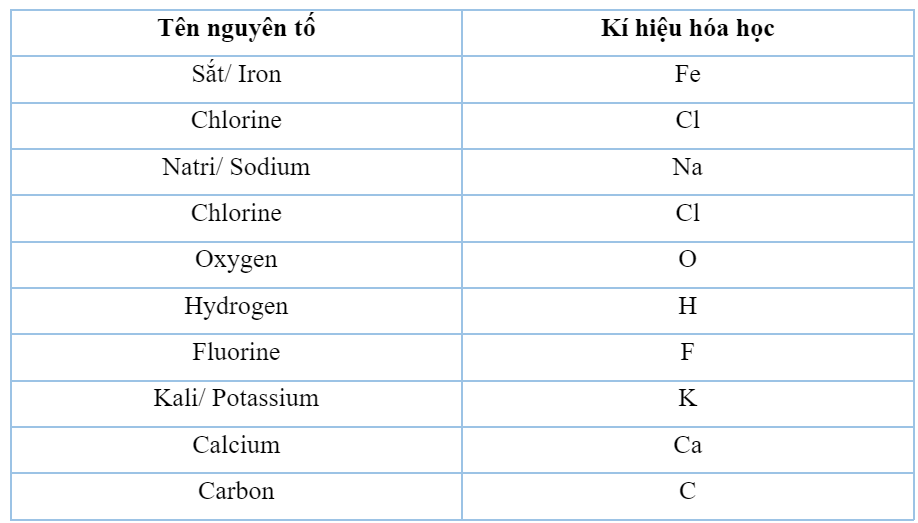 a) Ta có công thức dạng chung của sắt và chlorine: \({\rm{Fe}}_{\rm{x}}^{{\rm{III}}}{\rm{Cl}}_{\rm{y}}^{\rm{I}}\)
a) Ta có công thức dạng chung của sắt và chlorine: \({\rm{Fe}}_{\rm{x}}^{{\rm{III}}}{\rm{Cl}}_{\rm{y}}^{\rm{I}}\)
Áp dụng quy tắc hóa trị, ta có: x . III = y . I
\( \Rightarrow \frac{{\rm{x}}}{{\rm{y}}}{\rm{ = }}\frac{{\rm{I}}}{{{\rm{III}}}}{\rm{ = }}\frac{{\rm{1}}}{{\rm{3}}}\)
⇨ Chọn x = 1; y = 3.
⇨ Công thức hóa học cần tìm là FeCl3.
b) Ta có công thức dạng chung của sodium và oxygen là \({\rm{Na}}_{\rm{x}}^{\rm{I}}{\rm{O}}_{\rm{y}}^{{\rm{II}}}\)
Áp dụng quy tắc hóa trị: x . I = y . II
\( \Rightarrow \frac{{\rm{x}}}{{\rm{y}}}{\rm{ = }}\frac{{{\rm{II}}}}{{\rm{I}}}{\rm{ = }}\frac{{\rm{2}}}{{\rm{1}}}\)
⇨ Chọn x = 2; y = 1.
⇨ Công thức hóa học cần tìm là Na2O.
c) Ta có công thức hóa học dạng chung của hydrogen và fluorine là \({\rm{H}}_{\rm{x}}^{\rm{I}}{\rm{F}}_{\rm{y}}^{\rm{I}}\)
Áp dụng quy tắc hóa trị: x . I = y . I
\( \Rightarrow \frac{{\rm{x}}}{{\rm{y}}}{\rm{ = }}\frac{{\rm{I}}}{{\rm{I}}}{\rm{ = }}\frac{1}{{\rm{1}}}\)
⇨ Chọn x = 1; y = 1.
⇨ Công thức hóa học cần tìm là HF.
d) Ta có công thức hóa học dạng chung của potassium và chlorine là \({\rm{K}}_{\rm{x}}^{\rm{I}}{\rm{Cl}}_{\rm{y}}^{\rm{I}}\)
Áp dụng quy tắc hóa trị: x . I = y . I
\( \Rightarrow \frac{{\rm{x}}}{{\rm{y}}}{\rm{ = }}\frac{{\rm{I}}}{{\rm{I}}}{\rm{ = }}\frac{1}{{\rm{1}}}\)
⇨ Chọn x = 1; y = 1.
⇨ Công thức hóa học cần tìm là KCl.
e) Ta có công thức hóa học dạng chung của calcium và nhóm nguyên tử CO3 là \({\rm{Ca}}_{\rm{x}}^{{\rm{II}}}{\rm{(C}}{{\rm{O}}_3})_{\rm{y}}^{{\rm{II}}}\)
Áp dụng quy tắc hóa trị: x . II = y . II
\( \Rightarrow \frac{{\rm{x}}}{{\rm{y}}}{\rm{ = }}\frac{{{\rm{II}}}}{{{\rm{II}}}}{\rm{ = }}\frac{{\rm{2}}}{{\rm{2}}}{\rm{ = }}\frac{{\rm{1}}}{{\rm{1}}}\)
⇨ Chọn x = 1; y = 1.
⇨ Công thức hóa học cần tìm là CaCO3.
7.10
Sử dụng thông tin trong Bảng hóa trị thường gặp của một số nguyên tố hóa học (Bảng 7.2 trang 43 SGK), hãy viết công thức hóa học của:
a) copper (I) oxide, (hợp chất hai nguyên tố giữa Cu và O, trong đó Cu hóa trị I).
b) zinc phosphate (hợp chất chứa Zn liên kết với nhóm nguyên tử PO4).
c) calcium carbonate (hợp chất chứa Ca liên kết với nhóm nguyên tử CO3).
d) sodium hydroxide (hợp chất chứa Na liên kết với nhóm nguyên tử OH).

- Quy tắc hóa trị: Trong công thức hóa học của hợp chất hai nguyên tố, tích của chỉ số và hóa trị của nguyên tố này bằng tích của chỉ số và hóa trị của nguyên tố kia.
Ví dụ: \({\rm{P}}_{\rm{2}}^{\rm{V}}{\rm{O}}_{\rm{5}}^{{\rm{II}}}\), ta có: 2 . V = 5 . II.
- Quy ước:
+ Nguyên tố H luôn có hóa trị I.
⇨ Nguyên tử của nguyên tố khác liên kết với bao nhiêu H thì hóa trị bằng bấy nhiêu,
+ Nguyên tố O luôn có hóa trị II.

a) Ta có công thức hóa học dạng chung của copper (I) oxide là \({\rm{Cu}}_{\rm{x}}^{\rm{I}}{\rm{O}}_{\rm{y}}^{{\rm{II}}}\)
Áp dụng quy tắc hóa trị: x . I = y . II
\( \Rightarrow \frac{{\rm{x}}}{{\rm{y}}}{\rm{ = }}\frac{{{\rm{II}}}}{{\rm{I}}}{\rm{ = }}\frac{{\rm{2}}}{{\rm{1}}}\)
⇨ Chọn x = 2; y = 1.
⇨ Công thức hóa học cần tìm là Cu2O.
b) Ta có công thức hóa học dạng chung của zinc phosphate là \({\rm{Zn}}_{\rm{x}}^{{\rm{II}}}{\rm{(P}}{{\rm{O}}_4})_{\rm{y}}^{{\rm{III}}}\)
Áp dụng quy tắc hóa trị: x . II = y . III
\( \Rightarrow \frac{{\rm{x}}}{{\rm{y}}}{\rm{ = }}\frac{{{\rm{III}}}}{{{\rm{II}}}}{\rm{ = }}\frac{3}{2}\)
⇨ Chọn x = 3; y = 2.
⇨ Công thức hóa học cần tìm là Zn3(PO4)2.
c) Ta có công thức hóa học dạng chung của calcium carbonate là \({\rm{Ca}}_{\rm{x}}^{{\rm{II}}}{\rm{(C}}{{\rm{O}}_3})_{\rm{y}}^{{\rm{II}}}\)
Áp dụng quy tắc hóa trị: x . II = y . II
\( \Rightarrow \frac{{\rm{x}}}{{\rm{y}}}{\rm{ = }}\frac{{{\rm{II}}}}{{{\rm{II}}}}{\rm{ = }}\frac{{\rm{2}}}{{\rm{2}}}{\rm{ = }}\frac{{\rm{1}}}{{\rm{1}}}\)
⇨ Chọn x = 1; y = 1.
⇨ Công thức hóa học cần tìm là CaCO3.
d) Ta có công thức hóa học dạng chung của sodium hydroxide là \({\rm{Na}}_{\rm{x}}^{\rm{I}}{\rm{(OH)}}_{\rm{y}}^{\rm{I}}\)
Áp dụng quy tắc hóa trị: x . I = y . I
\( \Rightarrow \frac{{\rm{x}}}{{\rm{y}}}{\rm{ = }}\frac{{\rm{I}}}{{\rm{I}}}{\rm{ = }}\frac{1}{{\rm{1}}}\)
⇨ Chọn x = 1; y = 1.
⇨ Công thức hóa học cần tìm là NaOH.
7.11
Hãy tính hóa trị của đồng và sắt trong các hợp chất sau: Cu(OH)2, Fe(NO3)3.
(Biết hóa trị của nhóm OH là I và của nhóm NO3 là I).

- Quy tắc hóa trị: Trong công thức hóa học của hợp chất hai nguyên tố, tích của chỉ số và hóa trị của nguyên tố này bằng tích của chỉ số và hóa trị của nguyên tố kia.
Ví dụ: \({\rm{P}}_{\rm{2}}^{\rm{V}}{\rm{O}}_{\rm{5}}^{{\rm{II}}}\), ta có: 2 . V = 5 . II.
- Quy ước:
+ Nguyên tố H luôn có hóa trị I.
⇨ Nguyên tử của nguyên tố khác liên kết với bao nhiêu H thì hóa trị bằng bấy nhiêu,
Advertisements (Quảng cáo)
+ Nguyên tố O luôn có hóa trị II.

* Cu(OH)2
Gọi hóa trị của Cu cần tìm là A
Ta có công thức dạng chung: \({\rm{Cu}}_{\rm{1}}^{\rm{A}}{\rm{(OH)}}_{\rm{2}}^{\rm{I}}\)
Áp dụng quy tắc hóa trị:
\(\begin{array}{l}{\rm{A }}{\rm{. 1 = I }}{\rm{. 2}}\\ \Rightarrow {\rm{A = }}\frac{{{\rm{I }}{\rm{. 2}}}}{{\rm{1}}}{\rm{ = II}}\end{array}\)
Vậy hóa trị của Cu trong hợp chất trên có hóa trị II.
* Fe(NO3)3
Ta có công thức dạng chung: \({\rm{Fe}}_{\rm{1}}^{\rm{A}}{\rm{(N}}{{\rm{O}}_{\rm{3}}}{\rm{)}}_{\rm{3}}^{\rm{I}}\)
Áp dụng quy tắc hóa trị:
\(\begin{array}{l}{\rm{A }}{\rm{. 1 = I }}{\rm{. 3}}\\ \Rightarrow {\rm{A = }}\frac{{{\rm{I }}{\rm{. 3}}}}{{\rm{1}}}{\rm{ = III}}\end{array}\)
Vậy hóa trị của Fe trong hợp chất trên có hóa trị III.
7.12
Chọn câu trả lời đúng:
A. Hợp chất ammonia có công thức hóa học là NH4.
B. Hợp chất carbon monooxide có công thức hóa học là CO2.
C. Hợp chất iron (III) oxide có công thức hóa học là Fe3O2.
D. Hợp chất zinc oxide có công thức hóa học là ZnO.

- Quy tắc hóa trị: Trong công thức hóa học của hợp chất hai nguyên tố, tích của chỉ số và hóa trị của nguyên tố này bằng tích của chỉ số và hóa trị của nguyên tố kia.
Ví dụ: \({\rm{P}}_{\rm{2}}^{\rm{V}}{\rm{O}}_{\rm{5}}^{{\rm{II}}}\), ta có: 2 . V = 5 . II.
- Quy ước:
+ Nguyên tố H luôn có hóa trị I.
⇨ Nguyên tử của nguyên tố khác liên kết với bao nhiêu H thì hóa trị bằng bấy nhiêu,
+ Nguyên tố O luôn có hóa trị II.

- Hợp chất ammonia là hợp chất của nitrogen hóa trị III và hydrogen hóa trị I.
Ta có công thức hóa học dạng chung của ammonia là \({\rm{N}}_{\rm{x}}^{{\rm{III}}}{\rm{H}}_{\rm{y}}^{\rm{I}}\)
Áp dụng quy tắc hóa trị: x . III = y . I
\( \Rightarrow \frac{{\rm{x}}}{{\rm{y}}}{\rm{ = }}\frac{{\rm{I}}}{{{\rm{III}}}}{\rm{ = }}\frac{{\rm{1}}}{{\rm{3}}}\)
⇨ Chọn x = 1; y = 3.
⇨ Công thức hóa học cần tìm là NH3. ⇨ A sai.
- Hợp chất carbon monooxide là hợp chất của carbon hóa trị II và oxygen hóa trị II
Ta có công thức hóa học dạng chung của carbon monooxide là \({\rm{C}}_{\rm{x}}^{{\rm{II}}}{\rm{O}}_{\rm{y}}^{{\rm{II}}}\)
Áp dụng quy tắc hóa trị: x . II = y . II
\( \Rightarrow \frac{{\rm{x}}}{{\rm{y}}}{\rm{ = }}\frac{{{\rm{II}}}}{{{\rm{II}}}}{\rm{ = }}\frac{{\rm{2}}}{{\rm{2}}}{\rm{ = }}\frac{{\rm{1}}}{{\rm{1}}}\)
⇨ Chọn x = 1; y = 1.
⇨ Công thức hóa học cần tìm là CO. ⇨ B sai.
- Hợp chất iron (III) oxide là hợp chất của iron hóa trị III và oxygen hóa trị II.
Ta có công thức hóa học dạng chung của iron (III) oxide là \({\rm{Fe}}_{\rm{x}}^{{\rm{III}}}{\rm{O}}_{\rm{y}}^{{\rm{II}}}\)
Áp dụng quy tắc hóa trị: x . III = y . II
\( \Rightarrow \frac{{\rm{x}}}{{\rm{y}}}{\rm{ = }}\frac{{{\rm{III}}}}{{{\rm{II}}}}{\rm{ = }}\frac{3}{{\rm{2}}}{\rm{ }}\)
⇨ Chọn x = 3; y = 2.
⇨ Công thức hóa học cần tìm là Fe2O3. ⇨ C sai.
- Hợp chất zinc oxide là hợp chất của Zinc hóa trị II và oxygen hóa trị II.
Ta có công thức hóa học dạng chung của zinc oxide là \({\rm{Zn}}_{\rm{x}}^{{\rm{II}}}{\rm{O}}_{\rm{y}}^{{\rm{II}}}\)
Áp dụng quy tắc hóa trị: x . II = y . II
\( \Rightarrow \frac{{\rm{x}}}{{\rm{y}}}{\rm{ = }}\frac{{{\rm{II}}}}{{{\rm{II}}}}{\rm{ = }}\frac{{\rm{2}}}{{\rm{2}}}{\rm{ = }}\frac{{\rm{1}}}{{\rm{1}}}\)
⇨ Chọn x = 1; y = 1.
⇨ Công thức hóa học cần tìm là ZnO. ⇨ D đúng.
⇨ Chọn D.
7.13
Cho biết công thức hóa học của hợp chất được tạo bởi hai nguyên tố X và O (oxygen); Y và H (hydrogen) lần lượt là XO và YH3.
Hãy lập công thức hóa học của hợp chất giữa X với Y, biết X và Y có hóa trị bằng hóa trị của chúng trong các hợp chất XO và YH3.

- Quy tắc hóa trị: Trong công thức hóa học của hợp chất hai nguyên tố, tích của chỉ số và hóa trị của nguyên tố này bằng tích của chỉ số và hóa trị của nguyên tố kia.
Ví dụ: \({\rm{P}}_{\rm{2}}^{\rm{V}}{\rm{O}}_{\rm{5}}^{{\rm{II}}}\), ta có: 2 . V = 5 . II.
- Quy ước:
+ Nguyên tố H luôn có hóa trị I.
⇨ Nguyên tử của nguyên tố khác liên kết với bao nhiêu H thì hóa trị bằng bấy nhiêu,
+ Nguyên tố O luôn có hóa trị II.

Để tìm được công thức hóa học của hợp chất được tại bởi nguyên tố X và Y, ta cần biết được hóa trị của hai nguyên tố X và Y.
- Xét hợp chất XO.
Gọi hóa trị của X cần tìm là A
Ta có công thức dạng chung: \({\rm{X}}_{\rm{1}}^{\rm{A}}{\rm{O}}_{\rm{1}}^{{\rm{II}}}\)
Áp dụng quy tắc hóa trị:
\(\begin{array}{l}{\rm{A }}{\rm{. 1 = II }}{\rm{. 1}}\\ \Rightarrow {\rm{A = }}\frac{{{\rm{II }}{\rm{. 1}}}}{{\rm{1}}}{\rm{ = II}}\end{array}\)
Vậy hóa trị của X là II.
- Xét hợp chất YH3.
Gọi hóa trị của Y cần tìm là B
Ta có công thức dạng chung: \({\rm{Y}}_{\rm{1}}^{\rm{B}}{\rm{H}}_{\rm{3}}^{\rm{I}}\)
Áp dụng quy tắc hóa trị:
\(\begin{array}{l}{\rm{B }}{\rm{. 1 = I }}{\rm{. 3}}\\ \Rightarrow {\rm{B = }}\frac{{{\rm{I }}{\rm{. 3}}}}{{\rm{1}}}{\rm{ = III}}\end{array}\)
Vậy hóa trị của Y là III.
- Hợp chất của X hóa trị II và Y hóa trị III.
Ta có công thức hóa học dạng chung của hợp chất là \({\rm{X}}_{\rm{x}}^{{\rm{II}}}{\rm{Y}}_{\rm{y}}^{{\rm{III}}}\)
Áp dụng quy tắc hóa trị: x . II = y . III
\( \Rightarrow \frac{{\rm{x}}}{{\rm{y}}}{\rm{ = }}\frac{{{\rm{III}}}}{{{\rm{II}}}}{\rm{ = }}\frac{3}{2}\)
⇨ Chọn x = 3; y = 2.
⇨ Công thức hóa học cần tìm là X3Y2.
7.14
Lập công thức hóa học và tính khối lượng phân tử của hợp chất được tạo thành bởi:
a) K và Cl, Ba và Cl, Al và Cl.
b) K và nhóm SO4, Ba và nhóm SO4, Al và nhóm SO4.
(Biết khối lượng nguyên tử của K = 39; Cl = 35,5; Ba = 137; Cl = 27; S = 32; O = 16).

- Quy tắc hóa trị: Trong công thức hóa học của hợp chất hai nguyên tố, tích của chỉ số và hóa trị của nguyên tố này bằng tích của chỉ số và hóa trị của nguyên tố kia.
Ví dụ: \({\rm{P}}_{\rm{2}}^{\rm{V}}{\rm{O}}_{\rm{5}}^{{\rm{II}}}\), ta có: 2 . V = 5 . II.
- Quy ước:
+ Nguyên tố H luôn có hóa trị I.
⇨ Nguyên tử của nguyên tố khác liên kết với bao nhiêu H thì hóa trị bằng bấy nhiêu,
+ Nguyên tố O luôn có hóa trị II.
- Khối lượng phân tử AxBy
\({{\rm{M}}_{{{\rm{A}}_{\rm{x}}}{{\rm{B}}_{\rm{y}}}}}{\rm{ = x }}{\rm{. }}{{\rm{M}}_{\rm{A}}}{\rm{ + y }}{\rm{. }}{{\rm{M}}_{\rm{B}}}\)

a) * K và Cl
Ta có công thức hóa học dạng chung của potassium và chlorine là \({\rm{K}}_{\rm{x}}^{\rm{I}}{\rm{Cl}}_{\rm{y}}^{\rm{I}}\)
Áp dụng quy tắc hóa trị: x . I = y . I
\( \Rightarrow \frac{{\rm{x}}}{{\rm{y}}}{\rm{ = }}\frac{{\rm{I}}}{{\rm{I}}}{\rm{ = }}\frac{1}{{\rm{1}}}\)
⇨ Chọn x = 1; y = 1.
⇨ Công thức hóa học cần tìm là KCl.
\(\begin{array}{l} \Rightarrow {{\rm{M}}_{{\rm{KCl}}}}{\rm{ = 1 }}{\rm{. }}{{\rm{M}}_{\rm{K}}}{\rm{ + 1 }}{\rm{. }}{{\rm{M}}_{{\rm{Cl}}}}\\{\rm{ = 39 + 35,5 = 74,5 (amu)}}\end{array}\)
* Ba và Cl
Ta có công thức hóa học dạng chung của barium và chlorine là \({\rm{Ba}}_{\rm{x}}^{{\rm{II}}}{\rm{Cl}}_{\rm{y}}^{\rm{I}}\)
Áp dụng quy tắc hóa trị: x . II = y . I
\( \Rightarrow \frac{{\rm{x}}}{{\rm{y}}}{\rm{ = }}\frac{{\rm{I}}}{{{\rm{II}}}}{\rm{ = }}\frac{1}{{\rm{2}}}\)
⇨ Chọn x = 1; y = 2.
⇨ Công thức hóa học cần tìm là BaCl2.
\(\begin{array}{l} \Rightarrow {{\rm{M}}_{{\rm{BaC}}{{\rm{l}}_2}}}{\rm{ = 1 }}{\rm{. }}{{\rm{M}}_{{\rm{Ba}}}}{\rm{ + 2 }}{\rm{. }}{{\rm{M}}_{{\rm{Cl}}}}\\{\rm{ = 137 + 2 }}{\rm{. 35,5 = 208 (amu)}}\end{array}\)
* Al và Cl
Ta có công thức dạng chung của aluminium và chlorine: \({\rm{Al}}_{\rm{x}}^{{\rm{III}}}{\rm{Cl}}_{\rm{y}}^{\rm{I}}\)
Áp dụng quy tắc hóa trị, ta có: x . III = y . I
\( \Rightarrow \frac{{\rm{x}}}{{\rm{y}}}{\rm{ = }}\frac{{\rm{I}}}{{{\rm{III}}}}{\rm{ = }}\frac{{\rm{1}}}{{\rm{3}}}\)
⇨ Chọn x = 1; y = 3.
⇨ Công thức hóa học cần tìm là AlCl3.
\(\begin{array}{l} \Rightarrow {{\rm{M}}_{{\rm{AlC}}{{\rm{l}}_3}}}{\rm{ = 1 }}{\rm{. }}{{\rm{M}}_{{\rm{Al}}}}{\rm{ + 3 }}{\rm{. }}{{\rm{M}}_{{\rm{Cl}}}}\\{\rm{ = 27 + 3 }}{\rm{. 35,5 = 133,5 (amu)}}\end{array}\)
b) * Ta có công thức hóa học chung của potassium và gốc sunfat là: \({K_x}{(S{O_4})_y}\)
Áp dụng quy tắc hóa trị: x. II = y. I
\(\frac{x}{y} = \frac{2}{1}\)
Chọn x = 2; y = 1
Công thức hóa học cần tìm là:
\({M_{{K_2}SO4}}\)= 2. \({M_K}\)+ 1.\({M_{BaS{O_{_4}}}} = 1.{M_{Ba}} + 1.{M_{S{O_4}}}\)= 2.39 + 1. 96 = 174 (amu)
* Ta có công thức hóa học chung của barium và gốc sunfat là: \(B{a_x}{(SO4)_y}\)
Áp dụng quy tắc hóa trị: x. II = y. II
\(\frac{x}{y} = \frac{2}{2}\)
Chọn x = 1; y= 1
Công thức hóa học cần tìm là : \(BaS{O_4}\)
\({M_{BaS{O_4}}} = 1.{M_{Ba}} + 1.{M_{S{O_4}}}\) = 137 + 96 = 233(amu)
* Ta có công thức hóa học chung của alumiat và gốc sunfat là:
Áp dụng quy tắc hóa trị: x. II = y. III
\(\frac{x}{y} = \frac{2}{3}\)
Chọn x = 2; y = 3
Công thức hóa học cần tìm là \(A{l_2}{(S{O_4})_3}\)
\({M_{A{l_2}{{(SO4)}_3}}} = 2.{M_{Al}} + 3.{M_{S{O_4}}}\) = 2.27 + 3.96 = 324(amu)
7.15
Xác định thành phần phần trăm của các nguyên tố trong các hợp chất sau:
a) Si và O trong hợp chất SiO2 (là thành phần chính của thủy tinh).
b) Na và Cl trong hợp chất NaCl (muối ăn).
(Biết khối lượng nguyên tử của Si = 28; O = 16; Na = 23; Cl = 35,5).

- Khối lượng phân tử của một chất bằng tổng khối lượng của các nguyên tử trong phân tử khối của chất đó.
Đơn vị: amu.


a) SiO2 (thành phần chính của thủy tinh).
\(\begin{array}{l}{{\rm{M}}_{{\rm{Si}}{{\rm{O}}_{\rm{2}}}}}{\rm{ = 28 + 16 }}{\rm{. 2 = 60 (amu)}}\\{\rm{\% }}{{\rm{m}}_{{\rm{Si}}}}{\rm{ = }}\frac{{{\rm{1 }}{\rm{. 28}}}}{{60}}{\rm{ }}{\rm{. 100\% }} \approx {\rm{ 46,7\% }}\\{\rm{\% }}{{\rm{m}}_{\rm{O}}}{\rm{ = 100\% - 46,7\% = 53,3\% }}\end{array}\)
b) NaCl (muối ăn).
\(\begin{array}{l}{{\rm{M}}_{{\rm{NaCl}}}}{\rm{ = 23 + 35,5 = 58,5 (amu)}}\\{\rm{\% }}{{\rm{m}}_{{\rm{Na}}}}{\rm{ = }}\frac{{{\rm{1 }}{\rm{. 23}}}}{{58,5}}{\rm{ }}{\rm{. 100\% }} \approx {\rm{ 39,3\% }}\\{\rm{\% }}{{\rm{m}}_{{\rm{Cl}}}}{\rm{ = 100\% - 39,3\% = 60,7\% }}\end{array}\)
7.16
Tỉ lệ khối lượng giữa hai nguyên tố carbon và hydrogen trong hợp chất methan luôn không đổi là 3 : 1. Hãy lập công thức hóa học của khí methane, biết khối lượng nguyên tử của C = 12; H = 1.

- Công thức hóa học của một chất là cách biểu diễn chất bằng kí hiệu hóa học của nguyên tố kèm theo chỉ số ở chân bên phải kí hiệu hóa học.
- Chỉ số là những số nguyên, cho biết số nguyên tử của mỗi nguyên tố trong phân tử hợp chất. Chỉ số bằng 1 thì không ghi.
- Có thể tìm công thức hóa học của hợp chất bằng cách tìm chỉ số nguyên tối giản của các nguyên tử trong hợp chất.

Gọi công thức hóa học của khí methane là CxHy.
Ta có:
Khối lượng nguyên tử C trong khí methane: mC = 12.x = 12x
Khối lượng nguyên tử H trong khí methane: mH = 1.y = y
Theo đề bài:
\(\begin{array}{l}\frac{{{{\rm{m}}_{\rm{C}}}}}{{{{\rm{m}}_{\rm{H}}}}}{\rm{ = }}\frac{{\rm{3}}}{{\rm{1}}} \Leftrightarrow \frac{{{\rm{12x}}}}{{\rm{y}}}{\rm{ = }}\frac{{\rm{3}}}{{\rm{1}}} \Leftrightarrow \frac{{\rm{x}}}{{\rm{y}}}{\rm{ = }}\frac{{\rm{3}}}{{{\rm{12}}}}{\rm{ = }}\frac{{\rm{1}}}{{\rm{4}}}\\ \Rightarrow {\rm{x = 1; y = 4}}\end{array}\)
⇨ Công thức hóa học của khí methane là CH4.
7.17
Nguyên tử của các nguyên tố X, Y và Z lần lượt có 8, 17 và 11 electron. Nguyên tử neon và argon lần lượt có 10 và 18 electron.
a) Xác định công thức hóa học của hợp chất được tạo thành từ các nguyên tử của các nguyên tố sau:
(i) X và Z (ii) Y và Z (iii) X với X.
b) Kiểu liên kết hóa học giữa các nguyên tử trong các hợp chất trên là liên kết gì?
c) Dự đoán hai tính chất của hợp chất được tạo thành trong trường hợp a(i) và a(ii).

a)- X (Z = 8): X ở nhóm VIA trong bảng tuần hoàn.
⇨ X có 6 electron lớp ngoài cùng và X là phi kim.
⇨ X thiếu 2 electron để có lớp electron ngoài cùng giống Ne.
- Y (Z = 17): Y ở nhóm VIIA trong bảng tuần hoàn.
⇨ Y có 7 electron lớp ngoài cùng và X là phi kim.
⇨ Y thiếu 1 electron để có lớp electron ngoài cùng giống Ar.
- Z (Z = 11): Z ở nhóm IA trong bảng tuần hoàn.
⇨ Z có 1 electron lớp ngoài cùng và Z là kim loại.
⇨ Y dư 1 electron để có lớp electron ngoài cùng giống Ne.
(i) X là phi kim và Z là kim loại
⇨ X và Z tạo hợp chất có liên kết ion.
Để đạt được lớp electron giống khí hiếm gần chúng, X nhận 2 electron, Z nhường 1 electron.
⇨ Một nguyên tử X liên kết ion với hai nguyên tử Z.
⇨ Công thức hóa học của X và Z là Z2X.
(ii) Y là phi kim và Z là kim loại
⇨ Y và Z tạo hợp chất có liên kết ion.
Để đạt được lớp electron giống khí hiếm gần chúng, Y nhận 1 electron, Z nhường 1 electron.
⇨ Một nguyên tử Y liên kết ion với một nguyên tử Z.
⇨ Công thức hóa học của Y và Z là ZY.
(iii) X là phi kim
⇨ Hai nguyên tử của nguyên tố X tạo hợp chất cộng hóa trị.
Để đạt được lớp electron giống khí hiếm gần chúng, mỗi nguyên tử X đưa 2 electron để dùng chung.
⇨ Một nguyên tử X liên kết cộng hóa trị với một nguyên tử X.
⇨ Công thức hóa học của X với X là X2.
b) Z2X, ZY có liên kết hóa học là liên kết ion.
X2 có liên kết hóa học là liên kết cộng hóa trị.
c) Vì Z2X, ZY có liên kết hóa học là liên kết ion nên hợp chất của chúng là chất rắn ở điều kiện thường, khi tan trong nước tạo thành dung dịch dẫn điện.
* Lưu ý: để viết công thức hóa học của các hợp chất trên, sau khi đã biết hóa trị của các nguyên tố, để tim được chỉ số của các nguyên tử trong hợp chất, ta có thể dùng quy tắc hóa trị.
