Câu hỏi/bài tập:
Cho các nguyên tố sau: Li, Na, K, Ca. Nguyên tử của nguyên tố có bán kính bé nhất là
A. Li.
B. Na.
C. K.
D. Cs.

- Xu hướng biến đổi bán kính nguyên tử:
+ Trong một chu kì, theo chiều tăng dần của điện tích hạt nhân, bán kính nguyên tử giảm dần
+ Trong một nhóm, theo chiều tăng dần của điện tích hạt nhân, bán kính nguyên tử tăng dần
- Cách thực hiện:
Advertisements (Quảng cáo)
+ Bước 1: Xác định vị trí các nguyên tố trong bảng tuần hoàn (chu kì nào? Nhóm nào?)
+ Bước 2: Dựa vào các xu hướng biến đổi để xác định đáp án đúng

- Bước 1: Xác định vị trí các nguyên tố trong bảng tuần hoàn
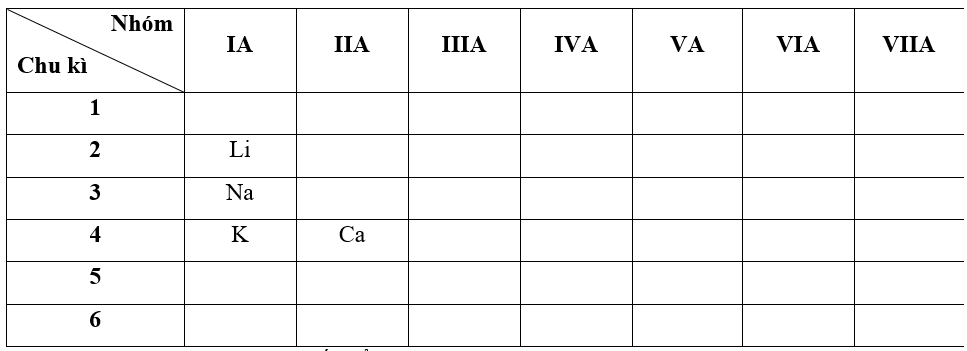
- Bước 2: Dựa vào xu hướng biến đổi bán kính nguyên tử:
+ Trong cùng một nhóm IA, theo chiều tăng dần về điện tích hạt nhân, ta có chiều tăng dần bán kính nguyên tử của các nguyên tố là: Li < Na < K
+ Trong cùng một chu kì 4, theo chiều tăng dần về điện tích hạt nhân, ta có chiều tăng dần bán kính nguyên tử của các nguyên tố là: Ca < K
=> Nguyên tử của nguyên tố có bán kính bé nhất là Li (Do Ca ở chu kì 4 nên có 4 lớp electron ” bán kính nguyên tử sẽ lớn hơn so với Li ở chu kì 2 chỉ có 2 lớp electron)
=> Đáp án: D
