Câu hỏi/bài tập:
Mô tả sự hình thành liên kết, biểu diễn dạng hình học của các ion phức chất sau:
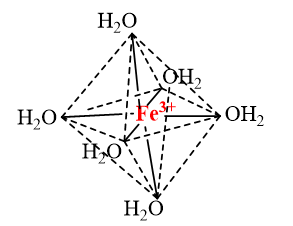
a) Phức chất bát diện \({\left[ {{\rm{Fe}}{{\left( {{{\rm{H}}_{\rm{2}}}{\rm{O}}} \right)}_{\rm{6}}}} \right]^{{\rm{3 + }}}}\).
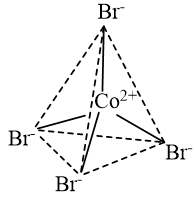
b) Phức chất tứ diện \({\left[ {{\rm{CoB}}{{\rm{r}}_{\rm{4}}}{\rm{ }}} \right]^{{\rm{2 - }}}}\).

- Theo thuyết Liên kết hoá trị, liên kết trong phức chất được hình thành do các phối tử cho cặp electron chưa liên kết vào các orbital lai hoá trống của nguyên tử trung tâm. Kiểu lai hoá các orbital của nguyên tử trung tâm quyết định dạng hình học của phức chất.
- Các phức chất có dạng hình học xác định:
Advertisements (Quảng cáo)
+ Phức chất loại [ML4] thường có dạng hình học tứ diện hoặc vuông phẳng.
+ Phức chất loại [ML6] thường có dạng bát diện.

a) Trong ion phức \({\left[ {{\rm{Fe}}{{\left( {{{\rm{H}}_{\rm{2}}}{\rm{O}}} \right)}_{\rm{6}}}} \right]^{{\rm{3 + }}}}\)có 6 liên kết cho – nhận giữa 6 phối tử \({{\rm{H}}_{\rm{2}}}{\rm{O}}\)với nguyên tử trung tâm \({\rm{F}}{{\rm{e}}^{3 + }}\) (có cấu hình electron [Ar]3d5). Mỗi liên kết cho – nhận được hình thành bởi 1 cặp electron chưa liên kết của phối tử \({{\rm{H}}_{\rm{2}}}{\rm{O}}\) và 1 orbital lai hoá sp3d2 trống của ion \({\rm{F}}{{\rm{e}}^{3 + }}\).
b) Trong ion phức \({\left[ {{\rm{CoB}}{{\rm{r}}_{\rm{4}}}{\rm{ }}} \right]^{{\rm{2 - }}}}\)có 4 liên kết cho – nhận giữa 4 phối tử \({\rm{B}}{{\rm{r}}^ - }\)với nguyên tử trung tâm \({\rm{C}}{{\rm{o}}^{2 + }}\) (có cấu hình electron [Ar]3d7). Mỗi liên kết cho – nhận được hình thành bởi 1 cặp electron chưa liên kết của phối tử \({\rm{B}}{{\rm{r}}^ - }\) và 1 orbital lai hoá sp3 trống của ion \({\rm{C}}{{\rm{o}}^{2 + }}\).