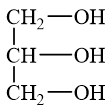
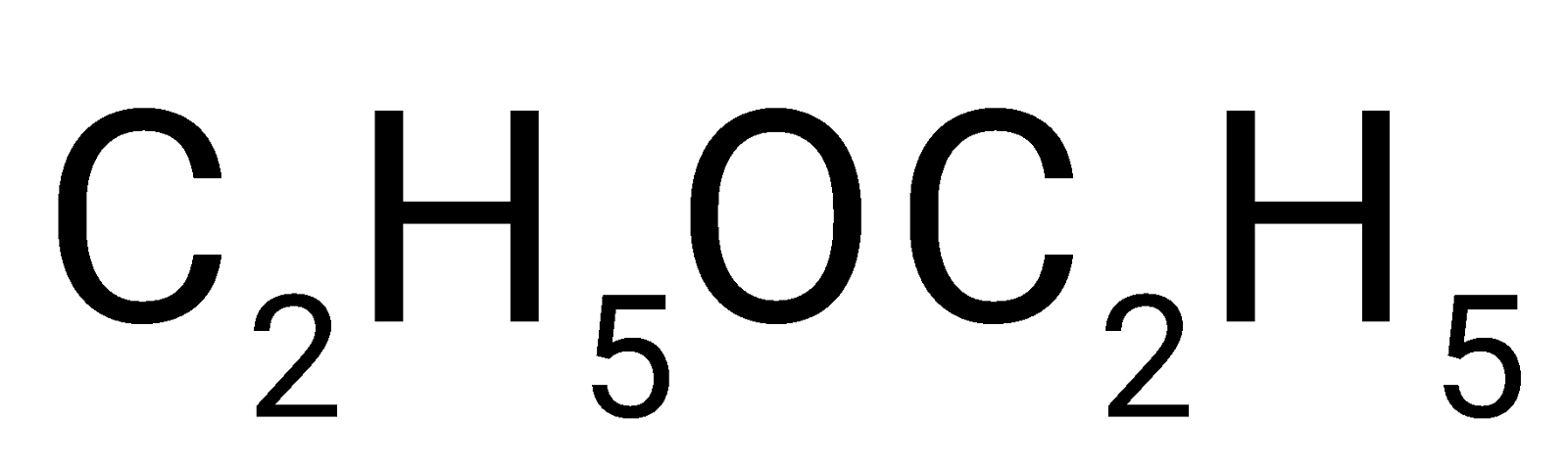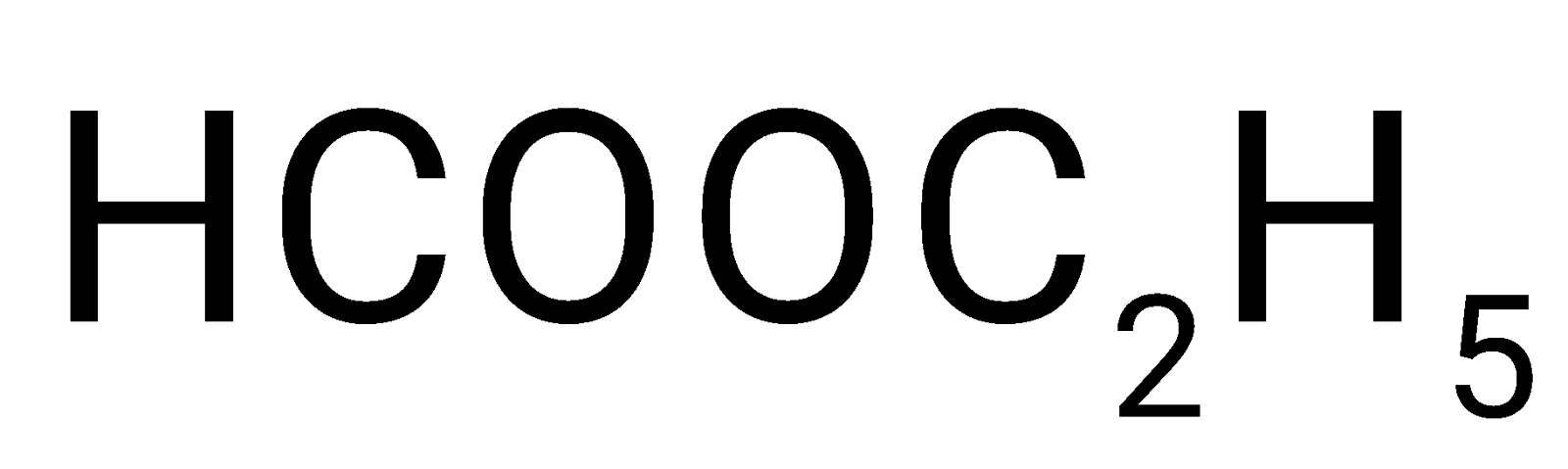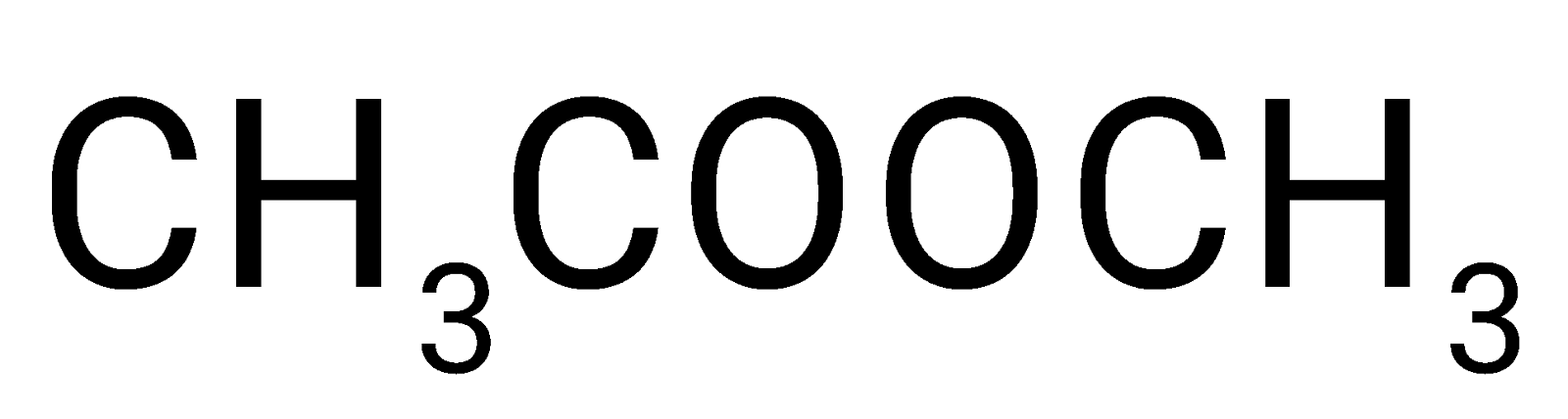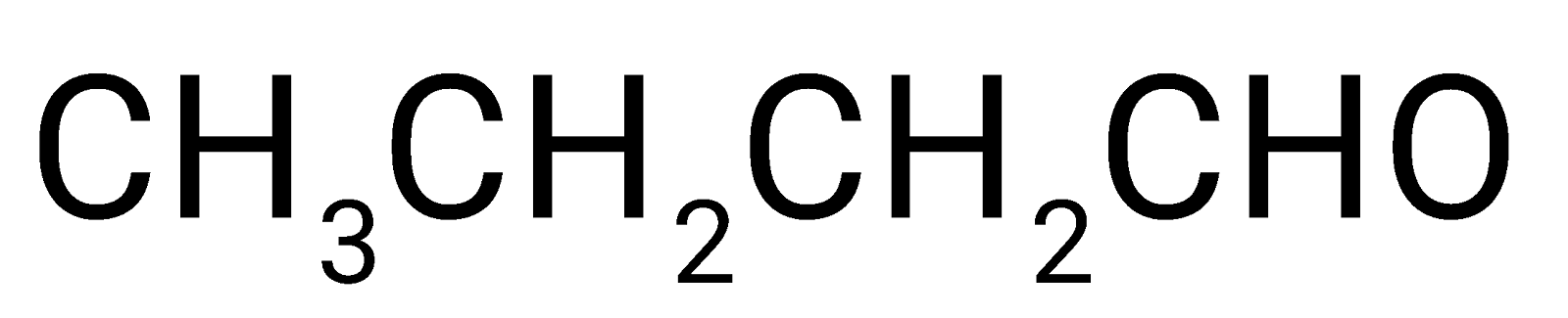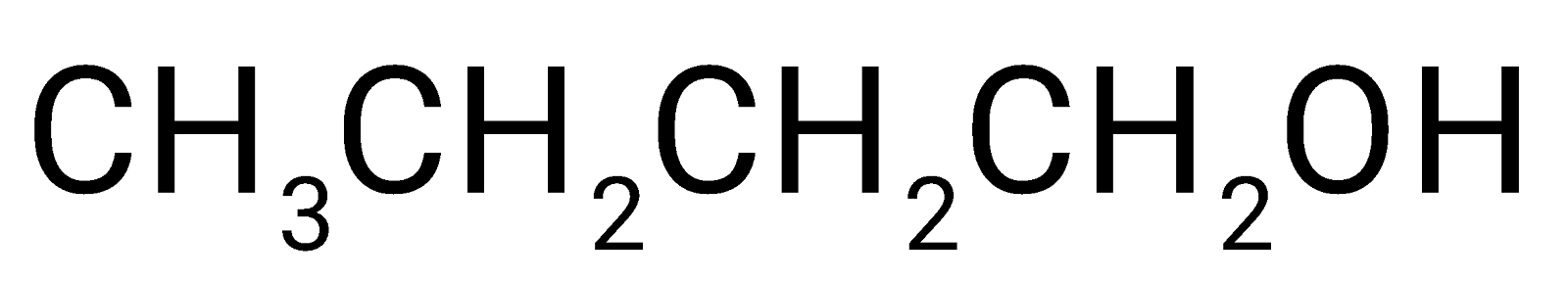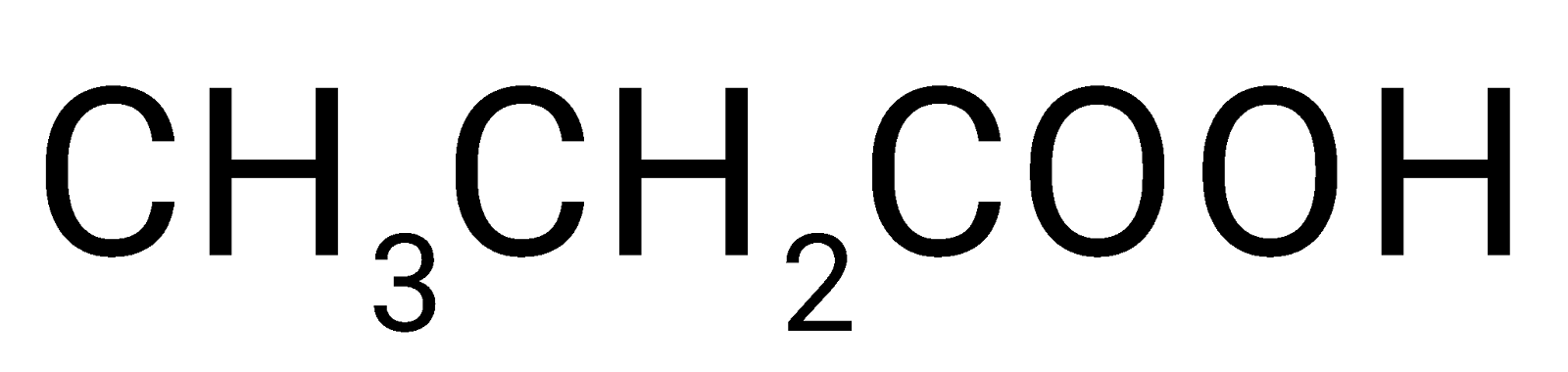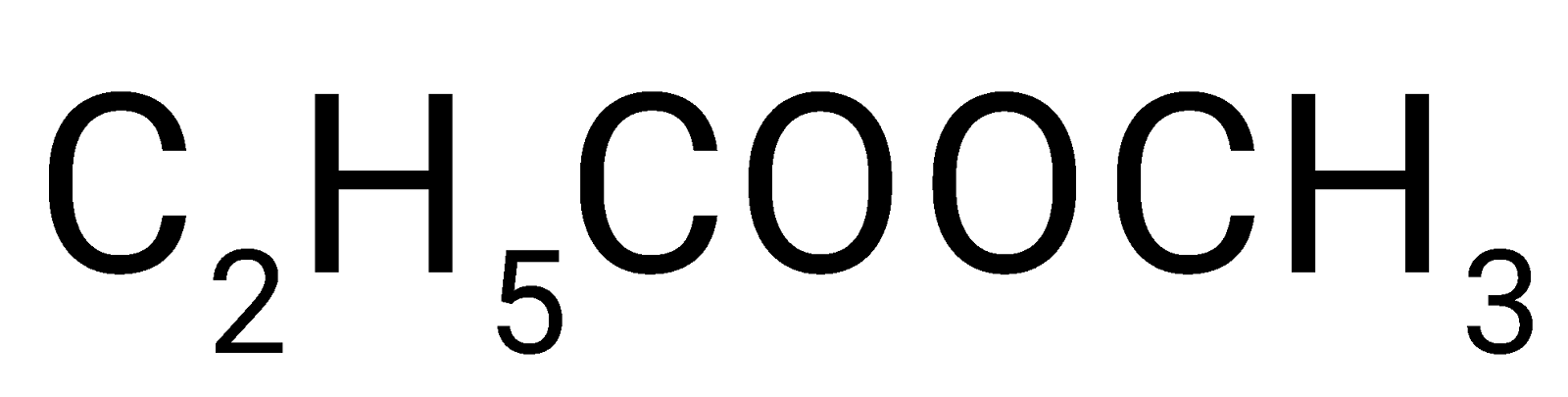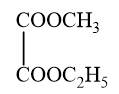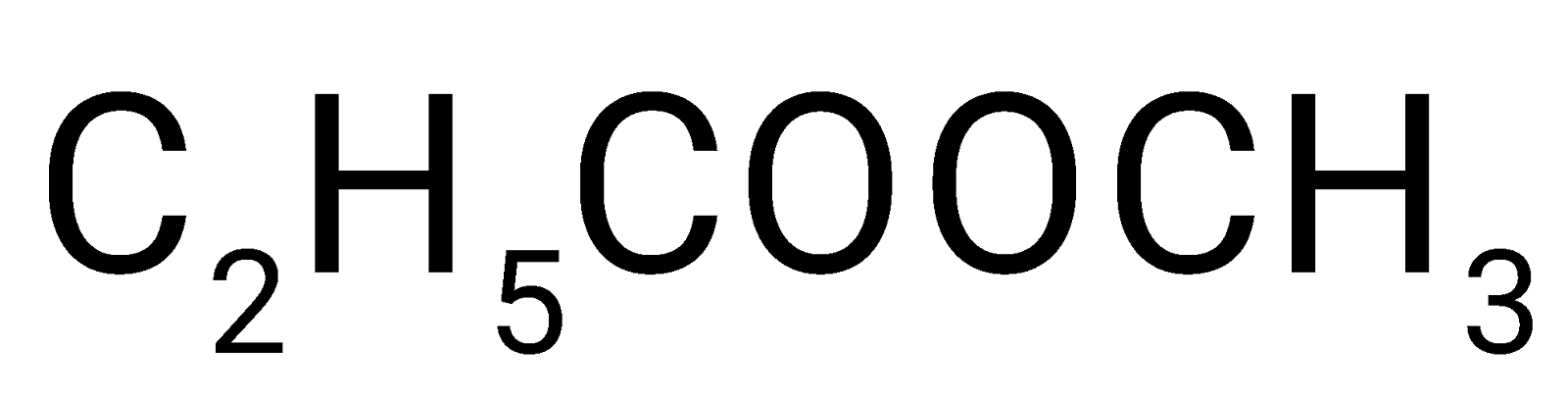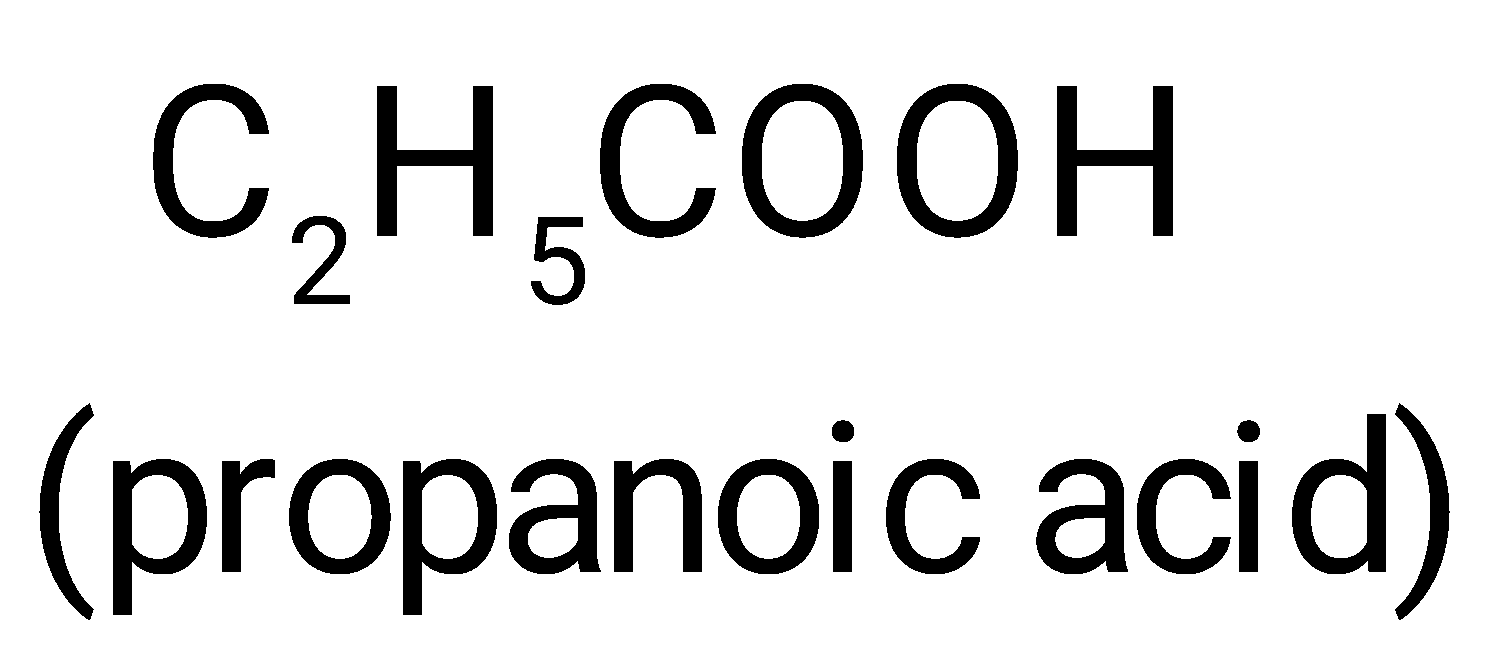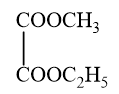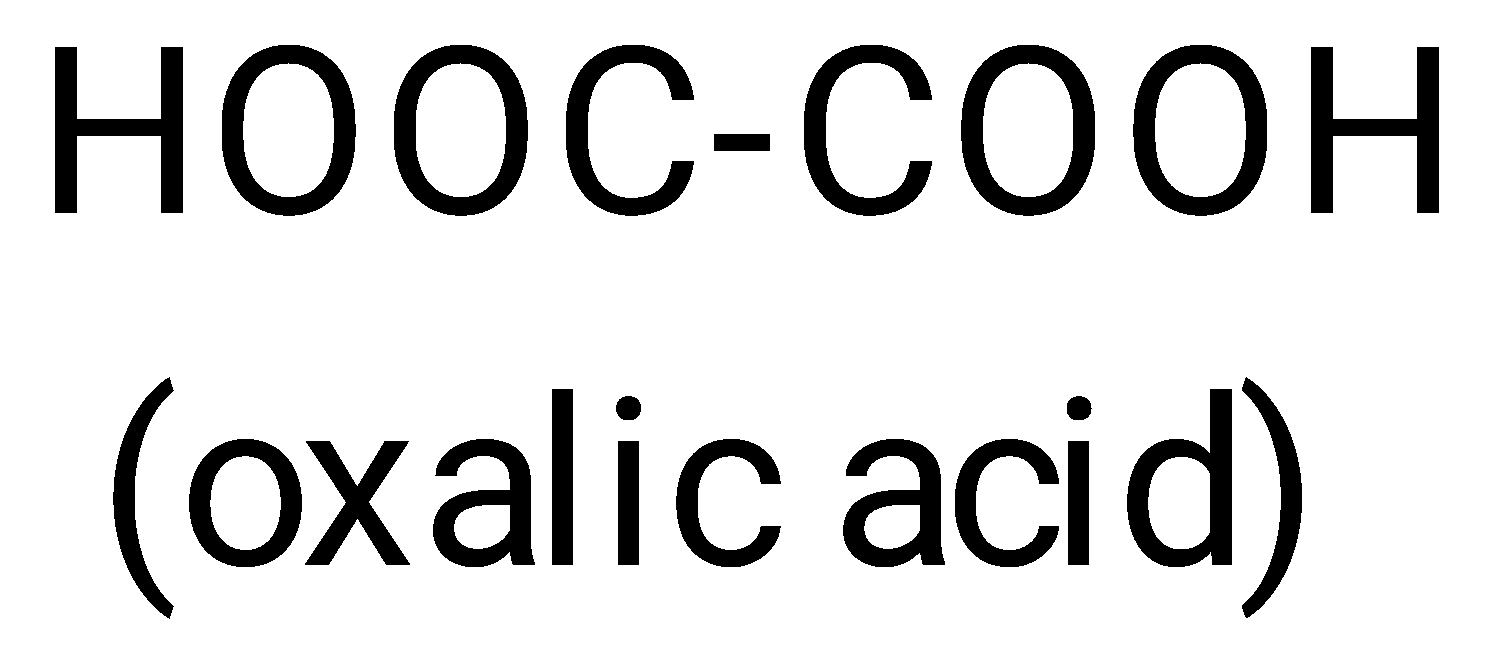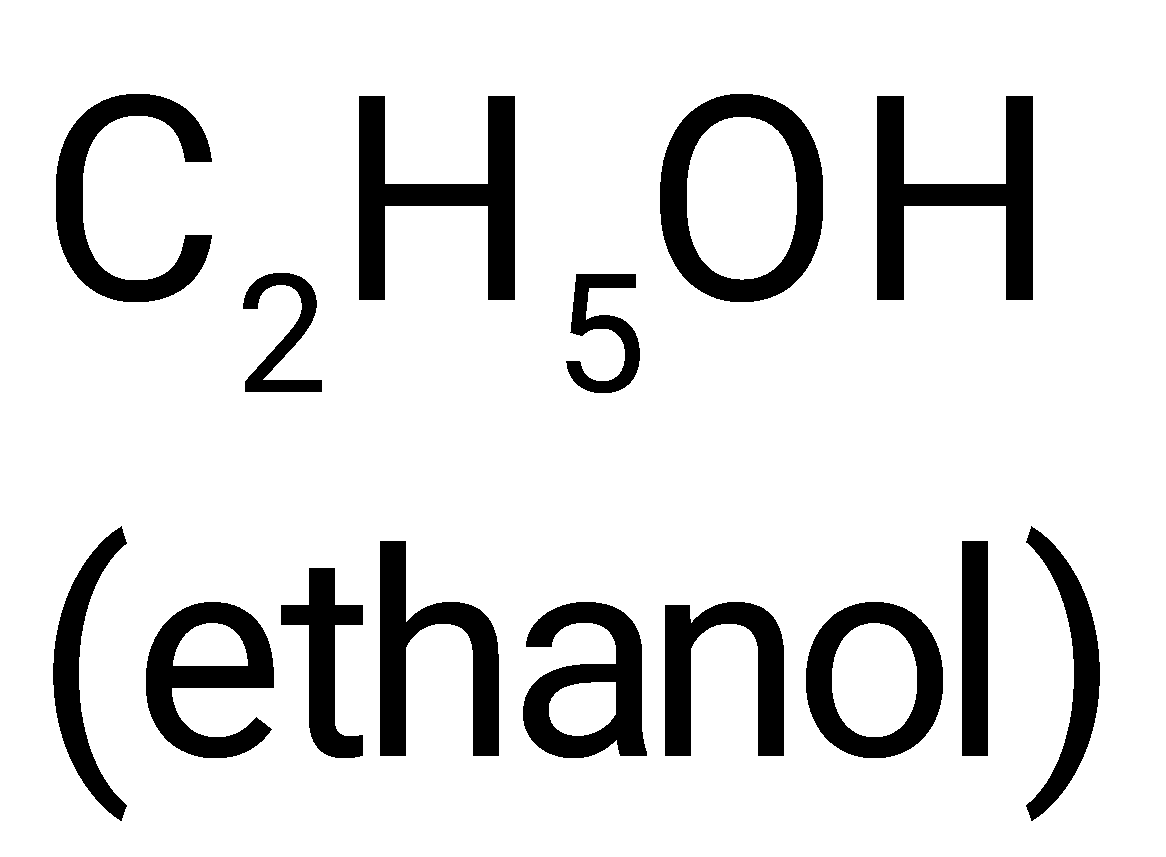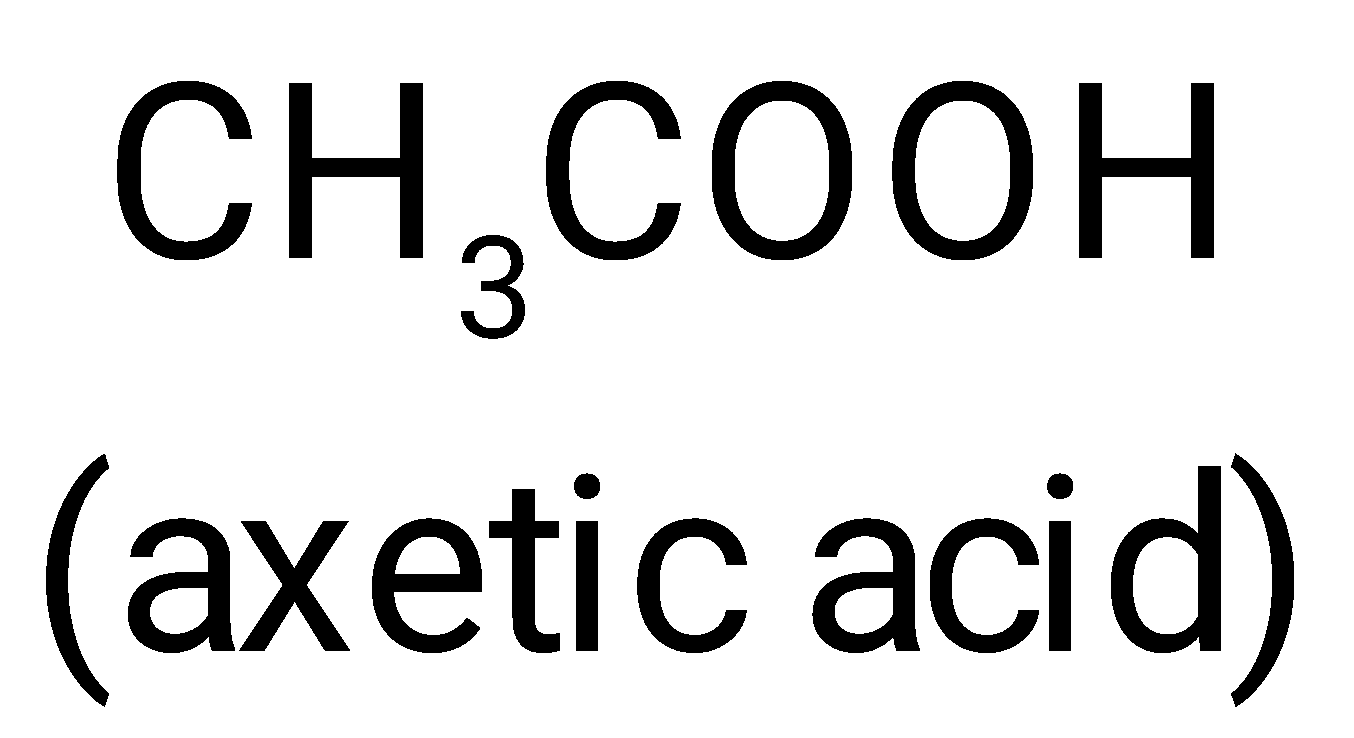1.1
Có bao nhiêu ester có công thức phân tử C4H8O2?
A. 2. B. 3. C. 4. D. 5.

- Khi thay nhóm OH trong nhóm carboxyl của carboxylic acid bằng nhóm OR’ thì được ester. Trong đó, R’ là gốc hydrocarbon.
- Công thức phân tử của ester no, hở, đơn: CnH2nO2 (n ≥ 2).

Các ester có công thức phân tử C4H8O2:
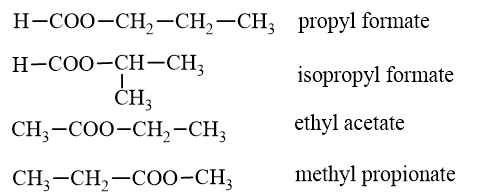
→ Chọn C.
1.2
Có bao nhiêu hợp chất hữu cơ đơn chức khác nhau có công thức phân tử C3H6O2?
A. 2. B. 3. C. 4. D. 5.

Công thức phân tử của ester no, hở, đơn: CnH2nO2 (n ≥ 2).
Công thức phân tử của acid no, hở, đơn: CnH2nO2 (n ≥ 1).

- Các đồng phân ester có công thức phân tử C3H6O2:
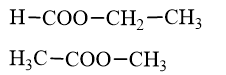
- Các đồng phân acid có công thức phân tử C3H6O2:
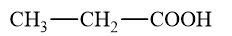
→ Chọn B.
1.3
Có 4 ester no, đơn chức, mạch hở được kí hiệu ngẫu nhiên lần lượt là X, Y, Z, T. Phân tử ester của mỗi chất nêu trên đều tạo bởi các carboxylic acid mạch không phân nhánh và ethyl alcohol. Độ tan của 4 ester được cho ở bảng sau:
|
Ester |
X |
Y |
Z |
T |
|
Độ tan (g/ 100g nước) |
8,7 |
10,5 |
2,2 |
4,9 |
Trong số 4 ester trên, ester có nhiều nguyên tử carbon nhất trong phântử là
A. Y. B. T. C. X. D. Z.

Độ tan trong nước của ester giảm khi độ dài mạch carbon tăng.

Trong số 4 ester trên, ester Z có độ tan nhỏ nhất nên Z có nhiều nguyên tử carbon nhất trong phântử.
→ Chọn D.
1.4
Cho 4 chất sau: butan-1-ol (1), butanoic acid (2), ethyl acetate (3) và pentan-2-ol (4). Chất có nhiệt độ sôi thấp nhất trong 4 chất nêu trên là
A. (1). B. (2). C. (3). D. (4).

Với các hợp chất có khối lượng phân tử tương đương, nhiệt độ sôi được sắp xếp theo thứ tự tăng dần như sau: hydrocarbon; aldehyde; ketone; ester; alcohol; carboxylic acid.

Ester có nhiệt độ sôi thấp hơn alcohol và carboxylic acid có cùng số C hoặc khối lượng nguyên tử tương đương nên Chất có nhiệt độ sôi thấp nhất trong 4 chất nêu trên là ethyl acetate.
→ Chọn C.
1.5
Tinh chất nào sau đây không phải là tính chất thích hợp giúp ethyl methanoate (HCOOC2H5) được sử dụng trong sản xuất một số loại nước hoa?
A. Khả năng dễ cháy. B. Có mùi thơm dễ chịu
C. Không độc hại.D. Nhiệt độ sôi thấp.

Nhiều ester được dùng làm dung môi, methyl methacrylate dùng để sản xuất răng giả, kính áp tròng, xi măng sinh học trong chấn thương chỉnh hình,... một số ester được dùng làm hương liệu trong công nghiệp thực phẩm, mĩ phẩm,...

Khả năng dễ cháy không phải là tính chất thích hợp giúp ethyl methanoate (HCOOC2H5) được sử dụng trong sản xuất một số loại nước hoa.
→ Chọn A.
1.6
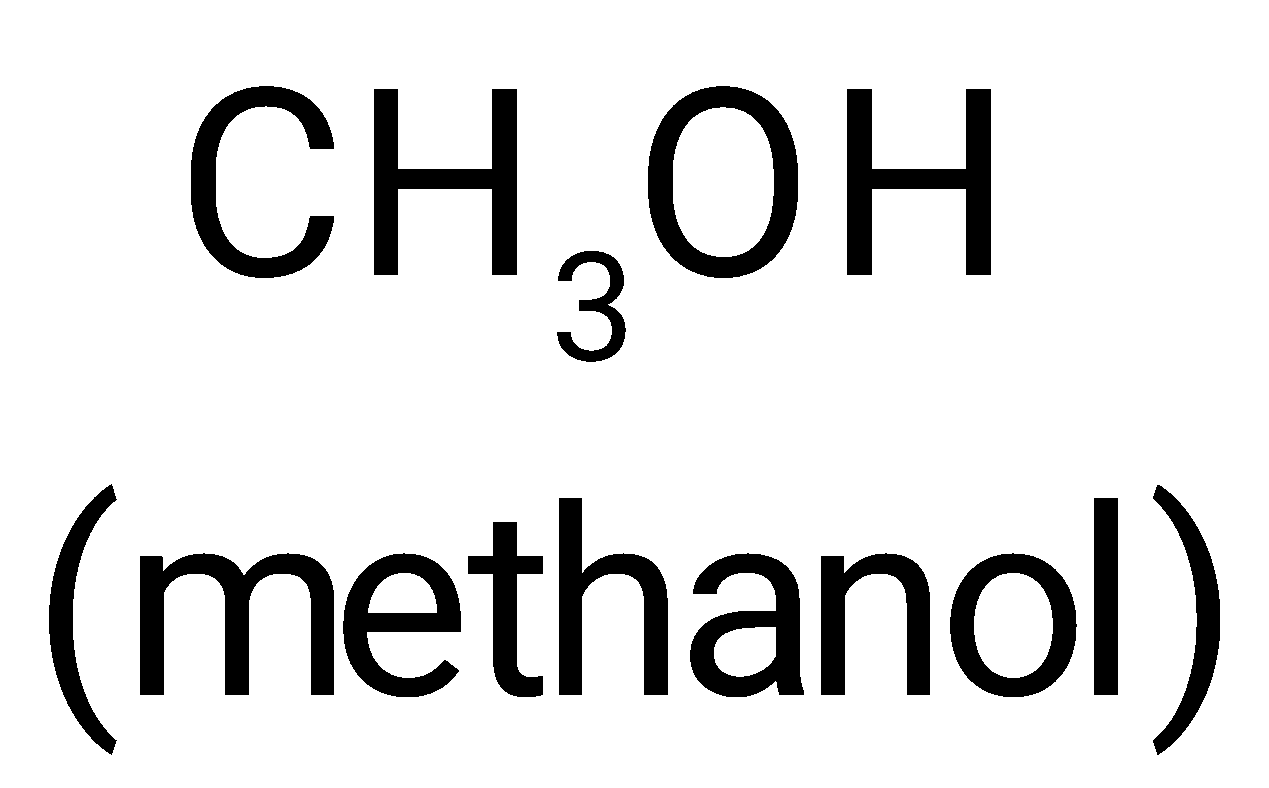
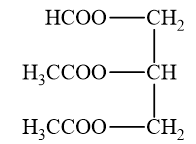
Ngoài sản phẩm phụ là nước, chất hữu cơ nào sau đây được hình thành từ phản ứng hoá học đã cho?
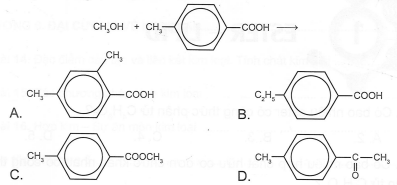

Ester thường được điều chế bằng cách đun hỗn hợp carboxylic acid, alcohol và dung dịch sulfuric acid đặc. Khi đó xảy ra phản ứng ester hoá.
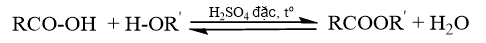

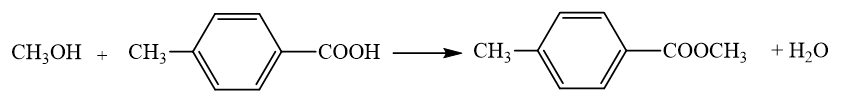
→ Chọn C.
1.7
Aspirin là một trong những loại thuốc giảm đau, hạ sốt được sử dụng rộng rãi trên toàn thế giới. Aspirin có công thức cấu tạo như sau:
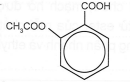
Trong điều kiện ẩm ướt, aspirin có thể bị thuỷ phân để tạo thành salicylic acid và acetic acid. Công thức cấu tạo nào sau đây là của salicylic acid?
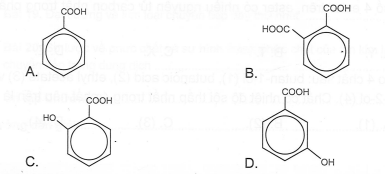

Ester bị thuỷ phân trong môi trường acid thường tạo thành carboxylic acid và alcohol (hoặc phenol) tương ứng. Phản ứng thuỷ phân ester trong môi trường acid thường là phản ứng thuận nghịch.
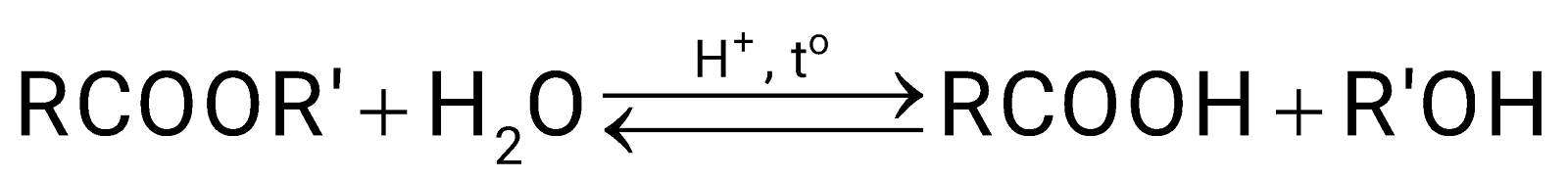

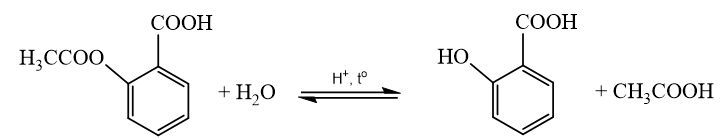
→ Chọn C.
1.8
Một nhóm học sinh đã thực hiện phản ứng điều chế ethyl acetate từ nguyên liệu ban đầu là acetic acid và ethanol trong phòng thí nghiệm. Khi phản ứng kết thúc, nhóm đã thu được hỗn hợp sản phẩm gồm ethyl acetate và acetic acid, ethanol còn dư theo phương trình hoá học:
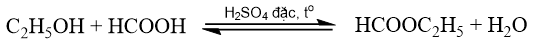
Vì ethyl acetate không phân cực, còn acetic acid và ethanol đều phân cực nên nhóm đã dùng dung môi hữu cơ không phân cực diethyl ether(C2H5OC2H5) để chiết ethyl acetate ra khỏi hỗn hợp sau phản ứng theo sơ đồ sau:
Cho các phát biểu sau về thí nghiệm của nhóm:
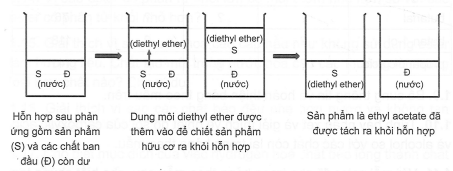
a) Diethyl ether là dung môi chiết lý tưởng trong thí nghiệm trên vì ethyl acetate tan tốt trong dung môi này, còn acetic acid và ethanol lại tan tốt trong nước.
b) Bằng phương pháp chưng cất đơn giản, ta có thể tách ethyl acetate ra khỏi dung môi diethyl ether sau khi chiết.
c) Do diethyl ether có nhiệt độ sôi thấp hơn nhiều so với ethyl acetate (34,6 °C so với 77,1 °C) nên có thể thu được ethyl acetate sau khi chiết bằng cách dùng đèn cồn đun nhẹ cho dung môi diethyl ether bay hơi.
d) Để an toàn, ta có thể dùng nước nóng liên tục tưới lên bình cầu trong phương pháp chưng cất đơn giản để tách ethyl acetate ra khỏi dung môi diethyl ether sau khi chiết.
Số phát biểu đúng là
A. 1. B. 2. C. 3. D. 4.

+ Các phần tử ester có nhiệt độ sôi thấp hơn so với alcohol và carboxylic acid có phân tử khối tương đương.
+ Các ester có phân tử khối thấp và trung bình thường là chất lỏng ở nhiệt độ phòng. Những ester có phân tử khối lớn thường ở dạng rắn. Ester thường nhẹ hơn nước và ít tan trong nước. Một số ester có mùi thơm của hoa, quả chín.

Các phát biểu đúng là a), b) và d).
Phát biểu c) sai vì diethyl ether dễ bay hơi khi đun nóng, hơi diethyl ether dễ cháy nên khi gặp lửa đèn cồn sẽ gây hỏa hoạn nguy hiểm. Do đó, để tách diethyl ether ra khỏi hỗn hợp, ta có thể tưới nước nóng liên tục lên bình cầu chưng cất.
→ Chọn C.
1.9
Bổ sung thông tin và hoàn thiện bảng theo mẫu trên.
|
Tên gọi |
Công thức cấu tạo |
Phân loại |
Phân tử khối |
Nhiệt độ sôi (oC) |
|
Diethyl ether |
? |
? |
? |
34 |
|
Ethyl formate |
? |
? |
? |
54 |
|
Methyl acetate |
? |
? |
? |
57 |
|
Butanal |
? |
? |
? |
76 |
|
Butan – 1 – ol |
? |
? |
? |
118 |
|
Propanoic acid |
? |
? |
? |
141 |

Dựa vào danh pháp để suy ra công thức cấu tạo và phân loại chất.

|
Tên gọi |
Công thức cấu tạo |
Phân loại |
Phân tử khối |
Nhiệt độ sôi (oC) |
|
Diethyl ether |
|
Ether |
74 |
34 |
|
Ethyl formate |
|
Ester |
74 |
54 |
|
Methyl acetate |
|
Ester |
74 |
57 |
|
Butanal |
|
Aldehyde |
72 |
76 |
|
Butan – 1 – ol |
|
Alcohol |
74 |
118 |
|
Propanoic acid |
|
Acid |
74 |
141 |
1.10
Trình bày nhận xét và giải thích về nhiệt độ sôi của carboxylic acid và alcohol so với các chất còn lại trong bảng theo mẫu.

Với các hợp chất có khối lượng phân tử tương đương, nhiệt độ sôi được sắp xếp theo thứ tự tăng dần như sau: hydrocarbon; aldehyde; ketone; ester; alcohol; carboxylic acid.

Nhiệt độ sôi của carboxylic acid và alcohol cao hơn so với các chất có phân tử khối xấp xỉ hoặc tương đương còn lại trong bảng, trong đó nhiệt độ sôi của carboxylic acid cao hơn alcohol. Đó là do chỉ có carboxylic acid và alcohol tạo được liên kết hydrogen liên phân tử, trong đó liên kết hydrogen giữa các phân tử carboxylic acid bền hơn so với giữa các phân tử alcohol.
1.11
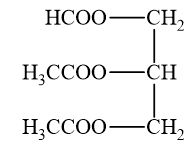
Với mỗi ester đã cho trong bảng theo mẫu sau, cho biết chúng tạo bởi từ những carboxylic acid và alcohol nào?
|
Ester |
Acid tạo thành và tên gọi |
Alcohol tạo thành và tên gọi |
|
|
? |
? |
|
Advertisements (Quảng cáo)
|
? |
? |
|
|
? |
? |

Khi thay thế nhóm OH ở nhóm carboxyl (-COOH) của carboxylic acid bằng nhóm –OR’ thì được ester. Trong đó R’ là gốc hydrocarbon.

|
Ester |
Acid tạo thành và tên gọi |
Alcohol tạo thành và tên gọi |
|
|
|
|
|
|
|
|
|
|
|
(glycerol) |
1.12
Cho 6 hợp chất sau: \({\rm{HCOOH}}\), \({\rm{C}}{{\rm{H}}_{\rm{3}}}{\rm{C}}{{\rm{H}}_{\rm{2}}}{\rm{C}}{{\rm{H}}_{\rm{2}}}{\rm{COOH}}\), \({\rm{C}}{{\rm{H}}_{\rm{3}}}{\rm{C}}{{\rm{H}}_{\rm{2}}}{\rm{C}}{{\rm{H}}_{\rm{2}}}{\rm{C}}{{\rm{H}}_{\rm{2}}}{\rm{OH}}\), \({\rm{C}}{{\rm{H}}_{\rm{3}}}{\rm{COOC}}{{\rm{H}}_{\rm{2}}}{\rm{C}}{{\rm{H}}_3}\),
\({\rm{C}}{{\rm{H}}_{\rm{3}}}{\rm{C}}{{\rm{H}}_{\rm{2}}}{\rm{C}}{{\rm{H}}_{\rm{2}}}{\rm{C}}{{\rm{H}}_{\rm{2}}}{\rm{C}}{{\rm{H}}_{\rm{2}}}{\rm{OH}}\) và \({\rm{HCOOC}}{{\rm{H}}_{\rm{2}}}{\rm{C}}{{\rm{H}}_{\rm{2}}}{\rm{C}}{{\rm{H}}_{\rm{2}}}{\rm{C}}{{\rm{H}}_3}\). Hoàn thiện bảng theo mẫu sau. Giải thích.
|
Hợp chất |
Nhiệt độ sôi (oC) |
Hợp chất |
Nhiệt độ sôi (oC) |
|
\({\rm{HCOOH}}\) |
100,8 |
? |
164 |
|
? |
117,7 |
\({\rm{C}}{{\rm{H}}_{\rm{3}}}{\rm{C}}{{\rm{H}}_{\rm{2}}}{\rm{C}}{{\rm{H}}_{\rm{2}}}{\rm{C}}{{\rm{H}}_{\rm{2}}}{\rm{C}}{{\rm{H}}_{\rm{2}}}{\rm{OH}}\) |
138 |
|
\({\rm{HCOOC}}{{\rm{H}}_{\rm{2}}}{\rm{C}}{{\rm{H}}_{\rm{2}}}{\rm{C}}{{\rm{H}}_{\rm{2}}}{\rm{C}}{{\rm{H}}_3}\) |
107 |
? |
77 |

Với các hợp chất có khối lượng phân tử tương đương, nhiệt độ sôi được sắp xếp theo thứ tự tăng dần như sau: hydrocarbon; aldehyde; ketone; ester; alcohol; carboxylic acid.

Do ester không tạo được liên kết hydrogen giữa các phân tử nên ester có nhiệt độ sôi thấp hơn so với các alcohol và carboxylic acid có cùng số nguyên tử carbon. Mặt khác, nhiệt độ sôi của carboxylic acid luôn cao hơn alcohol có cùng số nguyên tử carbon hoặc có phân tử khối tương đương, còn nhiệt độ sôi của các chất cùng dãy đồng đẳng tăng khi số nguyên tử carbon tăng, ta có kết quả sau:
|
Hợp chất |
Nhiệt độ sôi (oC) |
Hợp chất |
Nhiệt độ sôi (oC) |
|
\({\rm{HCOOH}}\) |
100,8 |
\({\rm{C}}{{\rm{H}}_{\rm{3}}}{\rm{C}}{{\rm{H}}_{\rm{2}}}{\rm{C}}{{\rm{H}}_{\rm{2}}}{\rm{COOH}}\) |
164 |
|
\({\rm{C}}{{\rm{H}}_{\rm{3}}}{\rm{C}}{{\rm{H}}_{\rm{2}}}{\rm{C}}{{\rm{H}}_{\rm{2}}}{\rm{C}}{{\rm{H}}_{\rm{2}}}{\rm{OH}}\) |
117,7 |
\({\rm{C}}{{\rm{H}}_{\rm{3}}}{\rm{C}}{{\rm{H}}_{\rm{2}}}{\rm{C}}{{\rm{H}}_{\rm{2}}}{\rm{C}}{{\rm{H}}_{\rm{2}}}{\rm{C}}{{\rm{H}}_{\rm{2}}}{\rm{OH}}\) |
138 |
|
\({\rm{HCOOC}}{{\rm{H}}_{\rm{2}}}{\rm{C}}{{\rm{H}}_{\rm{2}}}{\rm{C}}{{\rm{H}}_{\rm{2}}}{\rm{C}}{{\rm{H}}_3}\) |
107 |
\({\rm{C}}{{\rm{H}}_{\rm{3}}}{\rm{COOC}}{{\rm{H}}_{\rm{2}}}{\rm{C}}{{\rm{H}}_3}\) |
77 |
1.13
Thuỷ phân hoàn toàn triglyceride X thu được glycerol và 3 acid béo là lauric acid, palmitic acid và oleic acid. X có thể có bao nhiêu công thức cấu tạo?

Khi thay thế nhóm OH ở nhóm carboxyl (-COOH) của carboxylic acid bằng nhóm –OR’ thì được ester. Trong đó R’ là gốc hydrocarbon.

Khi thay thế nhóm OH ở nhóm carboxyl (-COOH) của carboxylic acid bằng nhóm –OR’ thì được ester. Trong đó R’ là gốc hydrocarbon.
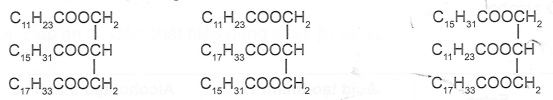
1.14
Vì sao ester có phân tử khối lớn có mùi thơm nhẹ hơn so với các ester có phân tử khối nhỏ hơn?

Dựa vào độ bay hơi của các ester.

Ester có mùi thơm được nhận biết thông qua khứu giác. Điều này phụ thuộc vào hiện tượng bay hơi của ester, có nghĩa liên quan đến nhiệt độ sôi của ester. Các ester có phân tử khối lớn hơn không có mùi thơm mạnh do có nhiệt độ sôi cao hơn các ester có phân tử khối nhỏ. Ngoài ra, các ester có phân tử khối lớn tuy hoà tan được trong chất béo nhưng không hoà tan được trong nước, vì vậy ngay cả khi chúng đến được mũi, chúng cũng sẽ không đi qua lớp chất nhầy để đến được các cơ quan thụ cảm mùi hương. Mặt khác với kích thước cồng kềnh, ester có phân tử khối lớn không tương thích với các thụ thể mùi hương. Do đó, ester có phân tử khối lớn hơn thì mùi thơm nhẹ hơn.
1.15
Giải thích vì sao nước hoa cao cấp hầu như không sử dụng ester làm hương liệu. Chất tạo mùi trong nước hoa cao cấp thường là những loại hợp chất nào? Cho ví dụ.

Khi gặp mồ hôi, ester dễ bị thủy phân tạo carboxylic acid gây mùi hôi.

- Mặc dù hương vị và mùi “trái cây” của ester rất dễ chịu, nhưng chúng hiếm khi được sử dụng trong các loại nước hoa cao cấp. Lý do là các ester không bền với mồ hôi. Khi tiếp xúc với mồ hôi, chúng bị thuỷ phân tạo ra các carboxylic acid thường có mùi không dễ chịu như các ester. Ví dụ, butyric acid có mùi giống như bơ bị ôi thiu, đây cũng là chất có trong thành phần các chất tạo nên mùi hôi cơ thể, được tạo thành do sự thuỷ phân ethyl butyrate và methyl butyrate. Ethyl butyrate và methyl butyrate là những ester có mùi hấp dẫn của dâu và táo.
- Trong nước hoa cao cấp, chất tạo hương có thể là hydrocarbon (terpene), aldehyde hoặc ketone. Ví dụ với terpene, myrcene (Cos) được tìm thấy trong nhiều cây gai dầu, trái cây họ cam quýt, xoài, nguyệt quế, đinh hương, ... Limonene, đồng phân của myrcene được tìm thấy trong vỏ của các loại trái cây có múi, rau mùi, cần tây và hạt hồi, ... Với aldehyde, hầu như không loại nước hoa nào trên thế giới tồn tại mà không có sự hiện diện của chúng, chẳng hạn decanal (C10H20O), undecanal (C11H22O), có trong thành phần tinh dầu cam, quýt, hoa hồng, đã góp phần cùng một số chất tạo mùi khác tạo nên hương thơm đặc sắc của những loại nước hoa nổi tiếng nhất thế giới.
Muscone (C16H30O) là một ketone chủ yếu tạo nên mùi thơm của xạ hương. Xạ hương tạo cho nước hoa một mùi thơm đặc biệt dễ chịu và bền lâu. Ngày nay, xạ hương được sử dụng trong nước hoa đều là xạ hương tổng hợp.
1.16
Giải thích vì sao các chất béo đều nhẹ hơn nước và không tan trong nước.

- Khối lượng riêng của chất béo nhỏ hơn khối lượng riêng của nước.
- Chất béo là phân tử không phân cực, tan không tốt trong dung môi phân cực là nước.

- Chất béo là những chất có phân tử lớn, cồng kềnh hơn nhiều so với phân tử nước. Do đó trong cùng một thể tích không gian, số các phân tử nước hiện diện nhiều hơn so với số các phân tử chất béo. Vì thế, chất béo có khối lượng riêng nhỏ hơn nước nên chất béo nhẹ hơn nước.
- Chất béo là phân tử không phân cực nên không tan trong dung môi phân cực là nước.
1.17
Cho biết mục đích của việc hydrogen hóa chất béo lỏng thành chất béo rắn.

Chất béo chứa gốc acid không no (chất béo lỏng) có phản ứng hydrogen hóa tạo chất béo rắn.

Trong công nghiệp thực phẩm, dầu thực vật được chuyển đổi từ chất lỏng sang chất rắn bằng phản ứng hydrogen hoá. Bơ thực vật (margarine) được “làm cứng” theo cách này để chúng trở nên rắn hoặc bản rắn trong điều kiện thường. Việc làm này sẽ giúp kéo dài thời hạn sử dụng của thực phẩm và giữ hương vị ổn định do khó bị oxi hoá hơn dầu thực vật.
1.18
Một nhóm học sinh dưới sự hướng dẫn của giáo viên muốn thực hiện thí nghiệm điều chế ester nên đã tiến hành theo các bước sau.
Bước 1: Cho vào bình cầu đáy tròn 22 mL pentyl alcohol (D = 0,81 g/mL) và V mL acetic acid (D = 1,05 g/mL).
Bước 2: Thêm tiếp vào bình cầu đó 4 mL dung dịch sulfuric acid đặc và một ít đá bọt. Đun hồi lưu hỗn hợp trong khoảng 30 phút.
Bước 3: Sau một thời gian, nhóm học sinh tiến hành cân khối lượng ester thu được sau khi tách khỏi hỗn hợp và làm sạch, cân hiển thị khối lượng 17 g.
a) Xác định V để tỉ lệ mol giữa pentyl alcohol và acetic acid là 1 : 1.
b) Đá bọt là gì? Nêu vai trò của đá bọt trong thí nghiệm trên.
c) Cho biết đặc điểm của phản ứng xảy ra trong thí nghiệm đã nêu.
d) Tính hiệu suất của phản ứng ester hóa trên.
e) Trong hỗn hợp phản ứng ban đầu ở bình cầu đáy tròn, nhóm thí nghiệm còn cho thêm một ít hạt silica gel có màu xanh vào trước khi đun hồi lưu.
– Mục đích của việc thêm vào các hạt silica gel là gì?
– Giải thích vì sao khi kết thúc thí nghiệm, các hạt silica gel từ màu xanh chuyển sang màu hồng.

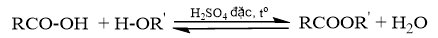
Phản ứng ester hóa là phản ứng giữa alcohol và carboxylic acid.

a) Ta có:
\(\begin{array}{l}{\rm{ }}{{\rm{n}}_{{{\rm{C}}_{\rm{5}}}{{\rm{H}}_{{\rm{12}}}}{\rm{O}}}} = {{\rm{n}}_{{{\rm{C}}_{\rm{2}}}{{\rm{H}}_{\rm{4}}}{{\rm{O}}_2}}}\\ \Leftrightarrow \frac{{22.0,81}}{{88}} = \frac{{{\rm{V}}.1,05}}{{60}}\\ \Rightarrow {\rm{V}} = \frac{{22.0,81.60}}{{88.1,05}} \simeq 11,57{\rm{ (mL)}}\end{array}\)
b) Đá bọt là loại đá được hình thành bởi dung nham núi lửa phun trào, có độ xốp cao và nhẹ.
Vai trò của đá bọt là giúp hỗn hợp phản ứng không bị sôi mạnh.
c) Phản ứng xảy ra trong thí nghiệm là phản ứng ester hóa. Đây là phản ứng thuận nghịch:
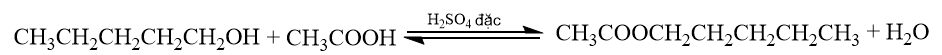
d) Theo phương trình hóa học: \({{\rm{n}}_{{\rm{este(LT)}}}} = {{\rm{n}}_{{\rm{alcohol}}}} = 0,2025{\rm{ }}({\rm{mol}})\)
\(\begin{array}{l} \Rightarrow {{\rm{m}}_{{\rm{este(LT)}}}} = 0,2025.130 = 26,325{\rm{ }}({\rm{g}})\\ \Rightarrow H\% = \frac{{17}}{{26,325}} \times 100\% \simeq 65,58\% \end{array}\)
e) Hạt silica gel có nhiệm vụ hấp thụ nước sinh ra trong phản ứng ester hoá, nhờ đó giúp hiệu suất ester hoá tăng lên.
Hạt silica gel có màu xanh do được nhuộm CoCl2. Khi hấp thụ một lượng nước bão hoà sẽ chuyển sang màu hồng, là màu của phức chất [Co(H2O)6]Cl2, hay viết dưới dạng muối ngậm nước là CoCl2.6H2O.
Bằng cách sấy khô silicagel đã hấp thụ nước, ta có thể tái sử dụng các hạt silica gel đã bão hoà nước.
1.19
Vì sao nói chất béo là thức ăn quan trọng của con người?

Chất béo là nguồn cung cấp các acid béo.

Một lượng nhỏ chất béo là phần thiết yếu của chế độ ăn uống cân bằng, lành mạnh. Chất béo là nguồn cung cấp các acid béo thiết yếu mà cơ thể không tự tổng hợp được. Ngoài ra, chất béo còn giúp cơ thể hấp thụ vitamin A, D và E. Những vitamin này tan trong chất béo, có nghĩa chúng chỉ có thể được cơ thể hấp thụ khi có mặt chất béo.
1.20
Vì sao trong thực tế, dầu thực vật tuy chứa chủ yếu chất béo không no nhưng lại khó bị ôi thiu hơn mỡ động vật chứa chủ yếu chất béo no?

Trong quá trình sản xuất dầu thực vật, người ta thường cho thêm một lượng nhỏ chất chống oxi hoá.

Trong thực tế, dầu thực vật tuy chứa chủ yếu chất béo không no nhưng lại khó bị ôi thiu hơn mỡ động vật chứa chủ yếu chất béo no. Nguyên nhân là do trong quá trình sản xuất dầu thực vật, người ta thường cho thêm một lượng nhỏ chất chống oxi hoá là một số dẫn xuất của phenol.
1.21
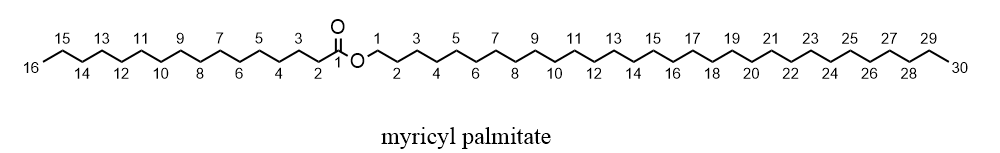
Một trong những cách làm mới lại bề mặt các vật dụng bằng gỗ đó là sử dụng sáp ong để đánh bóng. Sáp ong là một lipid với thành phần chính là myricyl palmitate. Đây là một ester có mạch không phân nhánh, công thức phân tử là C46H92O2. Viết công thức khung phân tử của myricyl palmitate.

Khi thay thế nhóm OH ở nhóm carboxyl (-COOH) của carboxylic acid bằng nhóm –OR’ thì được ester. Trong đó R’ là gốc hydrocarbon.

1.22
a) Viết công thức khung phân tử của stearic acid và oleic acid, biết oleic acid là acid béo omega-9, có liên kết đôi C=C ở dạng cis.
b) Dự đoán nhiệt độ nóng chảy của oleic acid và stearic acid. Giải thích.

Khi thay thế nhóm OH ở nhóm carboxyl (-COOH) của carboxylic acid bằng nhóm –OR’ thì được ester. Trong đó R’ là gốc hydrocarbon.

a)
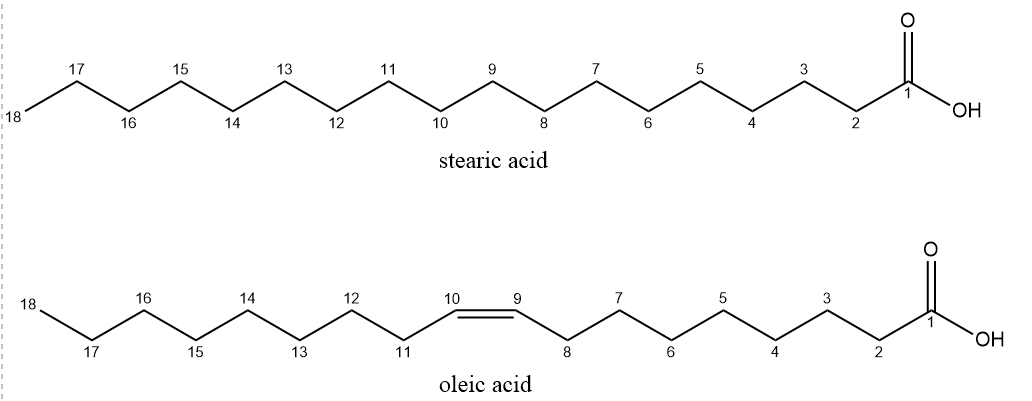
b) Oleic acid có liên kết đôi C=C ở dạng cis, zigzag hơn stearic acid là acid béo no. Do đó các phân tử stearic acid trong mạng tinh thể xếp khít với nhau hơn so với oleic acid. Kết quả là lực hút giữa các phân tử stearic acid mạnh hơn so với oleic acid làm cho nhiệt độ nóng chảy của stearic acid (69 °C) cao hơn oleic acid (13,4 °C).
1.23
Cho bảng số liệu sau:
|
Acid béo |
Palmitic acid |
Stearic acid |
Oleic acid |
|
Nhiệt độ nóng chảy (oC) |
64 |
70 |
4 |
|
Chất béo |
Tripalmitin |
Tristearin |
Triolein |
|
Nhiệt độ nóng chảy (oC) |
66 |
72 |
-4 |
a) Viết công thức cấu tạo các chất béo trong bảng trên.
b) Dầu olive có hàm lượng các gốc oleate là 84%. Dầu ca cao có tổng hàm lượng các gốc palmitate và stearate là 62%. Dầu nào có nhiệt độ đông đặc thấp hơn? Giải thích.

- Khi thay thế nhóm OH ở nhóm carboxyl (-COOH) của carboxylic acid bằng nhóm –OR’ thì được ester. Trong đó R’ là gốc hydrocarbon.
- Ở điều kiện thường các chất béo no ở thể rắn, các chất béo không no ở thể lỏng.

a)
|
Tên chất béo |
Công thức cấu tạo |
|
Tripalmitin |
(C15H31COO)3C3H5 |
|
Tristearin |
(C17H35COO)3C3H5 |
|
Triolein |
(C17H33COO)3C3H5 |
b) Dầu olive có hàm lượng các gốc acid béo không no cao, còn dầu ca cao có tổng hàm lượng các gốc acid béo no cao. Do đó ở điều kiện thường, dầu olive ở thể lỏng còn dầu ca cao lại ở thể rắn, có nghĩa là dầu olive có nhiệt độ đông đặc thấp hơn (–6 °C) so với dầu ca cao (34 °C).