Câu hỏi trang 24
| Câu hỏi mở đầu: Khi các phản ứng hoá học xảy ra, lượng các chất tham gia phản ứng giảm dần, lượng các chất sản phẩm tăng dần vậy tổng khối lượng các chất trước và sau phản ứng có thay đổi khôngCâu hỏi |

áp dụng định luật bảo toàn khối lượng
 Áp dụng định luật bảo toàn khối lượng tổng khối lượng các chất sản phẩm bằng tổng khối lượng các chất tham gia phản ứng
Áp dụng định luật bảo toàn khối lượng tổng khối lượng các chất sản phẩm bằng tổng khối lượng các chất tham gia phản ứng
| Câu hỏi 1: So sánh tổng khối lượng của các chất trước phản ứng với tổng khối lượng các chất sau phản ứng |
Phương pháp giải:
Dựa vào định luật bảo toàn khối lượng để trả lời câu hỏi

ta cốc 1 đổ vào cốc 2 sinh ra phản ứng
BaCl2 + Na2SO4 BaSO4 + 2NaCl
Áp dụng định luật bảo toàn khối lượng ta có
mBaCl2 + mNa2SO4 = mBaSO4 + mNaCl
Vậy tổng khối lượng các chất sản phẩm sau phản ứng bằng với tổng khối lượng chất sản phẩm
Câu hỏi trang 25
| Câu hỏi 1: Giải thích tại sao khối lượng cacbon dyoxid bằng tổng khối lượng carbon oxygen |
Phương pháp giải:
Áp dụng định luật bảo toàn khối lượng

Khối lượng carbon dioxide bằng tổng khối lượng carbon và oxygen vì trong các phản ứng hoá học, chỉ có liên kết giữa các nguyên tử C và O thay đổi, còn số nguyên tử của mỗi nguyên tổ hoá học vẫn giữ nguyên nên tổng khối lượng của các chất tham gìa phản ứng bằng tổng khối lượng của các sản phẩm.
|
Câu hỏi 2: 1. Sau khi đốt cháy than tổ ong (thành phần chính là carbon) thì thu được xỉ than. Xỉ than nặng hơn hay nhẹ hơn than tổ ongCâu hỏi Giải thích. 2. Vôi sống (calcium oxide) phản ứng với một số chất có mặt trong không khí như sau: Calcium oxide + Carbon dioxide ——> Calcium carbonate Calcium oxide + Nước ——> Calcium hydroxide Khi làm thí nghiệm, một học sinh quên đậy nắp lọ đựng vôi sống (thành phần chính là CaO), sau một thời gian thì khối lượng của lọ sẽ thay đổi như thế nàoCâu hỏi |
Phương pháp giải:
Áp dụng định luật bảo toàn khối lượng khối lượng các chất tham gia phản ứng bẳng tổng khối lượng chất sản phẩm.
Dựa vào phương trình hoá học của thí nghiệm để giải thích

1. Xỉ than nhẹ hơn than tổ ong. Vì Carbon đã tác dụng với oxygen trong không khí tạo thành khí carbon dioxide. Lượng khí sinh ra đã làm giảm lượng C trong than làm khối lượng xỉ than nhẹ hơn khối lượng viên than ban đầu.
Carbon + oxygen ——> Carbon dioxide
2. Vôi sống (calcium oxide) phản ứng với một số chất có mặt trong không khí như sau:
Calcium oxide + Carbon dioxide ——> Calcium carbonate
Calcium oxide + Nước ——> Calcium hydroxide
Khi làm thí nghiệm, một học sinh quên đậy nắp lọ đựng vôi sống (thành phần chính là CaO), sau một thời gian thì khối lượng của lọ sẽ tăng lên.
Câu hỏi trang 26
|
Câu hỏi: Lập phương trình hoá học Advertisements (Quảng cáo) a, Fe + O2 → Fe3O4 b, Al + HCl → AlCl3 + H2 c, Al2(SO4)3 + NaOH → Al(OH)3 + Na2SO4 d, CaCO3 + HCl → CaCl2 + CO2 + H2O |

Áp dụng các bước lập phương trình hoá học, cân bằng phương trình.

a, 6Fe + 4O2 → 2Fe3O4
b, 2Al + 6HCl → 2AlCl3 + 3H2
c, Al2(SO4)3 + 6NaOH → 2Al(OH)3 + 3Na2SO4
d, CaCO3 + 2HCl → CaCl2 + CO2 + H2O
Câu hỏi trang 27
|
Câu hỏi 1: Sơ đồ của phản ứng hoá học khác với phương trình hoá học ở điểm nàoCâu hỏi Nêu ý nghĩa của phương trình hoá học. |

dựa vào khái niệm về phương trình hoá học và phản ứng hoá học

- Sơ đồ của phản ứng hoá học khác với phương trình hoá học là trong PTHH cho biết trong phản ứng hoá học, lượng các chất tham gia và lượng các chất sản phẩm tuân theo một tỉ lệ xác định.
- Ý nghĩa của phương trình hoá học: cho biết tỉ lệ (số mol,số phân tử,...) các chất trong phản ứng.
| Câu hỏi 2: Lập phương trình hoá học và xác định tỉ lệ số phân tử của các chất trong sơ đồ phản ứng hoá học sau: Na2CO3 + Ba(OH)2 →BaCO3 + NaOH |
Phương pháp giải: dựa và các bước lập phương trình hoá học đã học

: Áp dụng các bước lập phương trình hoá học, cân bằng phương trình.
PTHH: Na2CO3 + Ba(OH)2 → BaCO3 + 2NaOH
Tỉ lệ số phân tử chất trong phản ứng là:
Số phân tử Na2CO3 : số phân tử Ba(OH)2 : số phân tử BaCO3 : số phân tử NaOH = 1 : 1 : 1 : 2
| Câu hỏi 3: Giả thiết trong không khí sắt tác dụng với oxygen tạo thành gỉ sắt (Fe2O3). Từ 5,6 gam sắt có thể tạo ra tối đa bao nhiêu gam gỉ sắt. |

Dựa vào công thức tính số mol của nguyên tử/ phân tử, các bước lập phương trình hoá học và cân bằng phương trình hoá học

Phương trình:
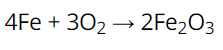
Ta có tỉ lệ:
Số mol Fe : số mol O2 : số mol Fe2O3 = 4 : 3 : 2
Từ tỉ lệ số mol ta xác định được tỉ lệ khối lượng các chất:
Khối lượng Fe : khối lượng O2 : khối lượng Fe2O3 = (56 x 4) : (32 x 3) : (160 x 2) = 7 : 3 : 10
Vậy cứ 7 gam Fe phản ứng hết với 3 gam O2 tạo ra 10 gam Fe2O3
Do đó, từ 5,6 gam Fe có thể tạo ra tối đa (5,6 x 10) : 7 = 8 gam gỉ sắt
