So sánh tính chất oxi hóa của các đơn chất F2, Cl2, Br2, I2. Dẫn ra những phương trình hóa học của phản ứng nếu có.
Hướng dẫn giải:
a) Tính oxi hóa giảm dần từ F2 đến I2
- Flo là phi kim mạnh nhất, oxi hóa được tất cả các kim loại kế cả vàng và platin . Clo, Brom và Iot tác dụng với một số kim loại.
- Phản ứng với hidro
H2 + F2\(\overset{-250^{\circ}C}{\rightarrow}\) 2HF
H2 +Cl2 \(\overset{as}{\rightarrow}\) 2HCl
H2 + Br2\(\overset{dun nong}{\rightarrow}\) 2HBr
Advertisements (Quảng cáo)
H2 +I2 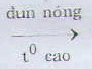 2HI
2HI
- Halogen đứng trước đẩy halogen đứng sau ra khỏi muối của chúng:
Cl2 + 2NaBr → 2NaCl + Br2
b) Tính khử của axit tăng dần theo chiều: HF < HCl < HBr < HI
- Chỉ có thể oxi hóa F bằng dòng điện. Còn ion Cl- , Br-, I- đều có thể bị oxi hóa khi tác dụng với chất oxi hóa mạnh.
- HF hoàn toàn không thể hiện tính khử. HCl chỉ thể hiện tính khử khi tác dụng với những chất oxi hóa mạnh. Axit sunfuric đặc bị HBr khử đến SO2 và bị HI khử đến H2S
8\(\overset{-1}{HI}\) + \(\overset{+6}{H_{2}SO_{4}}\) → 4\(\overset{0}{I_{2}}\)+\(H_{2}S^{-2}\)+ 4H2O
2HBr +H2SO4 đặc →\(\overset{0}{Br_{2}}\) + \(\overset{+4}{SO_{2}}\)+2H2O
