Câu hỏi/bài tập:
Hỗn hợp X gồm SO2 và O2 có tỉ khối so với H2 bằng 24. Nung nóng X trong bình kín chứa xúc tác V2O5, thu được hỗn hợp khí Y có tỉ khối so với H2 bằng 30. Viết phương trình hoá học và tính hiệu suất của phản ứng oxi hóa SO2 thành SO3.

Sử dụng công thức: \({\rm{H}} = \frac{{{{\rm{n}}_{{\rm{S}}{{\rm{O}}_{\rm{2}}}{\rm{ p/u}}}}}}{{{{\rm{n}}_{{\rm{S}}{{\rm{O}}_2}{\rm{ bd}}}}}} \times 100\% \)

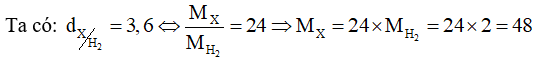
Advertisements (Quảng cáo)
\( \Leftrightarrow \frac{{64{{\rm{n}}_{{\rm{S}}{{\rm{O}}_{\rm{2}}}}} + 32{{\rm{n}}_{{{\rm{O}}_{\rm{2}}}}}}}{{{{\rm{n}}_{{\rm{S}}{{\rm{O}}_{\rm{2}}}}} + {{\rm{n}}_{{{\rm{O}}_{\rm{2}}}}}}} = 48 \Rightarrow 16{{\rm{n}}_{{\rm{S}}{{\rm{O}}_{\rm{2}}}}} = 16{{\rm{n}}_{{{\rm{O}}_{\rm{2}}}}} \Leftrightarrow \frac{{{{\rm{n}}_{{\rm{S}}{{\rm{O}}_{\rm{2}}}}}}}{{{{\rm{n}}_{{{\rm{O}}_{\rm{2}}}}}}} = \frac{1}{1}\)
Hỗn hợp X gồm SO2 và O2 có tỉ lệ mol tương ứng là 1 : 1.
Chọn \({{\rm{n}}_{{\rm{S}}{{\rm{O}}_{\rm{2}}}}} = 1{\rm{ (mol)}};{\rm{ }}{{\rm{n}}_{{{\rm{O}}_{\rm{2}}}}} = 1{\rm{ }}({\rm{mol}})\)
\( \Rightarrow \)\({{\rm{m}}_{\rm{X}}}{\rm{ = }}{{\rm{m}}_{{\rm{S}}{{\rm{O}}_{\rm{2}}}}} + {{\rm{m}}_{{{\rm{O}}_{\rm{2}}}}} = 1 \times 64 + 1 \times 32 = 96{\rm{ }}({\rm{gam}})\)
Bảo toàn khối lượng, ta có:

