Câu hỏi trang 100 Mở đầu
C2H5Cl là một dẫn xuất halogen. Dẫn xuất halogen có những tính chất và ứng dụng gì?

Dẫn xuất halogen có nhiều ứng dụng trong đời sống, công nghiệp hóa chất và y học.

- Tính chất:
+ Tính chất vật lí: Ở điều kiện thường, các dẫn xuất halogen có phân tử khối nhỏ ở thể khí. Các dẫn xuất halogen có phân tử khối lớn hơn thưởng ở thể lỏng hoặc ở thể rắn. Phần lớn dẫn xuất halogen nặng hơn nước và hầu như không tan trong nước, tan tốt trong dung môi hữu cơ kém phân cực như hydrocarbon, ether,...
+ Tính chất hóa học: Do halogen có độ âm điện lớn hơn carbon nên cặp electron dùng chung trong liên kết C-X (X là F, Cl, Br và I) bị hút về phía nguyên tử halogen, làm cho nguyên tử halogen mang một phần điện tích âm, nguyên tử carbon mang một phần diện tích dương và liên kết C−X phân cực. Nhờ có sự phân cực của liên kết C−X, dẫn xuất halogen dễ tham gia vào nhiều phản ứng hoá học. Hai loại phân ứng hoá học quan trọng của dẫn xuất halogen là phản ứng thể nguyên tử halogen và phản ứng tách hydrogen halide.
- Ứng dụng:
+ Làm dung môi, làm nguyên liệu: chloroform (CHCl3), carbon tetrachloride (CCl4),…
+ Làm chất gây mê, giảm đau: chloroform (CHCl3), ethyl chlordide,…
+ Thuốc trừ sâu: 2,4 – D, 2,4,5 – T,…
+ Chất dùng trong công nghệ làm lạnh: chlorofluorocarbon (CFC), hydrofluorocarbon (HFC).
Câu hỏi trang 100 Câu hỏi 1
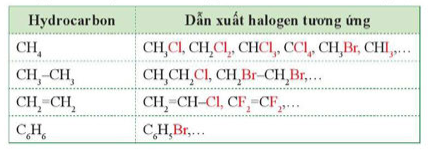
Có thể tạo được những dẫn xuất halogen nào từ các hydrocarbon sau: CH4, CH3–CH3 CH2=CH2 và C6H6?

Khi thay thế nguyên tử hydrogen của phân tử hydrocarbon bằng nguyên tử halogen được dẫn xuất halogen của hydrocarbon (gọi tắt là dẫn xuất halogen).

Câu hỏi trang 101 Câu hỏi 2
Trong các đồng phân cấu tạo có cùng công thức phân tử là C4H9Cl, hãy chỉ ra đồng phân mạch carbon, đồng phân vị trí nhóm chức.

Công thức cấu tạo biểu diễn thứ tự và cách thức liên kết (liên kết đơn, liên kết đôi, liên kết ba) giữa các nguyên tử trong phân tử.
Những hợp chất khác nhau nhưng có cùng công thức phân tử được gọi là các chất đồng phân của nhau.

Các đồng phân cấu tạo có cùng công thức phân tử là C4H9Cl:
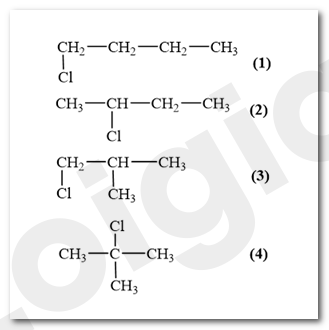
Đồng phân mạch carbon: (1) và (3); (2) và (4).
Đồng phân vị trí nhóm chức. (1) và (2); (3) và (4).
Câu hỏi trang 102 Luyện tập 1
Viết công thức cấu tạo và gọi tên thay thế của các hợp chất có cùng công thức phân tử là C5H11Cl.

- Công thức cấu tạo biểu diễn thứ tự và cách thức liên kết (liên kết đơn, liên kết đôi, liên kết ba) giữa các nguyên tử trong phân tử.
- Danh pháp thay thế: Trong phân tử dẫn xuất halogen, các nguyên tử halogen được coi là nhóm thế halogeno (fluoro, chloro, bromo, iodo) gắn vào mạch chính của hydrocarbon. Đánh số thứ tự chỉ vị trí nguyên tử carbon mạch chính sao cho tổng số của số chỉ vị trí của các nhóm thể là nhỏ nhất. Đối với dẫn xuất halogen không no, ưu tiên đánh số từ phía đầu mạch gần liên kết bội hơn.Tên thay thế của các dẫn xuất halogen được gọi như sau:


Các hợp chất có cùng công thức phân tử là C5H11Cl:

Câu hỏi trang 102 Luyện tập 2
Cho các chất có công thức: CH3F, CH3Cl, CH3Br, CH3I và nhiệt độ sôi của chúng (không theo thứ tự) là 42,4 °C, 3,6 °C, -24,2 °C, –78,4 °C. Hãy dự đoán nhiệt độ sôi tương ứng với mỗi chất trên. Giải thích.

Với các dẫn xuất halogen cùng gốc alkyl nhiệt độ sôi tăng theo chiều tăng của nguyên tử khối halogen.

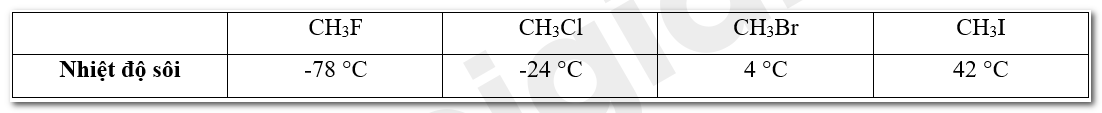
Giải thích: Với các dẫn xuất halogen cùng gốc alkyl nhiệt độ sôi tăng theo chiều tăng của nguyên tử khối halogen.
Câu hỏi trang 102 Câu hỏi 3
Dựa vào giá trị độ âm điện của carbon, hydrogen và chlorine, nhận xét về sự phân cực của các liên kết C-C, C-H và C-Cl.

Hiệu độ âm điện giữa hai nguyên tử càng lớn, liên kết càng phân cực.

Độ âm điện của các nguyên tố C, H, Cl có giá trị lần lượt là: 2,55; 2,20; 3,16.
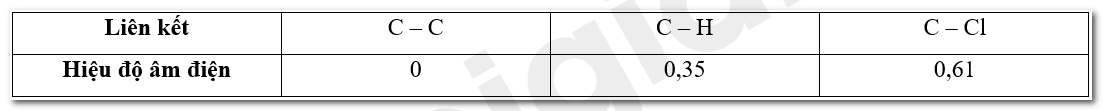
Nhận xét: Độ phân cực tăng dần từ liên kết C – C, C – H, C – Cl.
Câu hỏi trang 103 Luyện tập 3
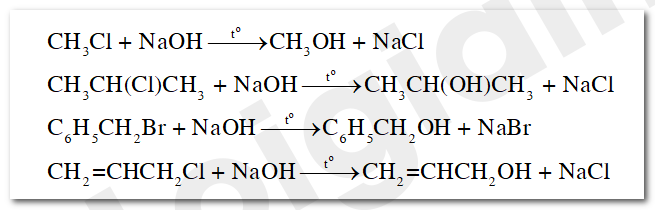
Viết phương trình hoá học của phản ứng xảy ra khi đun các hợp chất sau với dung dịch sodium hydroxide: CH3Cl, CH3CHClCH3, C6H5CH2Br và CH2=CHCH2Cl.

Đun dẫn xuất halogen (R-X, trong đó, X liên kết với nguyên tử C no) với dung dịch kiềm, thu được alcohol (R-OH).
Với X là các halogen Cl, Br, I. Phản ứng này còn được gọi là phản ứng thuỷ phân dẫn xuất halogen.

Câu hỏi trang 103 Thực hành
Quan sát video thí nghiệm thuỷ phân dẫn xuất halogen, mô tả hiện tượng xảy ra. Giải thích.

Đun dẫn xuất halogen (R-X, trong đó, X liên kết với nguyên tử C no) với dung dịch kiềm, thu được alcohol (R-OH).
Với X là các halogen Cl, Br, I. Phản ứng này còn được gọi là phản ứng thuỷ phân dẫn xuất halogen.

- Hiện tượng: Xuất hiện kết tủa AgX. (Với X là Cl, Br, I)
- Giải thích: + Phản ứng thủy phân dẫn xuất halogen, tạo ra ion X-.
+ Sau đó nhỏ thêm dung dịch AgNO3, ion X- kết hợp với ion Ag+ tạo kết tủa AgX.
X- + Ag+ → AgX↓
Câu hỏi trang 103 Câu hỏi 4
Trong thí nghiệm Thuỷ phân dẫn xuất halogen, cho biết:
a) Cho nước vào ống nghiệm chứa dẫn xuất halogen sau đó thử phần nước bằng dung dich silver nitrate nhằm mục đích gì?
b) Vì sao phải acid hoá dung dịch sau khi thuỷ phân bằng dung dịch HNO3? Có thể thay dung dịch HNO3 bằng dung dịch H2SO4 hay HCl được không? Vì sao?

Advertisements (Quảng cáo)
a) ion X- kết hợp với ion Ag+ tạo kết tủa AgX.
b) Acid hóa tạo môi trường acid. Ag2SO4 và AgCl là kết tủa.

a) - Cho nước vào ống nghiệm chứa dẫn xuất halogen nhằm mục đích rửa ion halide (X-)
- Thử phần nước bằng dung dich silver nitrate nhằm mục đích kiểm tra phần nước có ion halide (X-) hay không.
b) - Acid hóa dung dịch sau khi thuỷ phân bằng dung dịch HNO3 để tránh trường hợp dư base, sinh ra kết tủa Ag2O:
AgNO3 + NaOH → AgOH + NaNO3
2AgOH → Ag2O + H2O
- Không thể thay dung dịch HNO3 bằng dung dịch H2SO4 hay HCl vì AgNO3 có thể phản ứng với H2SO4 hay HCl tạo kết tủa Ag2SO4 hay AgCl làm sai kết quả thí nghiệm.
AgNO3 + HCl → AgCl↓ + HNO3
2AgNO3 + H2SO4 → Ag2SO4↓+ 2HNO3
Câu hỏi trang 103 Luyện tập 4
Viết phương trình hoá học của phản ứng xảy ra khi đun các dẫn xuất halogen sau với dung dich potassium hydroxide trong ethanol.
a) 2-chloropropane
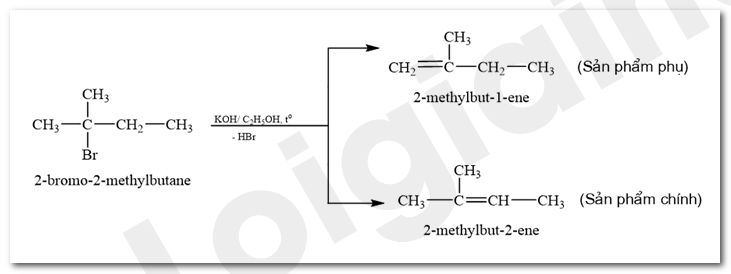
b) 2-bromo-2-methylbutane
Gọi tên các sản phẩm sinh ra.

Quy tắc Zaitsev: Trong phản ứng tách hydrogen halide ra khỏi dẫn xuất halogen, ưu tiên tách nguyên tử halogen cùng nguyên tử hydrogen ở nguyên tử carbon bên cạnh có bậc cao hơn.

a) 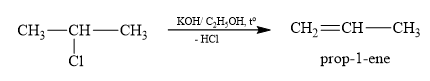
b)
Câu hỏi trang 104 Câu hỏi 5
Trình bày một số ứng dụng trong thực tiễn của dẫn xuất halogen.

Ứng dụng: làm dung môi, làm nguyên liệu; làm chất gây mê, giảm đau; thuốc trừ sâu; chất dùng trong công nghệ làm lạnh…

Ứng dụng:
+ Làm dung môi, làm nguyên liệu: chloroform (CHCl3), carbon tetrachloride (CCl4),…
+ Làm chất gây mê, giảm đau: chloroform (CHCl3), ethyl chlordide,…
+ Thuốc trừ sâu: 2,4 – D, 2,4,5 – T,…
+ Chất dùng trong công nghệ làm lạnh: chlorofluorocarbon (CFC), hydrofluorocarbon (HFC).
Câu hỏi trang 105 Câu hỏi 6
Giải thích vì sao không nên lạm dụng chất diệt cỏ, chất kích thích tăng trưởng 2,4-D và 2,4,5-T.

2,4-D và 2,4,5-T độc, có hại cho môi trường và con người.

Không nên lạm dụng chất diệt cỏ, chất kích thích tăng trưởng 2,4-D và 2,4,5-T vì
+ 2,4-D dùng làm thuốc trừ cỏ có chứa một lượng chất Chlorophenol không được tổng hợp hết gọi là phenol tự do. Chất Chlorophenol có mùi hôi nồng rất khó chịu, là nguyên nhân chính tạo nên mùi hôi đặc biệt của thuốc trừ cỏ 2,4-D. Chlorophenol có nhiều ảnh hưởng không tốt đối với sức khỏe con người và môi trường sống do trong tự nhiên, Chlorophenol tồn tại tương đối lâu và có thể chuyển hóa thành chất Dioxin.
+ Gây kháng thuốc ở cỏ dại. Do quá mức sử dụng, cỏ dại có thể phát triển khả năng kháng lại các chất diệt cỏ này, khiến thuốc kém hiệu quả.
Câu hỏi trang 105 Câu hỏi 7
Vì sao các hợp chất CFC hiện nay không còn được sử dụng trong công nghệ làm lạnh?

CFC thải ra môi trường không khí, có thể khuếch tán đến tầng đối lưu và dưới tác động của ánh sáng mặt trời, tạo ra các gốc tự do, dẫn đến việc phá huỷ tầng ozone và gây ra hiệu ứng nhà kính.

Khi thải các hợp chất CFC ra môi trường không khí, chúng có thể khuếch tán đến tầng đối lưu và dưới tác động của ánh sáng mặt trời, tạo ra các gốc tự do, dẫn đến việc phá huỷ tầng ozone và gây ra hiệu ứng nhà kính.Do đó để bảo vệ tầng ozone, hiện nay trong công nghệ làm lạnh, người ta đã không còn sử dụng các hợp chất CFC.
Bài tập Bài 1
Cho các dẫn xuất halogen có công thức cấu tạo sau: CH3Cl, CH3CH2Cl, C6H5Br, CHCl3, và CH2BrCH2Br.
a) Gọi tên các chất trên theo danh pháp thay thế.
b) Viết phương trình hoá học của phản ứng điều chế các chất trên từ hydrocarbon tương ứng.

a) Tên thay thế của các dẫn xuất halogen được gọi như sau:

b) Sử dụng phản ứng thế halogen vào alkane, benzene và phản ứng cộng của alkene để viết phản ứng điều chế.

a)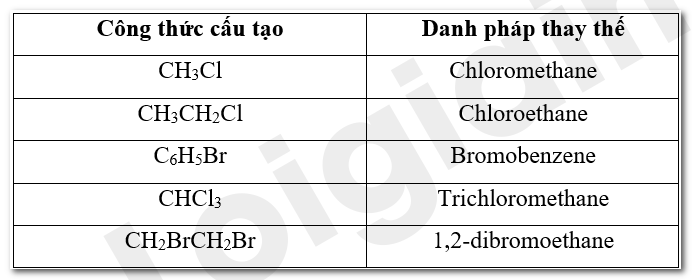
b)
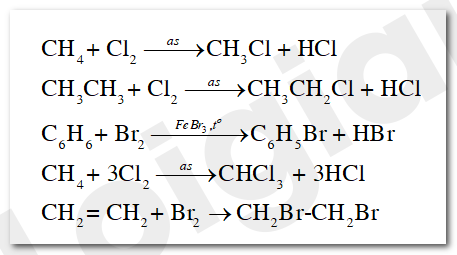
Bài tập Bài 2
PVC là một trong những polymer được ứng dụng nhiều trong đời sống và sản xuất. Hoàn thành sơ đồ phản ứng tổng hợp PVC dưới đây.
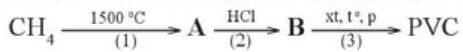

A là acetylene (CH≡CH), B là vinyl chloride (CHCl=CH2)

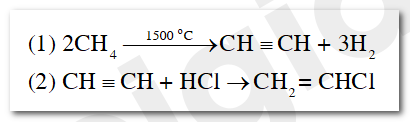
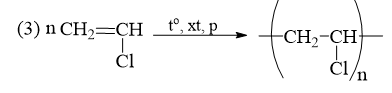
Bài tập Bài 3
Ethyl chloride hóa lỏng được sử dụng làm thuốc xịt có tác dụng giảm đau tạm thời khi chơi thể thao.
a) Cho:
Khi xịt thuốc vào chỗ đau thì người ta cảm giác nóng hay lạnh?
b) Viết phương trình hóa học của phản ứng điều chế ethyl chloride từ ethane.

a) \({\Delta _{\rm{r}}}{\rm{H}}_{{\rm{298}}}^{\rm{0}}\)> 0: Phản ứng thu nhiệt.
b) Sử dụng phản ứng thế halogen của alkane để điều chế ethyl chloride từ ethane.

a) Vì phản ứng có \({\Delta _{\rm{r}}}{\rm{H}}_{{\rm{298}}}^{\rm{0}}\)> 0 nên ethyl chloride hóa lỏng là phản ứng thu nhiệt. Do đó khi xịt ethyl chloride vào chỗ đau thì người ta cảm giác lạnh.
b)
