Người ta có thể điều chế brom bằng cách cho axit sunfuric đặc tác dụng với hỗn hợp rắn KBr và MnO2.
a) Viết phương trình hóa học và cho biết vai trò của từng chất trong phản ứng.
b) Tính khối lượng của mỗi chất cần dùng đề điều chế 32g brom.

a) Phương trình phản ứng xảy ra:
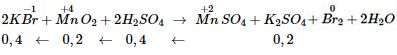
Advertisements (Quảng cáo)
KBr là chất khử; MnO2 là chất oxi hóa, H2SO4 là môi trường.
b) Tính khối lượng mỗi chất đem dùng.
\({n_{B{r_2}}} = {{32} \over {160}} = 0,2\,\,\left( {mol} \right)\)
Theo phương trình phản ứng ta có:
\(\eqalign{ & {n_{KBr}} = 0,4\,\left( {mol} \right) \cr&\Rightarrow {m_{KBr}} = 0,4.119 = 47,6\,\left( {gam} \right) \cr & {n_{Mn{O_2}}} = 0,2\,\left( {mol} \right) \cr&\Rightarrow {m_{Mn{O_2}}} = 0,2.87 = 17,4\,\left( {gam} \right) \cr & {n_{{H_2}S{O_4}}} = 0,4\,\left( {mol} \right) \cr&\Rightarrow {m_{{H_2}S{O_4}}} = 0,4.98 = 39,2\,\left( {gam} \right) \cr} \)
