Câu hỏi/bài tập:
Hỗn hợp X gồm N2 và H2 có tỉ lệ mol tương ứng là 1 : 4. Nung nóng X trong bình kín ở nhiệt độ khoảng 450 °C có bột Fe xúc tác, thu được hỗn hợp khí Y có tỉ khối so với H2 bằng 4. Hiệu suất của phản ứng tổng hợp NH3 là
A. 20%. B. 25%. C. 30%. D. 10%.

Sử dụng công thức: \({\rm{H\% }} = \frac{{{{\rm{n}}_{{\rm{sp(tt)}}}}}}{{{{\rm{n}}_{{\rm{sp(lt)}}}}}} \times 100\% \)

Hỗn hợp X gồm N2 và H2 có tỉ lệ mol tương ứng là 1 : 4.
Chọn \({{\rm{n}}_{{{\rm{N}}_{\rm{2}}}}} = 1{\rm{ (mol)}};{\rm{ }}{{\rm{n}}_{{{\rm{H}}_{\rm{2}}}}} = 4{\rm{ }}({\rm{mol}})\)
Gọi x (mol) là số mol N2 phản ứng.
Xét cân bằng:
Advertisements (Quảng cáo)
\({{\rm{N}}_2}\left( g \right){\rm{ }} + {\rm{ }}3{{\rm{H}}_2}\left( g \right){\rm{ }} \mathbin{\lower.3ex\hbox{$\buildrel\textstyle\rightarrow\over{\smash{\leftarrow}\vphantom{_{\vbox to.5ex{\vss}}}}$}} {\rm{ }}2{\rm{N}}{{\rm{H}}_3}\left( g \right){\rm{ }}\)
Ban đầu (mol): 1 4 0
Phản ứng (mol): x → 3x → 2x
Cân bằng (mol): 1 - x 4 – 3x 2x
\( \Rightarrow \)Số mol khí sau phản ứng: \({\rm{(1}} - {\rm{x}}){\rm{ + (4 — 3x) + 2x = 5}} - {\rm{2x (mol)}}\)
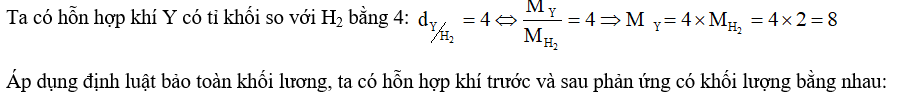
\(\begin{array}{l}{\rm{ }}{{\rm{m}}_{\rm{X}}} = {{\rm{m}}_{\rm{Y}}}\\ \Leftrightarrow {{\rm{m}}_{{{\rm{N}}_{\rm{2}}}}} + {{\rm{m}}_{{{\rm{H}}_{\rm{2}}}}} = {{\rm{m}}_{\rm{Y}}}\\ \Leftrightarrow 1 \times 28 + 4 \times 2 = 8 \times (5 - 2{\rm{x}})\\ \Rightarrow {\rm{x}} = 0,25{\rm{ (mol)}}\end{array}\)
\(\begin{array}{l} \Rightarrow {{\rm{n}}_{{{\rm{N}}_{\rm{2}}}{\rm{p/u}}}} = {\rm{x}} = 0,25{\rm{ }}({\rm{mol}})\\ \Rightarrow {\rm{H}} = \frac{{{{\rm{n}}_{{{\rm{N}}_{\rm{2}}}{\rm{p/u}}}}}}{{{{\rm{n}}_{{{\rm{N}}_{\rm{2}}}{\rm{bd}}}}}} \times 100\% = \frac{{0,25}}{1} \times 100\% = 25\% \end{array}\)
→ Chọn B.
