Giải chi tiết Câu hỏi trang 98 SGK Hóa 12 Cánh diều - Bài 14. Tính chất hóa học của kim loại.
Dựa vào thế điện cực chuẩn của kim loại trong Bảng 10.1, giải thích vì sao Cu và Ag không phản ứng với dung dịch hydrochloric acid 1M.

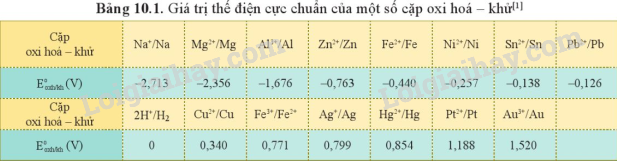
Advertisements (Quảng cáo)
Dựa vào thế điện cực chuẩn của Cu, Ag và so sánh với thế điện cực chuẩn của H+. Giá trị thế điện cực chuẩn \(E_{M + /M}^o\)< 0 có thể khử được ion H+.

Vì \(E_{C{u^{2 + }}/Cu}^o = 0,34V;E_{A{g^ + }/Ag}^o = 0,799V\)> \(E_{{H^ + }/H}^o\)nên không khử được ion H+. Do đó Cu, Ag không tác dụng với dung dịch hydrochloric acid.
