I. TÍNH CHẤT HÓA HỌC CỦA PHI KIM
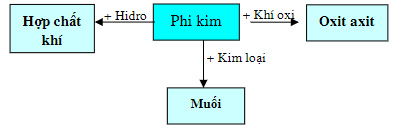
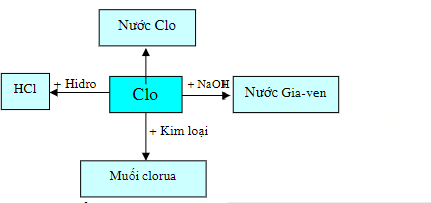
1. Tính chất hóa học của clo
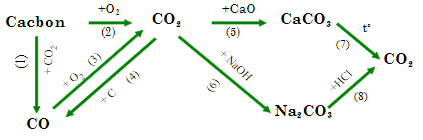
2. Tính chất hóa học của cacbon và hợp chất của cacbon
II. BẢNG TUẦN HOÀN CÁC NGUYÊN TỐ HÓA HỌC
1. Cấu tạo bảng tuần hoàn
Ô: Ô nguyên tố cho biết số hiệu nguyên tử, kí hiệu hóa học, tên nguyên tố, nguyên tử khối của nguyên tố đó.
Chu kì: là dãy các nguyên tố mà nguyên tử của chúng có cùng số lớp electron và được xếp theo chiều điện tích hạt nhân tăng dần.
Advertisements (Quảng cáo)
Nhóm: gồm các nguyên tố mà nguyên tử của chúng có sô electron lớp ngoài cùng bằng nhau, do đó có tính chắt tương tự nhau.
2. Sự biến đổi tính chất của các nguyên tố trong bảng tuần hoàn
Trong chu kì:
Số e lớp ngoài cùng của nguyên tử tăng dần từ 1 đến 8 electron.
Tính kim loại của các nguyên tố giảm dần, đồng thời tính phi kim của các nguyên tố tăng dần.
Trong nhóm: Trong một nhóm, khi đi từ trên xuống dưới theo chiều tăng của điện tích hạt nhân. Số lớp electron trong nguyên tử tăng dần, tính kim loại của các nguyên tố tăng dần, đồng thời tính phi kim của các nguyên tố giảm dần.
3. Ý nghĩa của bảng tuần hoàn:
- Biết vị trí của nguyên tô ta có thể suy đoán cấu tạo nguyên tử và tính chất của nguyên tố.
- Biết cấu tạo nguyên tử của nguyên tố có thể suy đoán vị trí và tính chất nguyên tố đó.
