Điiot pentaoxit \(\left( {{I_2}{O_5}} \right)\) tác dụng với cacbon monooxit tạo ra cacbon ddiooxit và iot.
a) Lập phương trình hóa học của phản ứng oxi hóa – khử trên.
b) Khi cho 1 lít hỗn hợp khí có chứa CO và \(C{O_2}\) tham gia phản ứng thì khối lượng điiot pentaoxit bị khử là 0,50g. Tính thành phần phần trăm về thể tích của CO trong hỗn hợp khí. Biết rằng ở điều kiện thí nghiệm, thể tích mol của chất khí V = 24 lít.

a) Phương trình phản ứng: \({I_2}\mathop {{O_5}}\limits^{ + 5} + \mathop C\limits^{ + 2} O\,\, \to \,\,\mathop C\limits^{ + 4} {O_2} + \mathop {{I_2}}\limits^0 \)
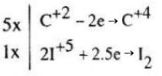
\( {I_2}{O_5} + 5CO\,\, \to \,\,5C{O_2} + {I_2}. \)
Advertisements (Quảng cáo)
b) Tính phần trăm về thể tích CO trong hỗn hợp khí:
Gọi x là số mol của CO, y là số mol của CO2 có trong 1 lít hỗn hợp.
Ta có \(x + y = {1 \over {24}}\,\,\,\left( 1 \right)\)
Chỉ có CO tham gia phản ứng. Theo phương trình phản ứng:
\({n_{CO}} = 5{n_{{I_2}{O_5}}} = {{5.0,5} \over {334}} = x\)
Ta có: \(\% {V_{CO}} = \% {n_{CO}} = {{2,5} \over {334}}.24.100 \approx 18\% .\)
