5. Cho một lượng hỗn hợp Mg – Al tác dụng với dung dịch HCl dư thu được 8,96 lít H2. Mặt khác, cho lượng hỗn hợp như trên tác dụng với dung dịch NaOH dư thì thu được 6,72 lít H2. Các thể tích khí đều đo ở đktc.
Tính khối lượng của mỗi kim loại có trong lượng hỗn hợp đã dùng.
Hướng dẫn.
nH2 ở (1) và (2) = 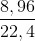 = 0,4 (mol); nH2 ở (3) =
= 0,4 (mol); nH2 ở (3) = 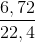 = 0,3 (mol)
= 0,3 (mol)
2Al + 6HCl → 2AlCl3 + 3H2 ↑ (1)
0,3 0,3 (mol)
Advertisements (Quảng cáo)
Mg + 2HCl → MgCl2 + H2 ↑ (2)
0,1 0,1 (mol)
2Al + 2NaOH + 2H2O → 2NaAlO2 + 3H2↑ (3)
0,2 0,3 (mol)
=> mMg = 21.0,1 = 2,4 (gam); mAl = 27.0,2 = 5,4 (gam).
