Câu hỏi trang 15 Mở đầu
Trả lời câu hỏi Mở đầu trang 15
Cùng với chất béo và protein, carbohydrate là một trong ba nguồn cung cấp dinh dưỡng cấn thiết cho cơ thể.
Carbohydrate là gì? Chúng có cấu tạo, tính chất hoá học như thế nào và được ứng dụng ra sao trong đời sống?

Nêu khái niệm, cấu tạo, tính chất hóa học và ứng dụng của carbohydrate.

- Carbohydrate là những hợp chất hữu cơ tạp chức, thường có công thức chung là Cn(H2O)m.
- Cấu tạo:
+ Trong phân tử carbohydrate có nhiều loại nhóm chức (tạp chức).
+ Cấu trúc phân tử dạng mạch hở hoặc mạch vòng.
- Tính chất hóa học: phụ thuộc vào các loại nhóm chức trong phân tử carbohydrate, ví dụ:
+ Tính chất của polyalcohol.
+ Tính chất của aldehyde.
+ Phản ứng thủy phân của disaccharide, polysaccharide.
- Ứng dụng:
+ Glucose, fructose được sử dụng nhiều trong lĩnh vực y tế, công nghiệp thực phẩm.
+ Saccharose được sử dụng nhiều trong công nghiệp thực phẩm như chế biến nước giải khát, siro, bánh mứt, kẹo,... và trong sản xuất dược phẩm.
+ Maltose cũng được sử dụng phổ biến trong sản xuất bánh kẹo và sản xuất bia.
+ Tinh bột dùng làm lương thực,... Cellulose dùng để sản xuất sơn mài, thuốc súng không khói, tơ visco, giấy bóng kính,...
Câu hỏi trang 15 Tranh luận
Trả lời câu hỏi Thảo luận trang 15
Dựa vào đặc điểm nào để phân loại carbohydrate?

Carbohydrate được phân thành 3 loại: monosaccharide, disaccharide và polysaccharide.


Dựa vào phản ứng thủy phân carbohydrate để phân loại carbohydrate thành:
+ Monosaccharide: Là nhóm carbohydrate đơn giản nhất, không bị thuỷ phân. Ví dụ: glucose, fructose.
+ Disaccharide: Là nhóm carbohydrate phức tạp hơn, khi bị thuỷ phân hoàn toàn, mỗi phân tử tạo thành hai phân tử monosaccharide. Ví dụ: saccharose, maltose.
+ Polysaccharide: Là nhóm carbohydrate phức tạp nhất, khi bị thuỷ phân hoàn toàn, mỗi phân tử tạo thành nhiều phân tử monosaccharide. Ví dụ: tinh bột, cellulose.
Câu hỏi trang 16
Trả lời câu hỏi Luyện tập trang 16
Tại sao mật ong ngọt hơn nhiều các loại trái cây chín?

Fructose là chất rắn, dễ tan trong nước, có vị ngọt hơn glucose.
Glucose có nhiều trong trái cây chín. Fructose có nhiều trong mật ong.

Trái cây chín chứa nhiều glucose, mật ong chứa nhiều fructose mà fructose có vị ngọt hơn glucose nên mật ong ngọt hơn nhiều các loại trái cây chín.
Câu hỏi trang 17 Tranh luận1
Trả lời câu hỏi Thảo luận 1 trang 17
So sánh đặc điểm cấu tạo của phân tử glucose và fructose ở dạng mạch hở.

Glucose và fructose đều có công thức phân tử là C6H12O6.
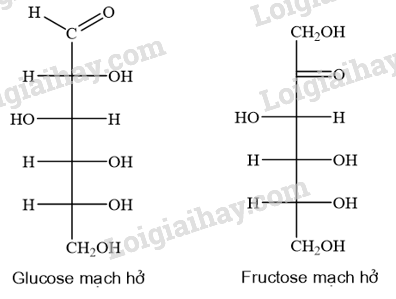

- Giống: Phân tử glucose và fructose đều là các polyalcohol (có nhiều nhóm –OH).
- Khác:
+ Phân tử glucose có một nhóm aldehyde (-CHO).
+ Phân tử fructose có một nhóm ketone (-C=O)
Câu hỏi trang 17 Tranh luận2
Trả lời câu hỏi Thảo luận 2 trang 17
Tiến hành Thí nghiệm 1, quan sát hiện tượng xảy ra. Nhận xét và rút ra kết luận.

Polyalcohol có các nhóm –OH liền kề làm tan kết tủa Cu(OH)2.

- Hiện tượng:
+ Khi nhỏ dung dịch CuSO4 vào dung dịch NaOH, xuất hiện kết tủa màu xanh lam là Cu(OH)2. \({\rm{CuS}}{{\rm{O}}_{\rm{4}}} + 2{\rm{NaOH}} \to {\rm{Cu(OH}}{{\rm{)}}_{\rm{2}}} + {\rm{N}}{{\rm{a}}_{\rm{2}}}{\rm{S}}{{\rm{O}}_{\rm{4}}}\)
+ Nhỏ dung dịch glucose vào ống nghiệm chứa kết tủa, lắc đều, kết tủa tan. Phản ứng xảy ra như sau:
\(2{{\rm{C}}_{\rm{6}}}{{\rm{H}}_{{\rm{12}}}}{{\rm{O}}_{\rm{6}}} + {\rm{Cu(OH}}{{\rm{)}}_{\rm{2}}} \to {{\rm{(}}{{\rm{C}}_{\rm{6}}}{{\rm{H}}_{{\rm{11}}}}{{\rm{O}}_{\rm{6}}}{\rm{)}}_{\rm{2}}}{\rm{Cu}} + 2{{\rm{H}}_{\rm{2}}}{\rm{O}}\)
- Nhận xét: Glucose có khả năng hòa tan Cu(OH)2 trong môi trường base ở nhiệt độ thường.
- Kết luận: Trong phân tử glucose có các nhóm –OH kề nhau, do đó glucose có tính chất của polyalcohol (hòa tan Cu(OH)2 ở nhiệt độ thường).
Câu hỏi trang 17 Tranh luận3
Trả lời câu hỏi Thảo luận 3 trang 17
Tiến hành Thí nghiệm 2 theo hướng dẫn. Nhận xét và giải thích hiện tượng quan sát được sau thí nghiệm.

Aldehyde phản ứng với thuốc thử Tollens, tạo lớp bạc bám (phản ứng tráng bạc).
Phản ứng tráng bạc của aldehyde: 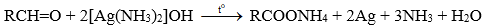

- Hiện tượng: có sự tạo thành kết tủa trắng bạc bám trên thành ống nghiệm.
- Nhận xét: Glucose phản ứng với thuốc thử Tollens tạo thành kết tủa trắng bạc.
- Giải thích hiện tượng: Glucose phản ứng với dung dịch AgNO3/NH3 tạo thành kết tủa Ag.
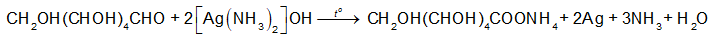
Câu hỏi trang 18 Tranh luận1
Trả lời câu hỏi Thảo luận 1 trang 18
Tiến hành Thí nghiệm 3 theo hướng dẫn. Nhận xét hiện tượng xảy ra trong thí nghiệm. Vì sao fructose cũng tham gia phản ứng này?

Phản ứng oxi hóa aldehyde: 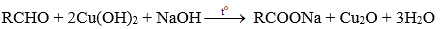
Frutose chuyển hóa thành glucose trong môi trường kiềm.

- Nhận xét:
+ Glucose hòa tan Cu(OH)2 ở nhiệt độ thường:
\(2{{\rm{C}}_{\rm{6}}}{{\rm{H}}_{{\rm{12}}}}{{\rm{O}}_{\rm{6}}} + {\rm{Cu(OH}}{{\rm{)}}_{\rm{2}}} \to {{\rm{(}}{{\rm{C}}_{\rm{6}}}{{\rm{H}}_{{\rm{11}}}}{{\rm{O}}_{\rm{6}}}{\rm{)}}_{\rm{2}}}{\rm{Cu}} + 2{{\rm{H}}_{\rm{2}}}{\rm{O}}\)
Advertisements (Quảng cáo)
+ Glucose phản ứng với Cu(OH)2 trong môi trường base khi đun nóng tạo kết tủa màu đỏ gạch.
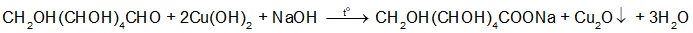
- Tuy fructose không có nhóm –CHO nhưng trong môi trường kiềm, frutose chuyển hóa thành glucose nên fructose vẫn tham gia phản ứng với Cu(OH)2 trong môi trường base khi đun nóng.
Câu hỏi trang 18 Tranh luận2
Trả lời câu hỏi Thảo luận 2 trang 18
Tiến hành Thí nghiệm 4 theo hướng dẫn. Nêu hiện tượng xảy ra. Giải thích.

Phản ứng oxi hóa aldehyde bằng nước bromine
\({\rm{RCH = O + B}}{{\rm{r}}_{\rm{2}}}{\rm{ + }}{{\rm{H}}_{\rm{2}}}{\rm{O}} \to {\rm{RCOOH + 2HBr}}\)

- Hiện tượng: nước bromine bị mất màu.
- Giải thích: Glucose có nhóm chức –CHO, bromine oxi hóa glucose, phản ứng xảy ra làm nước bromine mất màu.
\({\rm{C}}{{\rm{H}}_{\rm{2}}}{\rm{OH(CHOH}}{{\rm{)}}_{\rm{4}}}{\rm{CHO + B}}{{\rm{r}}_{\rm{2}}}{\rm{ + }}{{\rm{H}}_{\rm{2}}}{\rm{O}} \to {\rm{C}}{{\rm{H}}_{\rm{2}}}{\rm{OH(CHOH}}{{\rm{)}}_{\rm{4}}}{\rm{COOH + 2HBr}}\)
Câu hỏi trang 19 Tranh luận
Trả lời câu hỏi Thảo luận trang 19
Tại sao các phản ứng lên men lại cần nhiệt độ không quá cao?

Trong các phản ứng lên men, enzyme đóng vai trò là chất xúc tác. Bản chất của enzyme là protein, nhiệt độ cao làm biến tính enzyme, dẫn đến hoạt tính enzyme giảm mạnh.

Trong các phản ứng lên men, enzyme đóng vai trò là chất xúc tác. Cũng như nhiều phản ứng hóa học, tốc độ phản ứng có enzyme tăng khi nhiệt độ tăng. Tuy nhiên, ở nhiệt độ cao tốc độ phản ứng lại giảm do enzyme bị biến tính, thay đổi cấu trúc nên hoạt tính enzyme giảm mạnh. Vậy nên các các phản ứng lên men cần nhiệt độ không quá cao.
Câu hỏi trang 19 Vận dụng
Trả lời câu hỏi Vận dụng trang 19
Vì sao trong y học, người ta thường dùng glucose để trị chứng hạ đường huyết?

Glucose là chất dinh dưỡng có giá trị đối với con người do có thể hấp thụ trực tiếp vào máu để đi đến các mô và tế bào của cơ thể.

Trong chuyển hóa năng lượng, glucose là nguồn nguyên liệu quan trọng nhất để tạo ra năng lượng trong quá trình hô hấp tế bào. Khi thiếu glucose, các cơ quan không được cung cấp đủ năng lượng sẽ dẫn đến hoa mắt, chóng mặt, ớn lạnh, thậm chí là ngất, hiện tượng này gọi là hạ đường huyết. Do đó, trong y học, người ta thường dùng glucose để trị chứng hạ đường huyết.
Câu hỏi trang 20 Bài tập1
Trả lời câu hỏi Bài tập 1 trang 20
Có các phát biểu sau:
1) Glucose và fructose không tham gia phản ứng thuỷ phân.
2) Có thể phân biệt glucose và fructose bằng nước bromine.
3) Carbohydrate là những hợp chất hữu cơ tạp chức, thường có công thức chung là Cn(H2O)m.
4) Chất béo không phải là carbohydrate.
Số phát biểu đúng là
A. 1. B. 2. C. 3. D. 4.

- Monosaccharide: Là nhóm carbohydrate đơn giản nhất, không bị thuỷ phân. Ví dụ: glucose, fructose.
- Glucose có nhóm chức –CHO, bromine oxi hóa glucose, phản ứng xảy ra làm nước bromine mất màu.
- Carbohydrate là những hợp chất hữu cơ tạp chức, thường có công thức chung là Cn(H2O)m.
- Chất béo là triester của glycerol và acid béo.

1) Glucose và fructose không tham gia phản ứng thuỷ phân.
→ Đúng. Glucose và fructose là monosaccharide nên không tham gia phản ứng thuỷ phân.
2) Có thể phân biệt glucose và fructose bằng nước bromine.
→ Đúng. Glucose làm mất màu nước bromine, fructose không làm mất màu nước bromine.
3) Carbohydrate là những hợp chất hữu cơ tạp chức, thường có công thức chung là Cn(H2O)m.
→ Đúng.
4) Chất béo không phải là carbohydrate.
→ Đúng. Chất béo là triester của glycerol và acid béo không phải là carbohydrate.
Số phát biểu đúng là 4.
→ Chọn D.
Câu hỏi trang 20 Bài tập2
Trả lời câu hỏi Bài tập 2 trang 20
Cho biết mỗi nhận xét dưới đây là đúng hay sai?
a) Glucose và fructose là đồng phân cấu tạo của nhau.
b) Glucose và fructose là carbohydrate thuộc nhóm monosaccharide.
c) Có thể phân biệt glucose và fructose bằng thuốc thử Tollens.

a) Những hợp chất khác nhau nhưng có cùng công thức phân tử được gọi là những chất đồng phân.
b) Monosaccharide: Là nhóm carbohydrate đơn giản nhất, không bị thuỷ phân. Ví dụ: glucose, fructose.
c) Glucose phản ứng với thuốc thử Tollens tạo thành kết tủa trắng bạc.
Tuy không có nhóm -CHO trong phân tử, nhưng trong môi trường kiềm, fructose chuyển hoá thành glucose, nên có phản ứng với thuốc thử Tollens tương tự glucose.

a) Glucose và fructose là đồng phân cấu tạo của nhau.
→ Đúng. Glucose và fructose đều có công thức phân tử là C6H12O6 nên glucose và fructose là đồng phân cấu tạo của nhau.
b) Glucose và fructose là carbohydrate thuộc nhóm monosaccharide.
→ Đúng. Glucose và fructose là monosaccharide.
c) Có thể phân biệt glucose và fructose bằng thuốc thử Tollens.
→ Sai. Glucose phản ứng với thuốc thử Tollens tạo thành kết tủa trắng bạc. Trong môi trường kiềm của thuốc thử Tollens, fructose chuyển hóa thành glucose nên vẫn xảy phản ứng, tạo kết tủa trắng bạc. Do đó không thể dùng thuốc thử Tollens để phân biệt glucose và fructose.
Câu hỏi trang 20 Bài tập3
Trả lời câu hỏi Bài tập 3 trang 20
Đun nóng dung dịch chứa 10 gam glucose với dung dịch AgNO3 (dư) trong ammonia thấy có kim loại bạc tách ra. Tính khối lượng kim loại bạc tối đa thu được trong thí nghiệm.

Glucose phản ứng với dung dịch AgNO3/NH3 tạo thành kết tủa Ag.
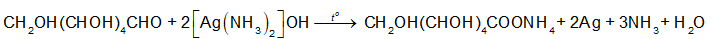

Ta có: \({{\rm{n}}_{{{\rm{C}}_{\rm{6}}}{{\rm{H}}_{{\rm{12}}}}{{\rm{O}}_{\rm{6}}}}} = \frac{{10}}{{180}} = \frac{1}{{18}}{\rm{ (mol)}}\)
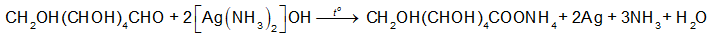
Theo phương trình hóa học: \({{\rm{n}}_{{\rm{Ag}}}}{\rm{ = 2}}{{\rm{n}}_{{{\rm{C}}_{\rm{6}}}{{\rm{H}}_{{\rm{12}}}}{{\rm{O}}_{\rm{6}}}}} = 2 \times \frac{1}{{18}}{\rm{ = }}\frac{1}{9}{\rm{ (mol)}}\)
\( \Rightarrow {{\rm{m}}_{{\rm{Ag}}}}{\rm{ = }}\frac{1}{9} \times {\rm{108}} = 12{\rm{ (g)}}\)
