Bài 5 trang 83 Tài liệu dạy - học Hóa học 8 tập 2. Nồng độ mol của dung dịch thu được là : \({CM_{.CuS{O_4}}} = {{{n_{CuS{O_4}}}} \over {{V_{{\rm{dd}}}}}} = {{0,2} \over {0,5}} = 0,4M\). Bài 42. Nồng độ dung dịch

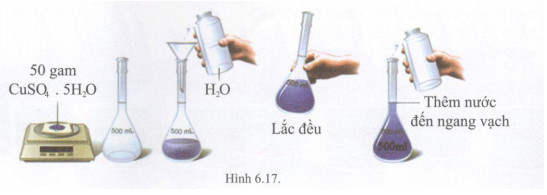
Cho bài tập thực nghiệm như hình 6.17 và tính nồng độ dung dịch thu được.

Advertisements (Quảng cáo)
Học sinh vào phòng thí nghiệm và làm thí nghiệm như hình vẽ.
Số mol của \(CuS{O_4}.5{H_2}O\) là :
\(\eqalign{ & {n_{CuS{O_4}.5{H_2}O}} = {{{m_{CuS{O_4}.5{H_2}O}}} \over {{M_{CuS{O_4}.5{H_2}O}}}} \cr&\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\,= {{50} \over {160 + 5.18}} = 0,2mol \cr & \Rightarrow {n_{CuS{O_4}}} = {n_{CuS{O_4}.5{H_2}O}} = 0,2mol \cr} \)
Nồng độ mol của dung dịch thu được là :
\({CM_{.CuS{O_4}}} = {{{n_{CuS{O_4}}}} \over {{V_{{\rm{dd}}}}}} = {{0,2} \over {0,5}} = 0,4M\)
