Khi đun hồi lưu (đun sôi có sinh hàn để ngưng tụ chất lỏng bay hơi trở lại bình phản ứng ) một hỗn hợp gồm 1 mol axit axetic và 1 mol 3-metylbutan-1-ol(ancol isoamylic ) có axit H2SO4 làm xúc tác, đến khi đạt trạng thái cân bằng hoá học thu được 0,67 mol isoamyl axetat (dầu chuối ).
a) Tính hằng số cân bằng của phản ứng este hoá trong điều kiện trên.
b) Nếu đun hỗn hợp gồm 2 mol axit axetic và 1 mol ancol isoamylic trong điều kiện như trên thì khi đạt trạng thái cân bằng hoá học thu được bao nhiêu mol este?
c) Nếu đun hỗn hợp gồm 1 mol axit axetic và 1 mol ancol isoamylic trong điều kiện như trên thì khi đạt trạng thái cân bằng hoá học thu được bao nhiêu mol este?
Có nhận xét gì về kết quả trong hai trường hợp a và b?
Hướng dẫn
a) Phương trình hoá học:
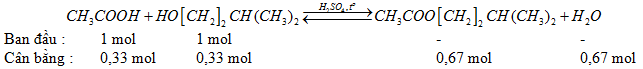
Advertisements (Quảng cáo)
\(\eqalign{ & {K_{cb}} = {{0,67.0,67} \over {{{(0,33)}^2}}} = 4,12 \cr & \cr} \)
b)
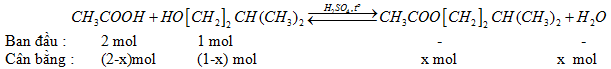
\({K_{cb}} = {{{x^2}} \over {(2 - x)(1 - x)}} = 4,12\)
Giải phương trình được: x = 0,85 mol.
c) Tương tự, số mol este thu được bằng 0,85 mol.
Như vậy, khi tăng số mol axit hoặc tăng số mol ancol thì số mol este thu được nhiều hơn. Có nghĩa là muốn thu được este với hiệu suất cao hơn cần lấy dư một trong hai chất phản ứng.
