Điện phân dung dịch \(CdS{O_4}\) (các điện cực trơ) nhận thấy ở một điện cực có kim loại bám vào, ở điện cực còn lại có khí thoát ra.
a) Hãy cho biết phản ứng hoá học xảy ra ở các điện cực và viết phương trình hoá học của sự điện phân.
b) Trong điều kiện công nghiệp, người ta điện phân dung dịch \(CdS{O_4}\) với cường độ dòng điện là 25 kA. Tính khối lượng kim loại Cd điều chế được sau 12 giờ. (MCd = 112,5 g/mol)
c) Tính thể tích khí (đktc) thu được ở điện cực còn lại.
Đáp án
a) Các phản ứng hoá học xảy ra trong quá trình điện phân:
\( \bullet \) Ở catot xảy ra sự khử các ion: \(C{d^{2 + }}:C{d^{2 + }} + 2e \to Cd\)
\( \bullet \) Ở anot xảy ra sự oxi hoá các phân tử \({H_2}O\), giải phóng khí \({O_2}\):
\(2{H_2}O \to 4{H^ + } + {O_2} + 4e\)
Advertisements (Quảng cáo)
\( \bullet \) Phương trình hoá học của sự điện phân:
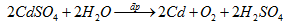
b) Khối lượng kim loại Cd điều chế được
\({m_{Cd}} = {{112,{{5.25.10}^3}.12.3600} \over {2.96500}} = 629,{5.10^3}\left( g \right) = 629,5kg\)
c) Thể tích khí oxi thu được ở anot:
Theo phương trình hoá học của sự điện phân: \({n_{{O_2}}} = {1 \over 2}{n_{Cd}}\)
Thể tích khí oxi thu được ở anot:
\({V_{{O_2}}} = {{22,4.629,{{5.10}^3}} \over {112,5.2}} = 62,{67.10^3}\)(lít) = 62,67 \({m^3}.\)
