Đun nóng hỗn hợp A gồm 1 mol axit axetic và 1 mol ancol etylic (có 0,10 mol axit sunfuric làm xúc tác ) đến khí đạt trạng thái cân bằng thu được hỗn hợp B trong đó có 0,67 mol etylic axetat.
a) Tính phần trăm khối lượng của mỗi chất trong hỗn hợp B
b) Tính hằng số cân bằng của phản ứng.
c) Muốn thu được lượng este nhiều hơn thì cần phải làm gì ? giải thích.

a)
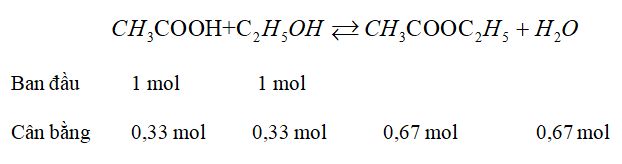
Khối lượng của hỗn hợp ban đầu m = 60 + 46 + 0,10.98 = 115,80 (g)
Khối lượng este = 0,67.88 =58,96 (g)
Khối lượng của nước = 0,67.18 =12,06 (g)
Khối lượng của axit axetic chưa phản ứng = 0,33. 60 = 19, 80 (g)
Advertisements (Quảng cáo)
Khối lượng ancol chưa phản ứng = 0,33. 46 = 15,18 (g)
Khối lượng axit sunfuric = 0,10.98 =9,80 (g)
Khối lượng hỗn hợp trước phản ứng = 115,80 g = khối lượng hỗn hợp sau phản ứng
\(\% {m_{axit\,axetic}} = 17,10\%\)
\(\% {m_{ancol}} = 13,10\% \)
%meste = 50,91 %; \(\% {m_{nuoc}} = 10,41\% \)
\(\% {m_{axit\,\,s{\rm{unfic}}}} = 8,46\% \)
b) Tính hằng số cân bằng
\(\eqalign{ & {K_{cb}} \cr & {K_{cb}} = {{0,67.0,67} \over {0,33.0,33}} = 4,122 \cr} \)
c) Để tăng lượng este cần làm cho cân bằng chuyển dịch theo chiều từ trái sang phải, vậy phải tăng số mol của một trong hai chất (axit axetic hay ancol etylic) hoặc chưng cất bởi lượng este trong quá trình phản ứng do nó có nhiệt độ sôi thấp (thấp hơn axit và ancol).
